
| A、电解池中阳极失去电子,发生还原反应 |
| B、用惰性电极电解饱和食盐水时,阳极的电极反应式为:2C1--2e一=C12↑ |
| C、粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| D、在镀件上镀银时,阳极为镀件,电解质溶液为AgNO3溶液 |


科目:高中化学 来源: 题型:
| A、①②④ | B、②④ |
| C、③④⑤ | D、③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5mol/L |
| B、0.8mol/L |
| C、1mol/L |
| D、1.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AgNO3 |
| B、HCl |
| C、NaOH |
| D、NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
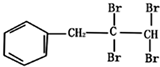 与NaOH的水溶液共热的化学方程式为
与NaOH的水溶液共热的化学方程式为
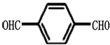 )的氧化产物“对苯二甲酸”与“乙二醇”发生缩聚,生成的聚酯纤维(涤纶)的结构简式为
)的氧化产物“对苯二甲酸”与“乙二醇”发生缩聚,生成的聚酯纤维(涤纶)的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 | 时间 浓度 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| ① | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| ② | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| ③ | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| ④ | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| t1~t2 | t2~t3 | t3~t4 | t4~t5 | t5~t6 |
| K1 | K2 | K3 | K4 | K5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com