
| ||
| 2×0.96 |
| 64 |
| 0.56 |
| 56 |
| 1 |
| 250 |


科目:高中化学 来源: 题型:
A、K=
| ||
B、K=
| ||
C、K=
| ||
D、K=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 制取少量蒸馏水 |
B、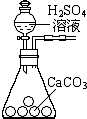 实验室制取CO2 |
C、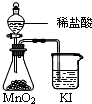 比较MnO2、Cl2、I2的氧化性 |
D、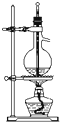 实验室用乙醇和浓硫酸制乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解池中阳极失去电子,发生还原反应 |
| B、用惰性电极电解饱和食盐水时,阳极的电极反应式为:2C1--2e一=C12↑ |
| C、粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
| D、在镀件上镀银时,阳极为镀件,电解质溶液为AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
物质 T/℃n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| 平衡时 | 2.000 | 0.040 | 0.030 | 0.030 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两途径最终到平衡时,体系内混合气的百分组成相同 |
| B、两途径最终达到平衡时,体系内混合气的百分组成不同 |
| C、达平衡时,途径I的反应速率v(A)等于途径II的反应速率v(A) |
| D、达平衡时,途径I所得混合气的密度与途径II所得混合气密度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烷和甲酸甲酯 |
| B、乙烷和乙醇 |
| C、苯和苯甲酸 |
| D、乙炔和苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com