
【题目】下列关于有机物的说法正确的有几个
①苯的邻位二氯取代物只有一种②甲烷的二氯取代产物有两种③C3H8的二氯代物共有4种④可用酸性高锰酸钾溶液除去乙烷中的乙烯⑤分子式是C4H8的烃分子中一定含有碳碳双键⑥将苯滴入溴水中,振荡后水层接近无色是因为苯与溴水发生了取代反应⑦苯的同系物是分子中仅含有一个苯环的所有烃类物质⑧lmolCH5+中含11NA个电子⑨1mol-OH中含9NA个电子⑩菲的结构简式为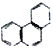 ,它与硝酸反应,可生成5种一硝基取代物
,它与硝酸反应,可生成5种一硝基取代物
A. 2个 B. 3个 C. 4个 D. 5个
【答案】C
【解析】①苯的邻位二氯取代物只有一种,正确;②甲烷的二氯取代产物有1种,错误;③C3H8的二氯代物共有4种,正确;④酸性高锰酸钾溶液把乙烯氧化为二氧化碳,除去了乙烯,引入了二氧化碳气体,不能达到提纯目的,④错误;⑤分子式是C4H8的烃分子可能为环烃,不含双键,错误;⑥将苯滴入溴水中,苯萃取溴在上层,物理变化,错误;⑦苯的同系物是分子中仅含有一个苯环的所有饱和烃类物质,错误;⑧lmolCH5+中含11NA个质子、含10NA电子,错误;⑨1mol-OH中含9NA个电子,正确;⑩苯环是平面正六边形,菲具有很高的对称性,沿如图虚线对称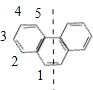 ,有如图所示5种H原子,故菲的一硝基取代物有5种,正确;符合题意选项为①③⑨⑩,正确选项C。
,有如图所示5种H原子,故菲的一硝基取代物有5种,正确;符合题意选项为①③⑨⑩,正确选项C。


科目:高中化学 来源: 题型:
【题目】某无色溶液中存在大量的Ba2+、NH4+、Cl-,该溶液中还可能大量存在的离子是( )
A. Fe3+B. CO32-C. Mg2+D. OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、在一个固定体积的密闭容器中,加入2 mol A和1 mol B,发生反应:2A(g)+B(g)![]() 3C(g)+D(g),达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度(用“大于”“小于”或“等于”表示)。
3C(g)+D(g),达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度(用“大于”“小于”或“等于”表示)。
(1)加入1 mol A和1 mol B时,C的平衡浓度_________W mol·L-1。
(2)加入2mol A、1mol B、3mol C、1mol D时,C的平衡浓度_________W mol·L-1。
(3)加入3 mol C和1 mol D时,C的平衡浓度_________W mol·L-1。
II、现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“<”或“=”)。(下列空填“增大”“减小”或“不变”,)
(2)若加入B(体积不变),则A的转化率_________。
(3)若升高温度,则平衡时B、C的浓度之比 c(B)/c(C)将_________。
(4)若加入催化剂,平衡时气体混合物的总物质的量_________。
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a升CO2气体通过足量Na2O2所得的气体与b升NO相混和时,可得到c升气体(相同状况),以下表达式中错误的是( )
A. 若a<b,则c>0.5(a+b) B. 若a>b,则c=0.5(a+b)
C. 若a=b,则c=0.5(a+b) D. 若a<b,则c<0.5(a+b)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中的各字母表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A是金属单质;B是淡黄色固体; C、D、E为无色气体,D能使湿润的红色石蕊试纸变蓝;H是无色液体。

(1)写出下列各物质的化学式:
B:____________________________;F:_______________________ 。
(2)写出D→E反应的化学方程式为:______________________ 。
(3)写出G→E反应的离子方程式:________________________________ ;若该反应中转移电子总数为9.03 ×1023 ,则被还原的G为___________________ g 。
(4)写出实验室制取D的化学方程式________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常利用SiO2 和碳反应来制取硅,写出反应的化学方程式___________________。
工业上还可以利用镁制取硅,反应为2Mg+SiO2 = 2MgO+Si,同时会发生副反应:2Mg + Si = Mg2Si。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2和H2O(g)的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用________(填序号)。
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通一段时间X气体,再加热反应物,其理由是 ___________________________;当反应引发后,移走酒精灯,反应能继续进行,其原因是______________________。
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,产生此现象的原因是副产物Mg2Si遇盐酸迅速反应生成SiH4(硅烷)气体,然后SiH4自燃.用化学方程式表示这两个反应①________________________②___________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究一包Na2O2样品是否已经变质:取少量样品,将其溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了m g样品,并设计用下图装置来测定过氧化钠的质量分数。
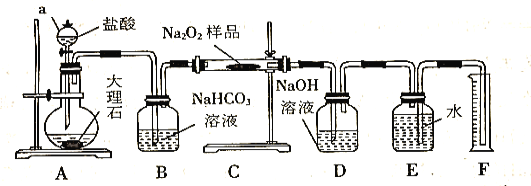
①装置D的作用是_________________________________;
②将仪器连接好以后,必须进行的第一步操作是_________________________________;
③写出装置C中发生主要反应的化学方程式_________________________________;
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是_______________(填序号);
a.读取气体体积前,需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低点相平时读取量筒中水的体积
⑤读出量筒内水的体积后,将其折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com