
【题目】【物质结构与性质】 (15 分)
钒、砷均属于第四周期元素,最高正价均为+5。
I .高纯度砷可用于生产具有“半导体贵族”之称的新型半导体材料GaAs,砷与氯气反应可得到 AsCl3、AsCl5两种氯化物。
(1)AsCl3分子的空间构型是 ,中心原子杂化类型是 。两种氯化物分子中属于非极性分子的是 。
(2)Ga与As相比,第一电离能较小的元素是 ,GaAs中砷的化合价为 。
II.钒是一种重要的战略金属,其最主要的用途是生产特种钢,其化合价有+5、+4、+3、+2等,工业上从炼钢获得的富钒炉渣中(内含 V2O5)提取钒的过程如下。
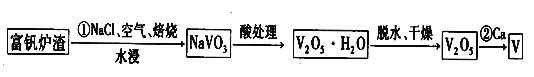
(3)基态钒原子的价电子排布式为 ,写出反应①的化学方程式: 。
(4)已知单质钒的晶胞为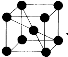 ,则 V 原子的配位数是 ,假设晶胞的边长为 a cm, 密度为 ρ g/cm3,则钒的相对原子质量为 。
,则 V 原子的配位数是 ,假设晶胞的边长为 a cm, 密度为 ρ g/cm3,则钒的相对原子质量为 。
【答案】(1)三角锥形;sp3杂化;AsCl5
(2)Ga;-3
(3)3d34s2;2V2O5+4NaCl+O2![]() 4NaVO3+2Cl2
4NaVO3+2Cl2
(4)8;NAρa3/2
【解析】
试题分析:(1)AsCl3分子的价层电子对数为4,含有一对孤对电子,所以立体构型为三角锥形,其中As的杂化轨道类型为sp3。AsCl3分子属于极性分子,AsCl5分子为正六面体构型,属于非极性分子。
(2)同周期自左向右原子半径逐渐减下,则原子半径Ga大于As,由于As的4p轨道电子处于半充满状态,稳定性强,所以第一电离能较小的元素是Ga;GaAs中砷的化合价为-3价。
(3)V为23号元素,根据构造原理知基态钒原子的价电子排布式为3d34s2,根据题给流程知V2O5、NaCl在空气中焙烧生成NaVO3和氯气,化学方程式为2V2O5+4NaCl+O2 ![]() 4NaVO3+2Cl2。
4NaVO3+2Cl2。
(4)根据单质钒的晶胞结构知V 原子的配位数是8,利用切割法计算每个晶胞中含有V的数目为8×1/8+1=2,则1mol晶胞的质量为2Mg,晶胞的边长为 a cm,则1mol晶胞的体积为NAacm3 ,晶胞密度为 ρ g/cm3,则钒的相对原子质量为NAρa3/2。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在一个4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:3 A(g)+B(g) ![]() 2 C(g)+x D(g),经2min后达到平衡状态,生成了2mol C,经测定D的浓度为0.5molL-1,下列判断正确的是( )
2 C(g)+x D(g),经2min后达到平衡状态,生成了2mol C,经测定D的浓度为0.5molL-1,下列判断正确的是( )
A.X = 3
B.A的转化率为50%
C.从反应开始到建立平衡,B的反应速率为0.5 molL-1min-1
D.达到平衡时,在相同温度下容器内混合气体的压强是反应前的95%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示。则甲和X不可能是
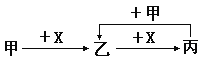
A.甲为c,X为O2 B.甲为SO2,X为NaOH溶液
C.甲为Al2O3,X为NaOH溶液 D.甲为AlCl3,X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是
选项 | 强电解质 | 弱电解质 | 非电解质 |
A | CaCO3 | H2SiO3 | 酒精 |
B | NaCl | NH3 | BaSO4 |
C | Fe | CH3COOH | 蔗糖 |
D | HNO3 | Fe(OH)3 | H2O |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,X与强酸、强碱溶液反应如下,则下列说法正确的是( )
Y![]() X
X![]() Z.
Z.
A.若X为单质铝,则Y的气体产物只能是氢气
B.若X为NaHCO3,则Z一定有CO2
C.若Y、Z为含铝元素的两种盐,则X一定为Al(OH)3
D.若X为乙酸乙酯,则生成物Y、Z中均含有乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ在某一容积为5 L的密闭容器内,加入 0.2 mol的CO和0.2 mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g);ΔH>0反应中CO2的浓度随时间变化情况如下图:
CO2(g)+H2(g);ΔH>0反应中CO2的浓度随时间变化情况如下图: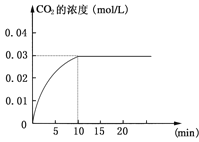
(1)根据上图数据,反应开始至达到平衡时,CO的化学反应速率为v(CO)= mol/(L·min);反应达平衡时,c(H2)=________ mol/L,该温度下的平衡常数K 。
(2) 判断该反应达到平衡的依据是________________。
① CO减少的化学反应速率和CO2减少的化学反应速率相等
② CO、H2O、CO2、H2的浓度都相等
③ CO、H2O、CO2、H2的浓度都不再发生变化
④ 正、逆反应速率都为零
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.1 mol的CO2和0.1 mol的H2,在相同的条件下,反应达平衡时,c(H2O)=_____________mol/L。
Ⅱ、在含有I-、Cl-的混合溶液中,逐滴加入一定量AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关。下列说法正确的是
A. 自来水中加入氯气与污水中加入明矾的原理相同
B. 汽油、甘油、花生油均能发生水解反应和氧化反应
C. 硫酸铜溶液可用于游泳池的消毒是利用了Cu2+能使蛋白质盐析
D. 现代工业生产中的芳香烃来源于石油的催化重整和煤的干馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com