

 );乙烯与水在一定条件下发生加成反应生成B为CH3CH2OH,乙醇被酸性重铬酸钾溶液氧化反生成C为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成D为CH3COOCH2CH3,以此解答该题.
);乙烯与水在一定条件下发生加成反应生成B为CH3CH2OH,乙醇被酸性重铬酸钾溶液氧化反生成C为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成D为CH3COOCH2CH3,以此解答该题. );乙烯与水在一定条件下发生加成反应生成B为CH3CH2OH,乙醇被酸性重铬酸钾溶液氧化反生成C为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成D为CH3COOCH2CH3,
);乙烯与水在一定条件下发生加成反应生成B为CH3CH2OH,乙醇被酸性重铬酸钾溶液氧化反生成C为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成D为CH3COOCH2CH3, ;C的结构简式为CH3COOH,其含有的官能团为羧基,
;C的结构简式为CH3COOH,其含有的官能团为羧基, ;羧基;
;羧基;| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


科目:高中化学 来源: 题型:
 某溶液中可能含有,OH-、CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图.下列判断正确的是( )
某溶液中可能含有,OH-、CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图.下列判断正确的是( )| A、原溶液中一定含有Na2SO4 |
| B、原溶液中一定含有的阴离子是OH-,CO32-,SiO32-,AlO2- |
| C、反应后形成的溶液溶质为NaCl |
| D、原溶液中含有CO32-与AlO2-的物质的量比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(CH3COO-)>c(Na+) |
| B、c(CH3COO-)<c(Na+) |
| C、c(CH3COO-)=c(Na+) |
| D、无法确定c(CH3COO-)与c(Na+)的关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
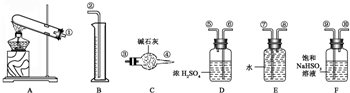
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
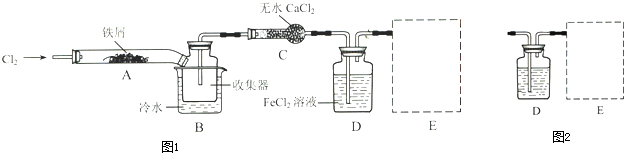
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 氯气是一种重要的化工原料.如图为实验室制取氯气的装置.请回答:
氯气是一种重要的化工原料.如图为实验室制取氯气的装置.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com