
【题目】人们将化合物分为电解质和非电解质两类,下列属于电解质的是
A. 氯气 B. 金属铝 C. 氯化钠 D. 汽油
科目:高中化学 来源: 题型:
【题目】在生产生活中,酸碱中和及溶液酸碱性研究具有十分重要的意义。
(1)常温下,将2种一元酸分别和NaOH溶液等体积混合,实验数据如下:
组别 | c(一元酸) | c(NaOH) | 混合溶液的pH |
甲 | c(HY)=0.1mol/L | 0.1mol/L | pH=7 |
乙 | c(HZ)=0.1mol/L | 0.1mol/L | pH=9 |
①甲组实验中HY为_________(填强、弱)酸,0.1 moL/L HY溶液的pH=_____________。
②乙组实验中发生反应的离子方程式为_________________________________。
③乙组实验所得溶液中由水电离出的c(OH-)=________ mol/L。
(2)常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL0.1000mol/LHCl溶液和20.00mL 0.1000mol/LCH3COOH溶液,得到2条滴定曲线,如下图所示。

①滴定HCl溶液的曲线是___________(填“I”或“Ⅱ”);
②a=__________ mL。
③c(Na+)=c(CH3COO-)的点是_____________。
④E点对应离子浓度由大到小的顺序为_________________。
(3)将一定量某浓度的NaOH溶液,加入MgCO3悬浊液中,可以生成更难溶的Mg(OH)2。该反应的离子方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G、L、I九种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E、B与G、D与L分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍。C和D的最外层电子数之和为11。请回答下列问题:
(1)以上非金属元素中所形成的最简单气态氢化物稳定性最弱的是(填化学式)______,E、F、L所形成的简单离子的半径由小到大的顺序为(用离子符号表示)_____。
(2)由L、I两元素可按原子个数比1∶1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为____。
(3)少量固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有淡黄色沉淀产生,并无气泡冒出,请结合信息写出该反应的离子方程式 _____________________________。
(4)由A、B、C、D按原子个数比4∶1∶1∶2形成一种化合物Y,则Y的化学式为_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸是实验室常用的一类物质,下列关于酸的认识和判断正确的是
A. HCl、CH3COOH均为含氧酸 B. 稀H2SO4具有强氧化性
C. 酸洒到实验台上,应用NaOH溶液处理 D. 铁、铝遇到冷的浓硫酸会发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
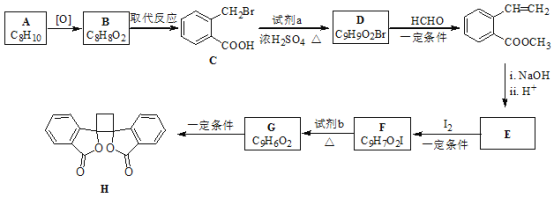
已知:
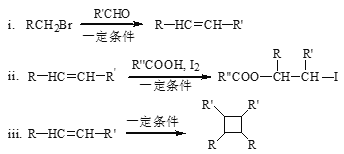
(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是__________。
(2)B的结构简式是__________。
(3)由C生成D的化学方程式是______________________________________________。
(4)由E与I2在一定条件下反应生成F的化学方程式是__________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是__________。
(5)试剂b是___________。
(6)下列说法正确的是___________(选填字母序号)。
a. G存在顺反异构体
b. 由G生成H的反应是加成反应
c. 1 mol G最多可以与1 mol H2发生加成反应
d. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
(7)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成,写出合成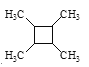 的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)__________。
的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是极其重要的化工原料,工业上将产生的NO2在密闭容器中用水多次反复循环吸收制备硝酸。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:_______
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。

①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至____后,迅速关闭K1,观察到U形管内的现象是______。
②装置Ⅲ中发生反应的化学方程式为__________。
③蘸NaOH溶液的棉花团的作用是____________。
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,长玻璃管中并未充满液体。设计简单方法检验长玻璃管中的气体是否含NO______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸晶体(H2C2O4·2H2O)的熔点为101℃,170℃分解。下列选用的装置和药品能达到实验目的的是
A | B | C | D |
|
|
|
|
制取SO2 | 制取NO2 | H2C2O4·2H2O分解 | 分离苯与溴苯 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的表达正确的是
A. 1s电子云呈球形,表示电子绕原子核做圆周运动
B. 钠原子由1s22s22p63p1→ls22s22p63p1时,原子释放能量,由基态转化成激发态
C. 因氧元素的电负性比氮元素的大,故氧原子的第一电离能比氮原子的大
D. 基态Fe原子的外围电子排布图为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2的熔点为-54.1 ℃,沸点为69.1 ℃,极易水解,遇潮湿空气会产生白雾。
(1)化合物SO2Cl2中S元素的化合价是__________。
(2)实验室中制备氯气时为得到干燥纯净的氯气,应将气体依次通过盛有_______和_______的洗气瓶。
(3)用如图所示装置制备SO2Cl2。

①B中冷凝水从__________ (填“m”或“n”)口进入。
②C中的药品是______。目的一是吸收外界空气中的水蒸气,目的二是:_______________。
③向A所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl-,写出SO2Cl2与H2O反应的化学方程式:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com