
已知16 g A与20 g B恰好完全反应,生成w g C和4 g D.在相同条件下,8 g A和15 g B混合反应,生成D和0.125 mol C物质,求C的摩尔质量是________.
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
(10分)(1)①根据图示,写出反应的热化学方程式: 。
②根据如图所示情况,判断下列说法中正确的是( )
A.其热化学方程式为:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+41kJ/mol
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其反应热值小于41 kJ/mol
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是 。
(3)如图是某温度下,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为: 。
a、b两条曲线产生区别的原因很可能是 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年云南蒙自高中高二上学期期中考试化学试卷 题型:填空题
(10分)(1)①根据图示,写出反应的热化学方程式: 。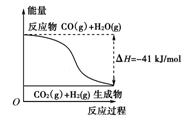
②根据如图所示情况,判断下列说法中正确的是( )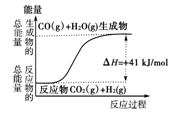
| A.其热化学方程式为:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+41 kJ/mol |
| B.该反应为吸热反应 |
| C.该反应为放热反应 |
| D.当H2O为液态时,其反应热值小于41 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:2013届云南蒙自高中高二上学期期中考试化学试卷 题型:填空题
(10分)(1)①根据图示,写出反应的热化学方程式: 。

②根据如图所示情况,判断下列说法中正确的是( )

A.其热化学方程式为:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+41 kJ/mol
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其反应热值小于41 kJ/mol
(2)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是 。
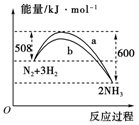
(3)如图是某温度下,N2与H2反应过程中能量变化的曲线图。该反应的热化学方程式为: 。

a、b两条曲线产生区别的原因很可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)由周期表中前20号元素组成的单质X2、Y和化合物Z的有关信息如下表,X2、Y 和Z之间的转化关系如下图(其他无关物质已略去)。请回答下列问题:
| 单质X2 | 标准状况下密度为3.17 g?L-1 |
| 单质Y | 通常状况下为一种淡黄色固体 |
| 化合物Z | 焰色反应呈紫色(透过蓝色钴玻璃观察) |
| 常温下0.1 mol?L-1 Z的水溶液pH=13 |
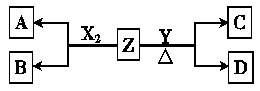
(1) Z的电子式为 。
(2)已知16 g固态单质Y在空气中完全燃烧放出148 kJ热量,则该反应的热化学方程式为 。
(3)已知C能与稀硫酸反应生成能使品红溶液褪色的气体,D中所含阴、阳离子的电子层排布相同。
①常温下D的水溶液pH>7,其原因是(用离子方程式表示) 。
②将20 mL 0.5 mol?L-1 C溶液逐滴加入20 mL 0.2 mol?L-1 KMnO4溶液(硫酸酸化)中,溶液恰好变为无色。写出该反应的离子方程式: 。
(4)①用石墨和铁作电极,在隔膜电解槽中电解A的溶液,阳极产生X2,电解A溶液的离子方程式为 。
②实验室常用含X元素的一种化合物E制取O2 ,工业上用无隔膜电解槽(石墨和铁作电极,温度为42~44 ℃)电解A的溶液生产化合物E。假设电解时电解槽进液口溶液中A 的浓度为2 mol?L-1,液口溶液中A的浓度为1.6 mol?L-1(进出口流量相同),则液口溶液中E的浓度为
mol?L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
(16分)(1)在容积为VL的密闭容器中发生2NO2(g)![]() 2NO(g)+O2(g)的反应。
2NO(g)+O2(g)的反应。 反应过程中NO2的物质的量随时间变化的状况如图所示。
反应过程中NO2的物质的量随时间变化的状况如图所示。
①不能说明该反应已达到平衡状态的是 ( )
A.V正(NO2)=2V逆(O2)
B.C(NO2)=C(NO)
C.气体的平均摩尔质量不变
D.NO的体积分数保持不变
②若曲线A和B表示的是该反应在某不同条件下的反应状况,则该不同条件是( )
A.有、无催化剂 B.温度不同 C.压强不同
③写出该反应的化学平衡常数K的表达式________________,并比较K800℃________________K850℃ (填>、<或=)。
(2)在以煤为主要原料的合成氨工业中,原料气氢气常用下述方法获得:
①C+H2O(g)![]() CO+H2;
CO+H2;
②CO+H2O(g)![]() CO2+H2 ;
CO2+H2 ;
已知CO(g)+1/2O2(g)=CO2(g);△H=-283.0kJ/mol ;
H2(g)+1/2O2(g)=H2O(g); △H=-285.8kJ/mol;写出上述CO与H2O(g)反应的热化学方程式。
![]() (3)处理含汞废水的方法很多。下面是常用的两种方法,汞的回收率很高。
(3)处理含汞废水的方法很多。下面是常用的两种方法,汞的回收率很高。
![]()
① 置换法:用废铜屑处理含Hg2+的废水。反应的离子方程式为________________。
② 化学沉淀法:用硫化钠处理含Hg(NO3)2的废水,生成HgS沉淀。已知Ksp(HgS) =1.6×10―52,当废水中c(S2―)=1×10―5mol/L时,c(Hg2+)=________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com