
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按如图所示装置进行实验(部分夹持仪器及加热装置未画出)。
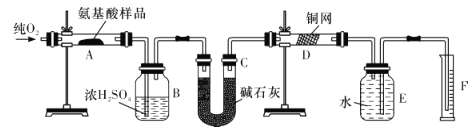
请回答下列有关问题:
(1)在安装E、F装置前,先要通入一段时间的氧气,其理由是_________。
(2)上述装置图中需要加热的仪器有________(填字母代号,下同),操作时应先点燃_____处的酒精灯。
(3)D装置的作用是_______________。
(4)A装置中发生反应的化学方程式是______________。
(5)读取N的体积时,应注意:①__________;②____________。
(6)实验中测得N2的体积为VmL(已折算成标准状况下)。为确定此氨基酸的分子式,还需要的有关数据有______(填字母代号)。
A.生成二氧化碳气体的质量 B.生成水的质量
C.通入氧气的体积 D.氨基酸的相对分子质量
【答案】 赶走装置中的N2、H2O、CO2等气体 AD D 吸收未反应完的氧气,保证最终测得的体积是N2的体积 ![]() 恢复到室温 上下移动量筒,使E、F装置中液面相平;读数时视线与量筒中凹液面最低处相切 ABD
恢复到室温 上下移动量筒,使E、F装置中液面相平;读数时视线与量筒中凹液面最低处相切 ABD
【解析】(1)在安装E、F装置前,先要通入一段时间的氧气,其理由是赶走装置中的N2、H2O、CO2等气体;(2)上述装置图中需要加热的仪器有硬质玻璃管AD,操作时应先点燃D处的酒精灯先给铜网加热;(3)D装置的作用是吸收未反应完的氧气,保证最终测得的体积是N2的体积;(4)A装置中氨基酸(CxHyOzNp)完全燃烧生成二氧化碳、水和氮气,发生反应的化学方程式是![]() ;(5)读取N的体积时,应注意:①恢复到室温;②上下移动量筒,使E、F装置中液面相平;读数时视线与量筒中凹液面最低处相切;(6)实验中测得N2的体积为VmL(已折算成标准状况下)。为确定此氨基酸的分子式,根据反应方程式
;(5)读取N的体积时,应注意:①恢复到室温;②上下移动量筒,使E、F装置中液面相平;读数时视线与量筒中凹液面最低处相切;(6)实验中测得N2的体积为VmL(已折算成标准状况下)。为确定此氨基酸的分子式,根据反应方程式![]() ,还需要的有关数据有二氧化碳气体的质量或物质的量、生成的水的质量或物质的量、氨基酸的相对分子质量等,答案选ABD。
,还需要的有关数据有二氧化碳气体的质量或物质的量、生成的水的质量或物质的量、氨基酸的相对分子质量等,答案选ABD。


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:
【题目】氢化钙可以作为生氢剂(其中CaH2中氢元素为﹣1价),反应方程式如下:CaH2+2H2O=Ca(OH)2+2H2↑,其中水的作用是( )
A.既不是氧化剂也不是还原剂
B.是氧化剂
C.是还原剂
D.既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁矿石(若只含铁的氧化物和SiO2)取36g溶于过量的稀盐酸中,过滤、洗涤、干燥后得5.6g不溶物,向得到的滤液中加入足量的NaOH溶液,过滤、洗涤后将沉淀灼烧,得32g红棕色固体.根据题意下列结论不正确的是( )
A. 由铁矿石转化为红棕色固体的过程中发生了氧化还原反应
B. 溶于盐酸后得到的滤液中n(Fe2+):n(Fe3+)=1:1
C. 铁矿石中的铁的氧化物的化学式一定是Fe3O4
D. 若稀盐酸为3.0molL﹣1 400mL,反应前后体积变化忽略不计,则滤液中剩余H+的物质的量浓度是0.5molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】晶须是由高纯度单晶生长而成的微纳米级的短纤维,工业应用的晶须主要是在人工控制条件下合成。
碳酸镁晶须(MgCO3·nH2O,n = 1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域。制取碳酸镁晶须的步骤如图:
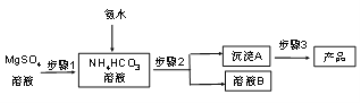
完成下列填空:
(1)步骤1必须将反应的温度控制在50℃,较好的加热方法是_______________________;氨水、硫酸镁、碳酸氢铵三者反应,除生成MgCO3·nH2O沉淀外,同时生成的产物还有______________________________________。
(2)步骤2是__________、洗涤,检验沉淀A已洗涤干净的方法是_____________________。
为测定碳酸镁晶须产品中n的值,某兴趣小组设计了如下装置,并进行了三次实验。(不考虑稀盐酸的挥发性)
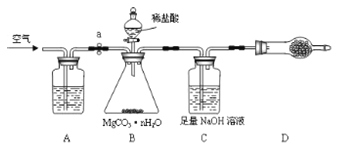
(3)装置A中盛放的溶液是_____________。装置D中盛放的固体是___________________,其作用是_________________________________。
(4)若三次实验测得每1.000g碳酸镁晶须产生的CO2平均值为a mol,则n值为__________________(用含a的代数式表达)。
(5)下列选项中,会造成实验结果偏大的是____________。 (选填序号)
①实验开始,未先通空气,即称量装置C; ②B中反应结束后,没有继续通空气;
③缺少装置A; ④缺少装置D;
⑤装置B中稀盐酸的滴加速率过快; ⑥装置C中的NaOH溶液浓度过大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在容积不变的密闭容器中进行如下反应:NO(g)+ CO(g)![]()
![]() N2(g)+ CO2(g);△H=-373.2 kJ/mol。右图曲线a表示该反应过程中,NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )
N2(g)+ CO2(g);△H=-373.2 kJ/mol。右图曲线a表示该反应过程中,NO的转化率与反应时间的关系。若改变起始条件,使反应过程按照曲线b进行,可采取的措施是( )
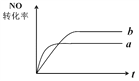
A. 加催化剂 B. 降低温度
C. 增大反应物中NO的浓度 D. 向密闭容器中加入氩气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KNO3固体样品中含有少量的KCl、BaCl2杂质,为了提纯KNO3并分离得到BaCl2,进行如下实验操作:
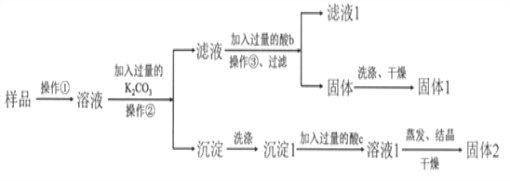
(1)试剂c的化学式是__________,固体1的化学式是__________。加入过量K2CO3所发生反应的化学方程式为________________________________。
(2)结合下图各物质的溶解度曲线可知操作③的名称是_______、________。
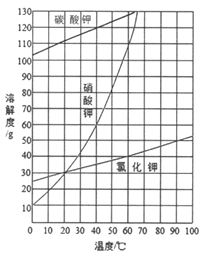
(3)有同学认为操作③之前无需加入过量的酸b,也能得到纯净的固体1,你认为该同学的观点是否正确?_____;并做出相应解释___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度、压强下,1体积X2(气)和3体积Y2(气)化合成2体积的气体化合物,则该气体化合物的化合式为( )
A.XY3
B.XY
C.X3Y
D.X2Y3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常利用铜萃取剂,使溶液中的Cu2+富集进入有机相,再经过进一步的反萃取实现金属铜的沉积、再生,铜萃取剂富集Cu2+的原理如下:
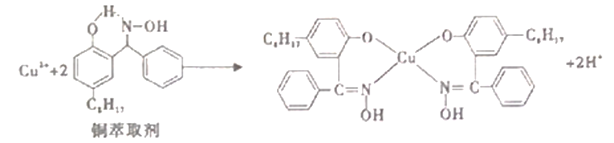
(1)基态铜原子所失去的第一个电子所占据的能层符号是______,价铜离子的简化电子排布式为_________。
(2)铜萃取剂中所含元素的电负性由大到小顺序为______,N原子以_____杂化轨道与O原子形成σ键。
(3)铜萃取剂与Cu2+形成的配合物在水相的溶解度______有机相的溶解度(填“>”、“<”、“=”),该配合物晶体类型为_____ 。
(4)某学生用硫酸铜溶液与氨水做了一组实验:CuSO4溶液![]() 蓝色沉淀
蓝色沉淀![]() 沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式_________;沉淀溶解后溶液中的阳离子内存在的化学健类型有________。
沉淀溶解。写出蓝色沉淀溶于氨水的离子方程式_________;沉淀溶解后溶液中的阳离子内存在的化学健类型有________。
(5)铜的一种氯化物的晶胞如图所示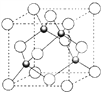 ,该氯化物的化学式_____,Cu和Cl之间最短距离为460.0pm,则晶体密度为______g/cm3。(列式表示)
,该氯化物的化学式_____,Cu和Cl之间最短距离为460.0pm,则晶体密度为______g/cm3。(列式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com