
����Ŀ��������dz����������������������ҩ���̻𣬹�ҵ����ʯ�����Ȼ����Ʊ�����ص�����������ʾ��

��֪���Ȼ�������Ҫ������Ӧ6Ca(OH)2 + 6Cl2![]() 5CaCl2+Ca(ClO)2+6H2O
5CaCl2+Ca(ClO)2+6H2O
���������գ�
(1)��ҵ���������ķ�����__________________��
(2)�Ȼ�������Ҫ���ƽϸ��¶ȣ���Ŀ���У�
��_____________________________�� ������ Cl2 �� Ca(OH)2 ֮��ĸ���Ӧ��
��3�����ȵ���Һ�м����Թ������Ȼ��أ����ܽ���ȫ�������ȴ���д�������ؾ���������д����ط�Ӧ�Ļ�ѧ����ʽ��__________________________________________________��
�õ�������ؾ����п��ܻẬ�������Ȼ��أ���һ���ᴿ�ķ�����_________________��
��4��Ϊ�ⶨ���þ���������صĴ��ȣ��� a g ��Ʒ�� b g �������̻�ϣ����ȸû����һ��ʱ������ʲ��μӷ�Ӧ����ȴ������ʣ������������ظ����ȡ���ȴ��������������¼�������±���
���ȴ��� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
ʣ�����������g�� | c | d | e | e |
�����м��Ȳ���ʱ��Ӧ����������_________�����������ƣ��С�
����ʵ�鲻�ؽ��е���μ��ȵ�ԭ����_______________________________________��
����ij�βⶨ�����������Ϊ-2.98%��д��������һ�����һ�ֿ��������
_______________________________________________________________
���𰸡� ��ⱥ��ʳ��ˮ �ӿ췴Ӧ���� Ca(ClO3)2 + 2KCl �� CaCl2 + 2KClO3�� �ؽᾧ ���� ʣ����������Ѻ��أ�˵�� KClO3 �ѷֽ���ȫ δ�ڸ���������ȴ��ʣ�������ˮ������ʱ�䲻�㣬�����δ��ȫ�ֽ⣨��дһ�֣�
��������(1)��ҵ����������ͨ����ⱥ��ʳ��ˮ�ķ�����õģ��ʴ�Ϊ����ⱥ��ʳ��ˮ��
(2)�Ȼ�������Ҫ���ƽϸ��¶ȣ��������ӿ췴Ӧ���ʣ������� Cl2 �� Ca(OH)2 ֮��ĸ���Ӧ���ʴ�Ϊ���ӿ췴Ӧ���ʣ�
��3�����ȵ���Һ�м����Թ������Ȼ��أ����ܽ���ȫ�������ȴ���д�������ؾ�����������Ӧ�Ļ�ѧ����ʽΪCa(ClO3)2 + 2KCl =CaCl2 + 2KClO3�����õ�������ؾ����п��ܻẬ�������Ȼ��أ�����ͨ���ؽᾧ�ķ��������ᴿ���ʴ�Ϊ��Ca(ClO3)2 + 2KCl =CaCl2 + 2KClO3�����ؽᾧ��
��4�������м��Ȳ���ʱ��Ӧ���������������н��У��ʴ�Ϊ��������
�����ݱ������ݣ�ʣ����������Ѻ��أ�˵�� KClO3 �ѷֽ���ȫ����ʵ�鲻�ؽ��е���μ��ȣ��ʴ�Ϊ��ʣ����������Ѻ��أ�˵�� KClO3 �ѷֽ���ȫ��
����ij�βⶨ�����������Ϊ-2.98%��˵���ⶨ���ƫ�ͣ����ܵ�ԭ���У�δ�ڸ���������ȴ��ʹ�ù��������ļ�����ƫС�����²�õ�����صĺ���ƫ�ͣ���������ػ������У�ʣ�������ˮ������ʱ�䲻�㣬�����δ��ȫ�ֽ�ȣ��ʴ�Ϊ��δ�ڸ���������ȴ����ʣ�������ˮ�����ʱ�䲻��������δ��ȫ�ֽ⣩��


 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д� һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�����������������ʵ�ֵ��ǣ� ��
A.CuO��Cu
B.Fe��FeCl2
C.HNO3��NO2
D.CaCO3��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������Ϊ72����������Ӧ���ɵ�һ�ȴ���ֻ��һ�֣����ǣ�
A������ B��2��������
C������ D��2,2����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ���������ˮ���ص��ǣ� ��
A. ������ˮB. NaCl�������������͵�ζ��
C. �ȵĴ�����Һ��ȥ������D. FeCl3������Һ�����ˮ���Ʊ�Fe(OH)3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ����˵����ȷ���ǣ� ��
A��ֱ������1 nm��100nm֮�������Ϊ����
B���ù��˵ķ�����ȥNaCl��Һ�к��е��������۽���
C��Fe(OH)3������ˮ����˲����ܾ��ȷ�ɢ��ˮ���γ��ȶ��ĺ��ɫ��Һ��
D���ö����ЧӦ����Fe(OH)3�����FeCl3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ���У���̬ԭ����δ�ɶԵ���������������������ͬ��Ԫ���м���
A. 2 B. 3 C. 4 D. 5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£����ڿ��淴ӦX (g) +4Y (g) ![]() 2Z (g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3 (����Ϊ��)���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷքeΪ0.lmol/L��0.4mol/L�� 0.1mol/L���������ж���ȷ����( )
2Z (g)����X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3 (����Ϊ��)���ﵽƽ��ʱ��X��Y��Z��Ũ�ȷքeΪ0.lmol/L��0.4mol/L�� 0.1mol/L���������ж���ȷ����( )
A. c1��c2=4��1 B. ƽ��ʱ��Y��Z����������֮��Ϊ1: 2
C. c1��ȡֵ��ΧΪ0mol/L<c1<0.14mol/L D. X��Y��ת�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʯ�ͻ�����һ�ֲ�ƷA����ϩ��Ϊ��Ҫԭ�Ϻϳ�һ�־��й���ζ������E�������������£�
��1��д������ٵĻ�ѧ����ʽ_______________��Ӧ����__________��
����ڵĻ�ѧ����ʽ______________��Ӧ����__________��
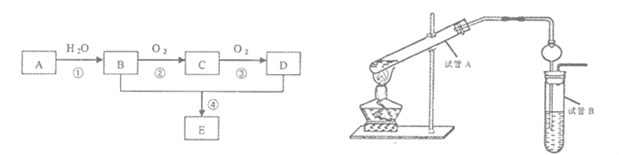
��2��ijͬѧ������ͼװ���Ʊ�����E���ش��������⣺
���Թ�A������Ӧ�Ļ�ѧ����ʽ_______________________��
���Թ�B�е��Լ���______________________�����������������ʵ�������______________����������ƣ����õ�����Ҫ��������Ϊ____________________��
�۲����ұ��Թܵĵ��ܽ���һ����״�������Ϊ_______________________��
��3��Ϊ���Ʊ���Ҫ���л�ԭ�ϡ���������(CH3��CH2Cl)����������λͬѧ��Ƶķ�����
��ͬѧ��ѡ��������������ڹ����������Ʊ���ԭ���ǣ�
CH3��CH3+Cl2 ![]() CH3��CH2Cl+HCl
CH3��CH2Cl+HCl
��ͬѧ��ѡ��ϩ�������Ȼ�����һ���������Ʊ���ԭ���ǣ�
CH2=CH2+HCl��CH3��CH2Cl
����Ϊ������λͬѧ�ķ����У���������____������������ɣ�____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���������Ȼ�ѧ����ʽ��
H2(g) + 1/2 O2(g) ![]() H2O(l) ��H=��300KJ��mol��1
H2O(l) ��H=��300KJ��mol��1
C3H8(g) + 5O2(g) ![]() 3CO2(g) + 4H2O(l) ��H =��2000.0 KJ��mol��1
3CO2(g) + 4H2O(l) ��H =��2000.0 KJ��mol��1
ʵ���������ı���Ļ�����干5mol����ȫȼ��ʱ����5000KJ�����������������ͱ���������ԼΪ�� ��
A. 7:10 B. 3:1 C. 10:7 D. 1:3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com