
【题目】—定条件下,对于可逆反应X (g) +4Y (g) ![]() 2Z (g),若X、Y、Z的起始浓度分别为c1、c2、c3 (均不为零),达到平衡时,X、Y、Z的浓度分別为0.lmol/L、0.4mol/L、 0.1mol/L,则下列判断正确的是( )
2Z (g),若X、Y、Z的起始浓度分别为c1、c2、c3 (均不为零),达到平衡时,X、Y、Z的浓度分別为0.lmol/L、0.4mol/L、 0.1mol/L,则下列判断正确的是( )
A. c1:c2=4:1 B. 平衡时,Y和Z的生成速率之比为1: 2
C. c1的取值范围为0mol/L<c1<0.14mol/L D. X、Y的转化率相等
【答案】D
【解析】A.设X转化的浓度为x,
X(g)+4Y(g)![]() 2Z(g)
2Z(g)
初始浓度:c1 c2 c3
转化浓度:x 4x 2x
平衡浓度:0.1moL·L-1 0.4mol·L-1 0.1mol·L-1
则:c1:c2=(x+0.1moL·L-1):(4x+0.4mol·L-1)=1:4,故A错误;
B.平衡时,正逆反应速率相等,则Y和Z的生成速率之比为4:2,即VY(正):VZ(逆)2:1,故B错误;C、反应为可逆反应,物质不可能完全转化,如反应向正反应分析进行,则0<c1,如反应向逆反应分析进行,则c1<0.15mol·L-1,故有0<c1<0.15mol·L-1,故C错误;D、反应前后X、Y气体的浓度比相同符合反应系数之比,所以达到平衡状态时,转化率相同,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】香天竺葵醇具有温和、香甜的玫瑰花气息,其结构式如图所示。下列有关香天竺葵醇的说法错误的是

A. 分子中含有两种官能团
B. lmol该物质与lmolHBr发生加成反应的产物共有5种(不考虑立体异构)
C. 使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色的原理不同
D. 香天竺葵醇能发生加聚反应和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B的结构简式如下:
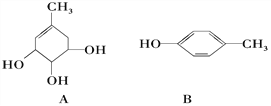
(1)A分子中含有的官能团的名称是___________________________________;
B分子中含有的官能团的名称是_________________________________________。
(2)A能否与氢氧化钠溶液完全反应________________________________________;
B能否与氢氧化钠溶液完全反应__________________________________。
(3)A在浓硫酸作用下加热可得到B,其反应类型和条件是_______________________。
(4)A、B各1 mol分别加入足量溴水,完全反应后消耗单质溴的物质的量分别是______mol,______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾是常见的氧化剂,用于制造火药、烟火,工业上用石灰乳氯化法制备氯酸钾的流程如下所示:

已知:氯化过程主要发生反应6Ca(OH)2 + 6Cl2![]() 5CaCl2+Ca(ClO)2+6H2O
5CaCl2+Ca(ClO)2+6H2O
完成下列填空:
(1)工业生产氯气的方法是__________________。
(2)氯化过程需要控制较高温度,其目的有:
①_____________________________; ②减少 Cl2 与 Ca(OH)2 之间的副反应。
(3)向热的滤液中加入稍过量的氯化钾,待溶解完全后进行冷却,有大量氯酸钾晶体析出,写出相关反应的化学方程式:__________________________________________________。
得到的氯酸钾晶体中可能会含有少量氯化钾,进一步提纯的方法是_________________。
(4)为测定所得晶体中氯酸钾的纯度,将 a g 样品与 b g 二氧化锰混合,加热该混合物一段时间后(杂质不参加反应)冷却,称量剩余固体质量,重复加热、冷却、称量操作,记录数据如下表:
加热次数 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量(g) | c | d | e | e |
①进行加热操作时,应将固体置于_________(填仪器名称)中。
②该实验不必进行第五次加热的原因是_______________________________________。
③若某次测定结果的相对误差为-2.98%,写出导致这一结果的一种可能情况。
_______________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 W、X、Y、Z 的原子序数依次递增,a、b、c、d、e、f 是由这些元素组成的化合物,d 是淡黄色粉末,m 为元素 Y 的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法错误的是

A. 简单离子半径:Z<Y
B. 阴离子的还原性:Y>W
C. 简单气态氢化物的热稳定性:Y>X
D. W2Y2 中含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素的单质和化合物在生产生活中有重要的用途。
(1)溴原子的核外电子排布式为[Ar]__________,有_____个未成对电子。
(2)在一定浓度的 HF 溶液中,氟化氢是以缔合形式(HF)2 存在的。使氟化氢分子缔合的作用力是____________。
(3)根据下表数据,分析熔点和硬度变化的原因:________________。
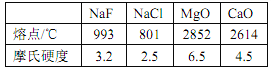
(4)HIO3 的酸性_____(填“强于”或“弱于”)HIO4,原因是_________________。
(5)ClO2中心氯原子的杂化类型为________,ClO3的空间构型为__________。
(6)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各微粒的相对位置。下图是 CaF2 的晶胞,其中原子坐标参数 A 处为(0,0,0);B 处为(![]() ,
, ![]() ,0);C 处为(1,1,1)。则 D 处微粒的坐标参数为__________。
,0);C 处为(1,1,1)。则 D 处微粒的坐标参数为__________。

②晶胞参数:描述晶胞的大小和形状。已知 CaF2 晶体的密度为 c gcm3,则晶胞中 Ca2+与离它最近的 F之间的距离为_________ nm(设 NA 为阿伏加德罗常数的值,用含 c、NA 的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硫的说法正确的是 ( )
A.硫在自然界中仅以化合态存在
B.硫可溶于水
C.硫单质在与Cu、Fe、O 2 的反应中均作氧化剂
D.硫易溶于二硫化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室进行NaCl溶液蒸发时,一般有以下操作过程 ①放置酒精灯 ②固定铁圈位置 ③放上蒸发皿④加热搅拌 ⑤停止加热、余热蒸干 。其正确的操作顺序为( )
A. ②③④⑤B. ①②③④⑤C. ②③①④⑤D. ②①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃能发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,下列有机物可与钠反应来合成环丙烷的是( )
A.CH3CH2CH2Br B.CH3CHBrCH2Br
C.CH2BrCH2CH2Br D.CH3CHBrCH2CH2Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com