
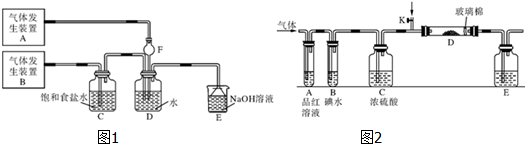
���� ��1����װ��ͼ��֪��Aװ�ò���������Ϊ��������
��2�������������������ʵ����֤�����������ԣ�����������ӱ�����Ϊ�����Ӻ������������Һ����ɫ֤����
������������������ݶ����������Ư���Ի�ԭ�����ʵ���ѡ���Լ���֤��
��3���ٶ����������Ư���ԣ�������ˮ��Ӧ����HClO��HClO����Ư���ԣ����������۷�Ӧ������ɫ���Ȼ�����
��ͨ������������������ȫ��Ӧ������ת�Ƶ�����Ŀ����IԪ�������������еĻ��ϼۣ�ȷ������ݴ���д����4����Ԫ��S��O���-2���������X��X��S��O��������4��3����N��S����N��O��=$\frac{4}{32}$��$\frac{3}{16}$=2��3����XΪS2O32-����S2O32-����Һ��������Ӧ���е���ɫ�������ɣ��õ���ɫ����ΪS���ϲ���Һ�����Ȼ�����Һ���а�ɫ�����������ҳ���������ܽ⣬˵������SO42-������������ԭ��Ӧ����������ԭΪ�����ӣ��ݴ���д��
��� �⣺��1����װ��ͼ��֪��Bװ���������ɺ�ͨ�뱥��ʳ��ˮ�У�˵���������ķ���װ�ã�ͨ��ʳ��ˮ��ȥ�����е��Ȼ������壬����Aװ�ò���������Ϊ����������������������ˮ�����壬ͨ��Fͨ��ˮ��ֹ������
�ʴ�Ϊ��SO2��
��2����Ϊ��֤ͨ��Dװ���е�������Cl2����SO2��������Cl2������ȡ����D����Һ�μ���ʢ���Ȼ�������Һ���Լ����Թ��ڣ��ټ������軯����Һ���Ѫ��ɫ������뱽����Һ����ɫ��֤�����������������ӣ�
�ʴ�Ϊ���ڣ��ۻ�ܣ���Һ��Ѫ��ɫ����ɫ��
����SO2������ȡ����D����Һ�μ���ʢ��Ʒ����Һ���Թ��л����Ը��������Һ���Թ�������Ϊ��ɫ��ȥ�������ָֻ���ɫ����Һ�����ɫ��
�ʴ�Ϊ���ݻ�ޣ���ɫ��ȥΪ��ɫ�����Ⱥ��ֱ�Ϊ��ɫ����Һ�����ɫ��
��3���ٶ����������Ư���ԣ�������ˮ��Ӧ����HClO��HClO����Ư���ԣ���ͨ�����������ͨ��������װ��A�е�Ʒ����Һ����ɫ�����������۷�Ӧ������ɫ���Ȼ�����
�ʴ�Ϊ����ͬ��������ɫ���̣�
��װ��B��װ��5.0mL 1.0mol•L-1�ĵ�ˮ����ͨ������Cl2��ȫ��Ӧ��ת����5.0��10-2mol���ӣ���IԪ�������������еĻ��ϼ�Ϊ$\frac{5.0��1{0}^{-2}mol}{0.005L��1mol/L}$=5������������ΪHIO3����������ԭΪHCl����Ӧ����ʽΪ��5Cl2+I2+6H2O=10HCl+2HIO3��
�ʴ�Ϊ��5Cl2+I2+6H2O�T2HIO3+10HCl��
��4����Ԫ��S��O���-2���������X��X��S��O��������4��3����N��S����N��O��=$\frac{4}{32}$��$\frac{3}{16}$=2��3����XΪS2O32-����S2O32-����Һ��������Ӧ���е���ɫ�������ɣ��õ���ɫ����ΪS���ϲ���Һ�����Ȼ�����Һ���а�ɫ�����������ҳ���������ܽ⣬˵������SO42-������������ԭ��Ӧ����������ԭΪ�����ӣ���Ӧ���ӷ���ʽΪ��H2O+S2O32-+Cl2=S��+SO42-+2Cl-+2H+��
�ʴ�Ϊ��S2O32-+Cl2+H2O�TSO42-+S��+2Cl-+2H+��
���� ���⿼���������Ʊ�����װ�õ������������������ԭ��Ӧ�������������������ʡ�ʵ�鷽����Ƶȣ��Ѷ��еȣ���1���Т�ע����ݵ���ע���ж�IԪ�������������еĻ��ϼۣ��Ƕ�ѧ���ۺ������Ŀ��飮


 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��SiO2��P2O5 | B�� | PCl3��CO2��H2SO4 | C�� | SiC��H2O��NH3 | D�� | HF��CO2��Si |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 L 0.2 mol•L-1 CH3COONa��Һ�к���0.2NA��CH3COO- | |
| B�� | ��״���£�22.4 L CO2����NA��̼��˫�� | |
| C�� | һ���¶��£���2 mol SO2��1 mol O2����װ�д����������з�����Ӧ��ת��4NA������ | |
| D�� | 1 mol�ǻ���-OH���к�9NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢ڢ� | C�� | �ڢۢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��Z��Y��X | |
| B�� | Z��X�γɻ��������������Z��ͬ��Ԫ����X�γɻ���������� | |
| C�� | CaY2��ˮ����������ԭ��Ӧʱ��CaY2ֻ�������� | |
| D�� | CaX2��CaY2��CaZ2��3�ֻ������У��������������Ӹ����Ⱦ�Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2XO2-����Һ�мȿɷ������룬�ֿɷ���ˮ�� | |
| B�� | c��H2XO2-��+c��HXO22-��+c��XO23-��+c��H3XO2��=0.01mol•L-1 | |
| C�� | c��H+��=c��OH-��+c��H3XO2�� | |
| D�� | c��Na+��+c��H+��=c��OH-��+c��H2XO2-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH2=CH-CH=CH2 | B�� | HOCH2-CH2OH | C�� | 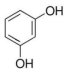 | D�� | HCOOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�ɢϵ�ķ�ɢ��ΪFe2O3 | |
| B�� | ����NaOHʱ�����ķ�Ӧ����Ϊ��Fe2++2Fe3++8OH-=Fe3O4+4H2O | |
| C�� | �ڵ糡�����£�����������ɢϵ��ɫ�����˵���÷�ɢϵ������� | |
| D�� | ���ù��˵ķ�������ɫ������������Na+���뿪 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com