
【题目】在25℃、101 kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式书写正确的是()
A. CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
B. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-1 451.52 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-1 451.52 kJ·mol-1
C. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-725.76 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-725.76 kJ·mol-1
D. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l)ΔH=+1451.52 kJ·mol-1
2CO2(g)+4H2O(l)ΔH=+1451.52 kJ·mol-1
【答案】B
【解析】
1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1451.52 kJ
A、甲醇燃烧是放热反应,焓变值为负值,故A错误;
B、1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1451.52 kJ,热化学方程式为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1451.52 kJ·mol-1,故B正确;
C、1g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1451.52 kJ,反应热数值计算错误,故C错误;
D、甲醇燃烧是放热反应,焓变值为负值,故D错误。
综上所述,本题正确答案为B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在1.0 L真空密闭容器中充入4.0 mol A(g)和4.0 mol B(g),在一定温度下进行反应:A(g)+B(g)![]() C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表:
C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(A)/mol | 4.0 | 2.5 | 1.5 | n2 | n3 |
n(C)/mol | 0 | 1.5 | n1 | 3 | 3 |
回答下列问题:
(1)随着温度的升高,该反应的化学平衡常数减小,则ΔH__________(填“>”“<”或“=”)0,反应从起始到20 min内C的平均反应速率是________。
(2)该温度下,上述反应的化学平衡常数为________。平衡时体系内气体的总压强是反应起始时总压强的________。
(3)下列选项中能说明该反应在一定温度和恒容条件下达到平衡状态的是________。
A.反应速率:vA(正)+vB(正)=vC(逆)
B.A的质量不再改变
C.B的转化率不再改变
D.密度不再改变
(4)若反应C(g)![]() A(g)+B(g) ΔH>0,进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。
A(g)+B(g) ΔH>0,进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。


①由图1可知,T1________(填“>”“<”或“=”)T2。
②由图2可知,当其他条件不变时,增大X的物质的量,C的平衡转化率将________(填“增大”“减小”或“不变”),其原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是人类生存和发展的重要支柱。根据要求回答下列问题。
(1)下列说法中错误的是______。

A.都是清洁能源
B.电能,H2属于二次能源,水力是一级能源
C.煤和石油属于化石燃料,燃烧会产生温室气体
D.氢能热值高,对环境无污染
(2)我国目前使用的主要能源是化石燃料,近年来我国能源总消费量与人均能源消费量如图。
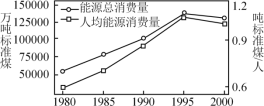
①在我国,煤的消费量巨大,且煤属于不可再生能源,寻找新能源是能源研究的主要课题之一。下列不属于新能源的是______。
A.太阳能 B.氢能 C.地热能 D.海洋能
E.生物质能 F.石油 G.天然气
②已知,1 kg煤大约放热2.9×104 kJ。风能能量巨大,地球上一年可利用的风能相当于5×1014 kw·h的电能。试计算,一年的风能若能全部利用,可相当于节省______吨燃煤。(已知,1 kw·h=3.6×103 kJ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法正确的是( )
A.除去N2中的少量O2:通过灼热的CuO粉末
B.除去CO2中的少量HCl:通入NaOH溶液
C.除去KCl溶液中的少量K2CO3:加入适量的盐酸
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去Na2CO3固体中混有的少量NaHCO3,可采取的方法是( )
A. 加热 B. 通入过量的CO2 C. 加入过量的石灰水 D. 加入稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌﹣锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)![]() Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是( )
A. 电池工作时,锌失去电子
B. 电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e﹣=Mn2O3(s)+2OH﹣(aq)
C. 电池工作时,电子由正极通过外电路流向负极
D. 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器能直接用酒精灯加热的是
①量筒 ②表面皿 ③烧杯 ④试管 ⑤容量瓶 ⑥蒸发皿 ⑦烧瓶
A. ②③④⑥⑦ B. ③⑥ C. ④⑥ D. ④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同情况下测得A(g)+3B(g)![]() 2C(g)+2D(g)的下列反应速率,其中反应速率最大的是
2C(g)+2D(g)的下列反应速率,其中反应速率最大的是
A. υ(D)=0.01 molL-1s-1 B. υ(C)=0.5 molL-1min-1
C. υ(B)=0.6 molL-1min-1 D. υ(A)=0.2molL-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰)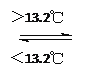 Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列说法正确的是( )
A. DH1>DH2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com