
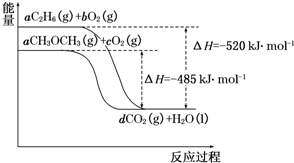
 当今世界,能源的发展日益成为全世界、全人类共同关心的问题.如图是乙烷(C2H6)、二甲醚(CH3OCH3)燃烧过程的能量变化图.请回答下列问题:
当今世界,能源的发展日益成为全世界、全人类共同关心的问题.如图是乙烷(C2H6)、二甲醚(CH3OCH3)燃烧过程的能量变化图.请回答下列问题:分析 (1)依据原子守恒分析可知氢原子守恒,6a=2,a=$\frac{1}{3}$,则根据图象分析可知 $\frac{1}{3}$mol乙烷完全燃烧放热520kJ,所以1mol乙烷完全燃烧放热为520KJ×3=1560kJ;
(2)液态乙烷变成气态要吸热;
(3)根据图象分析可知$\frac{1}{3}$mol二甲醚完全燃烧放热485KJ,结合热化学方程式书写方法标注物质聚集状态和对应反应的焓变写出;
(4)根据图象可知,消耗相同物质的量的乙烷和二甲醚生成的二氧化碳相同,但放出的热量乙烷多,据此分析.
解答 解:(1)依据原子守恒分析可知氢原子守恒,6a=2,a=$\frac{1}{3}$,则根据图象分析可知 $\frac{1}{3}$mol乙烷完全燃烧放热520kJ,所以1mol乙烷完全燃烧放热为520KJ×3=1560kJ,则乙烷的燃烧热△H=-1560kJ.mol-1,
故答案为:-1560kJ.mol-1;
(2)液态乙烷变成气态要吸热,等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物放出的热量少,
故答案为:少; 液态乙烷变成气态要吸热;
(3)根据图象分析可知$\frac{1}{3}$mol二甲醚完全燃烧放热485KJ,则1mol二甲醚完全燃烧放热=485KJ×3=1455KJ,反应的热化学方程式为:CH3OCH3(g)+3O2(g)→2CO2(g)+3H2O(l)△H=-1455 kJ•mol-1,
故答案为:CH3OCH3(g)+3O2(g)→2CO2(g)+3H2O(l)△H=-1455 kJ•mol-1;
(4)根据图象可知,消耗相同物质的量的乙烷和二甲醚生成的二氧化碳相同,但放出的热量乙烷多,所以放出相同的热量时,选择乙烷作为燃料产生的CO2较少,
故答案为:乙烷.
点评 本题考查了热化学方程式书写方法,反应焓变的计算应用,图象分析判断,掌握基础是解题关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 将大理石投入到足量盐酸中:CO32-+2H+═CO2↑+H2O | |
| B. | 铁钉放入硫酸铁溶液中:Fe+Fe3+═2Fe2+ | |
| C. | 向AlCl3溶液中加入过量的氨水反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 将稀硫酸滴入氢氧化钡溶液中:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 84% | B. | 50% | C. | 16% | D. | 39% |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Mg、Al | B. | Mg、Fe | C. | Zn、Fe | D. | Al、Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [H+] | B. | Ka(HF) | C. | $\frac{[{F}^{-}]}{[{H}^{+}]}$ | D. | $\frac{[{H}^{+}]}{[HF]}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 物质 | 试剂或操作名称 |
| ① | 除杂质:NaHCO3溶液(Na2CO3) | |
| ② | 除杂质:MgO(Al2O3) | |
| ③ | 除杂质:FeCl2溶液(FeCl3) | |
| ④ | 鉴别:NaCl、KCl | |
| ⑤ | 鉴别:AlCl3、Al2(SO4)3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定存在的离子为Fe3+、SO42- | |
| B. | 一定不存在的离子为CO32-、I- | |
| C. | 不能确定的离子为K+、SO42- | |
| D. | 确定是否含有K+离子需要经过焰色反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com