
【题目】溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否是大量分子或离子的集合体
B.分散质粒子的大小
C.是否能通过滤纸
D.是否均一、透明、稳定
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在CO2中,Mg燃烧生成MgO和C.下列说法正确的是( )
A.元素C的单质只存在金刚石和石墨两种同素异形体
B.Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg)
C.在该反应条件下,Mg的还原性强于C的还原性
D.该反应中化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水四氯化锡(SnCl4) 实验室可用熔融的锡(熔点为23.9℃)与Cl2反应制备SnCl4,装置如下图所示回答下列问题:

已知SnCl4在湿空气中极易水解生成SnO2·xH2O。
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
(1)a管的作用是________,装置A中发生反应的化学方程式是______________。
(2)装置B、C、F、G中盛放的最佳试剂依次为____________(填序号,试剂可重复使用)。
①饱和Na2CO3溶液 ②NaOH溶液 ③浓H2SO4 ④饱和NaCl溶液 ⑤H2O
(3)点燃酒精灯前需要进行的一步操作是______________。
(4)若撒去装置C,则装置D中可能会发生的主要副反应的化学方程式为___________。
(5)得到的产物中常混有SnCl2,某实验小组用碘氧化法滴定分析产品中SnCl4的含量(Sn2++I2=Sn4++2I-)。准确称取mg产品于锥形瓶中,用少量浓盐酸溶解,再加水稀释,淀粉溶液作指示剂,用0.1mol/L碘标准溶液滴定至终点,达到滴定终点时的现象为________,消耗碘标准溶液20.00mL,计算产品中SnCl4的含量______(用含m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期的5种元素的部分信息如下表所示:
元素代号 | 元素部分信息 |
X | X的阴离子核外电于云均呈球形 |
Y | 原子的能级上有3个未成对电子,其最简单气态氢化物在水中的溶解度在同族元素所形成的最简单气态氢化物中最大 |
Z | 基态原于核外有3个能级填充了电子,能量最高能级的电子数等于前两个能级的电子数之和 |
R | 元素原于的围电子排布式为nsn-1npn-1 |
T | 一种核素的质量数为65,中子数为36 |
根据上述元素信息,回答下列问题:
(1)基态T2+的电子排布式为____________。
(2)Y.Z.R 的电负性由大到小的顺序为____________ (用元素符号表示)。
(3)YX4+的空间构型为____________,离子中Y原子的杂化轨道类型为____________ ,YX4+电子式为________。
(4)YX3的一种等电子体分子是______,YX3 的键角大于X2Z的键角的主要原因是________。
(5)T单质不溶于YX3溶液,也不溶于X2Z溶液,但能溶于它们的混合溶液,其主要原因是形成了稳定的[T(YX3)4]2+,1mol该阳离子中共含有______mol σ键。
(6)Z、T组成的晶胞结构如下图所示。已知Z、T原子的半径分别为apm、bpm,晶胞边长为cpm,则该晶胞中原子的空间利用率为________(用代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A.CS2为V形的极性分子
B.ClO3﹣的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对
D.SiF4和SO3的中心原子均为sp2杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施对增大反应速率明显有效的是( )
A.Na与水反应时增大水的用量
B.Fe与稀硫酸反应制取氢气时,改用浓硫酸
C.在K2SO4与BaCl2两溶液反应时,加入少量氯化钠固体
D.将铝片改为铝粉,做铝与氧气反应的实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。
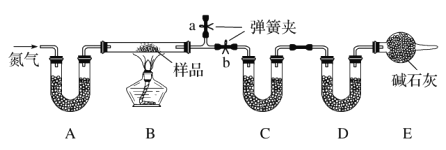
(1)加热前通入氮气的目的是__________,操作方法为_______________。
(2)装置A、C、D中盛放的试剂分别为A_____,C_____,D_____。
(3)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl的含量将_____(填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中NaHCO3的含量将_____;若撤去E装置,则测得Na2CO3·10H2O的含量将_____。
(4)若样品质量为wg,反应后C、D增加的质量分别为m1g、m2g,由此可知混合物中NaHCO3的质量分数为_______(用含w、m1、m2的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:

(1)保存过氧化氢的试剂瓶上最适合贴的标签是_____________(填字母)。
(2)下列反应中,H2O2体现还原性的是______________。
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
D.K2Cr2O7+4H2O2+2H+ =2CrO5+5H2O[CrO5称为过氧化铬,可写成CrO(O2)2]
(3)采矿废液中的氰化物(如KCN)一般用H2O2做无毒化处理,化学方程式为:KCN+H2O2+H2O=KHCO3+NH3↑(KCN中N为﹣3价),生成1mol NH3时转移的电子数为___________。
(4)H2O2被称为绿色氧化剂的理由是_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com