
����Ŀ��������Ԫ��W��X��Y��Z��ԭ��������������m��P��q��r��s������ЩԪ����ɵĶ�Ԫ��������³�ѹ��rΪҺ�壬�����Ϊ��ɫ���塣m��Ħ������Ϊp��2����n��Ԫ��Y�ĵ��ʣ�����ɫֲ�������ò�������ɫ���壬p������ʹʪ��ĺ�ɫʯ����ֽ������q��ʹƷ����Һ��ɫ���������ʵ�ת����ϵ����ͼ��ʾ������˵����ȷ����

A. q��s��Ϊ���������� B. ԭ�Ӱ뾶��W��Y��X
C. Z���⻯���Y���⻯���ȶ� D. Z�ĺ�������һ��ǿ��
���𰸡�B
��������n��Ԫ��Y�ĵ��ʣ�����ɫֲ�������ò�������ɫ���壬����nΪ������YΪ��Ԫ�ء�p������ʹʪ��ĺ�ɫʯ����ֽ������pΪ������q��ʹƷ����Һ��ɫ��qΪ��������n����������p����������ӦӦ�õõ�NO��ˮ����ΪrΪҺ�壬����rΪˮ��sΪNO��m�ķ�������p����������2��������m�ķ�����Ϊ34�����ǵ�m��������Ӧ�õ�������������mһ��ΪH2S�����ϵõ�������Ԫ��W��X��Y��Z�ֱ�ΪH��N��O��S��s��NO���Dz�������������ѡ��A����ԭ�Ӱ뾶Ϊ��W��H����Y��O����X��N����ѡ��B��ȷ���⻯����ȶ��ԣ�H2O(Y���⻯��)��H2S(Z���⻯��)��ѡ��C����Z��S���ĺ����������֣�����������ǿ�ᣬ����������ǿ�ᣬѡ��D����


 �ƸԾ���Ȥζ����ϵ�д�
�ƸԾ���Ȥζ����ϵ�д� ����С����ҵ��ϵ�д�
����С����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ���з���ʱ��������������ԭ��Ӧ�������û���Ӧ���� (����)
A. CH4��2O2![]() CO2��2H2O B. 2KClO3
CO2��2H2O B. 2KClO3![]() 2KCl��3O2��
2KCl��3O2��
C. S��O2![]() SO2 D. 8NH3+3Cl2=6NH4Cl+N2��
SO2 D. 8NH3+3Cl2=6NH4Cl+N2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯��������״���������μ�����̵����������ȡ�ʵ������NaOH�����ʵ��ˮ����(N2H4��H2O)Ϊԭ�Ͽ��Ʊ��⻯�ơ�
������ʾ��ˮ�����л�ԭ�ԣ�������ˮ���ܽ��������NaIO3��һ����������
�ش��������⣺
��1��ˮ���µ��Ʊ�
�йط�Ӧԭ��Ϊ��NaClO + 2NH3 = N2H4��H2O + NaCl��
������ͼװ����ȡˮ���£�������˳��Ϊ_________(������������Сд��ĸ��ʾ)��
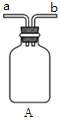
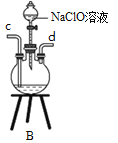
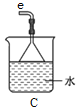
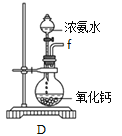
��װ��A��������_______��
�ۿ�ʼʵ��ʱ�������������еμ�Ũ��ˮ��һ��ʱ�������B��������ƿ�еμ�NaClO��Һ���μ�NaClO��Һʱ���ܹ��������___________
��2���⻯�Ƶ��Ʊ�
i. ��������ƿ�м���8.4gNaOH��30mLˮ�����衢��ȴ������25.4g�ⵥ�ʣ���������������������60~70������Ӧ��֣�
ii�����������Թ�����N2H4��H2O(ˮ����)����ԭNaIO��NaIO3����NaI��Һ��Ʒ��ͬʱ�ͷ�һ�ֿ����е����壻
iii����������ӦҺ�м���1.0g����̿����а�Сʱ��Ȼ����Һ�����̿����;
iv��������iii���������Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����ò�Ʒ24.0g��
�ܲ���i���˲��õļ��ȷ�����_________�� �ò��跴Ӧ��ȫ��������_________��
����ii��IO3�����뷴Ӧ�����ӷ���ʽΪ________________________________��
�ݲ���iii������Һ�����̿�������ķ�����_____________________________��
�ޱ���ʵ�����Ϊ__________��ʵ�鷢�֣�ˮ����ʵ������������ֵƫ�ߣ����ܵ�ԭ����________________________________________________��
�� ijͬѧ�����ƷNaI���Ƿ����NaIO3���ʡ�ȡ����������Ʒ���Թ��У���ˮ�ܽ⣬�μ���������Һ���ٵμ�����ϡ���ᣬƬ�̺���Һ�������ó�NaI�к���NaIO3���ʡ������۸�ʵ����۵ĺ�����___________________________������Ϊ����д�����ӷ���ʽ������Ϊ������˵�����ɣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�鹫˾������Li-SO2Cl2���õ�أ���ʾ��ͼ����ͼ��ʾ����֪����ܷ�ӦΪ��2Li+ SO2Cl2= 2LiCl+SO2�������������д������
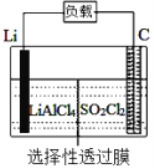
A. ��ع���ʱ����������Li������������Ӧ
B. ��ع���ʱ��������﮵缫�����ߡ����ء�̼��
C. ��ع���ʱ�����·����0.2 mol���ӣ���״��������4.48 L����
D. ��ع��������У�ʯī�缫��ӦʽΪSO2Cl2+2e-=2Cl-+SO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��A��ͨ�볱ʪ��Cl2���ر�B��ʱ��C������ĺ�ɫ������������������B����C����ɫ��������ɫ����Dƿ��װ�IJ��������� ��

A. ŨH2SO4 B. NaOH��Һ C. ����ʯ��ˮ D. ����NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(POCl3)�������л��ϳɵ��Ȼ����ʹ�����
��֪����KSCN+AgNO3=AgSCN��+KNO3��
��Ksp(AgCl) > Ksp(AgSCN)��
�����������������
��PCl3��POCl3�������Ϣ���±���
���� | �۵�/�� | �е�/�� | ��Է������� | ���� |
PCl3 | -111.8 | 74.2 | 137.5 | ��Ϊ��ɫҺ�壬��ˮ������ˮ�⣬���ɺ�������Ȼ��⣬�����ܡ� |
POCl3 | 2.0 | 105.3 | 153.5 |
ʵ������ȡPOCl3���ⶨ��Ʒ���ȵ�ʵ��������£�
��.�Ʊ�POCl3������������Һ̬PCl3�ķ�����ʵ��װ�ã����ȼ��г�װ��ʡ�ԣ����£�
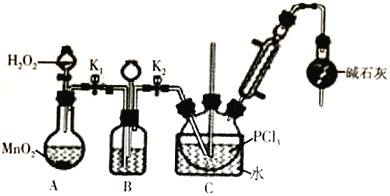
��1��װ��C��ʢװPCl3����������Ϊ_______________________����������PCl3�Ļ�ѧ����ʽΪ_______________________________��
��2��������װ��ɺ��װ��B�����Եķ�����_______________________________��
��3��װ��B��������________________________________���ش����㣩��
��4��װ��C�ķ�Ӧ�¶ȿ�����60-65��֮�䣬ԭ����____________________________________��
��.�ⶨ��Ʒ��POCl3���ȵ�ʵ�鲽�裺
��ʵ����������Ӧ����Һ����ȴ�����£�ȷ��ȡ1.3300 g��POCl3�ֲ�Ʒ�����ʲ�����Ԫ�أ�������ʢ��50.00mL����ˮ���ձ���ҡ������ȫˮ�⣬��ˮ��Һ���100.00mL��Һ��
��ȡ10.00mL��Һ����ƿ�У�����30.00mL0.1200mol��L-1AgNO3����Һ��
�ۼ�������������������ҡ�������ã�
�ܼ���ָʾ������0.1000 mol��L-1KSCN��Һ�ζ�������AgNO3��Һ�������յ�ʱ����ȥ12.00mLKSCN��Һ��
��5���ζ�������ѡ���ָʾ��Ϊ___________��Һ��
��6������۵�Ŀ����___________________________________________________��
��7����ò�Ʒ��POCl3�Ĵ���Ϊ__________%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ����(����)
A. 1 mol����ڱ�״���µ����ԼΪ11.2 L
B. 20 ����10 MPa״̬�£�32 g O2��O3�Ļ����������ԭ����Ϊ2.5NA
C. ��״���£�11.2 L H2CO3���е�ԭ����Ϊ3NA
D. ���³�ѹ�£�44 g CO2���е�ԭ����Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(Raney-Ni)��һ�ֶ�ṹ�������Ͻ𣬶���������ǿ�����ԣ���ϩ����Ȳ���⻯��Ӧ�ĸ�Ч������һ����ͭ����(��Ҫ��Cu��Fe��Co��Ni)��������������������:
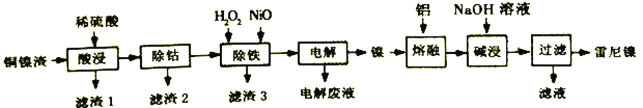
�±��г����йؽ������������������������pH:
�������� | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
��ʼ������pH | 1.5 | 6.5 | 7.7 |
������ȫ��pH | 3.3 | 9.9 | 9.2 |
��1���������ʱ����ͨ����������Ͻ��裬�ɽ�������1�������ܽ⣬���ӷ���ʽΪ___________��
��2����������ʱ���ȼ�������H2O2����Fe2+�����������ĵ�n(H2O2):n(Fe2+)=____���ټ���NiO�Ե�����Һ��pH��Ӧ����pH�ķ�ΧΪ__________________��
��3���������(�Զ��Բ������缫)��Ϊ�˻�õ��������������п�ѭ�����õ�������_______��
��4�����������Ϊ���γɶ�ṹ������������Ӧ�����ӷ���ʽΪ_________________��ʹ�����������������⻯��Ӧʱ����������Ҳ��ʵ���⻯��Ŀ�ģ�ԭ����____________________��
��5������Һ����Ҫ�ɷ������CO2��Ӧ�����ӷ���ʽΪ__________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com