
ΓΨΧβΡΩΓΩΖ÷±πΑ¥œ¬ΆΦΦΉΓΔ““Υυ ΨΉΑ÷ΟΫχ–– Β―ιΘ§ΆΦ÷–ΝΫΗω…’±≠άοΒΡ»ή“ΚΈΣΆ§≈®Ε»ΒΡœΓΝρΥαΘ§““÷–GΈΣΒγΝςΦΤΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ

(1)“‘œ¬–π ω÷–Θ§’ΐ»ΖΒΡ «__________ΓΘ
AΘ°ΦΉ÷––ΩΤ§ «ΗΚΦΪΘ§““÷–Ά≠Τ§ «’ΐΦΪ
BΘ°ΝΫ…’±≠÷–Ά≠Τ§±μΟφΨυ”–Τχ≈ί≤ζ…ζ
CΘ°ΝΫ…’±≠÷–»ή“ΚpHΨυ‘ω¥σ
DΘ°≤ζ…ζΤχ≈ίΒΡΥΌΕ»ΦΉ÷–±»““÷–¬ΐ
EΘ°““ΒΡΆβΒγ¬Ζ÷–ΒγΝςΖΫœρZnΓζCu
F. ““»ή“Κ÷–SO42-œρΆ≠Τ§ΖΫœρ“ΤΕ·
(2)±δΜ·Ιΐ≥Χ÷–ΡήΝΩΉΣΜ·ΒΡ÷ς“Σ–Έ Ϋ «ΘΚΦΉΈΣ__________ΘΜ““ΈΣ__________ΓΘ
(3)‘Ύ““ Β―ι÷–Θ§Ρ≥Ά§―ßΖΔœ÷≤ΜΫω‘ΎΆ≠Τ§…œ”–Τχ≈ί≤ζ…ζΘ§Εχ«“‘Ύ–ΩΤ§…œ“≤≤ζ…ζΝΥΤχΧεΘ§Ζ÷Έω‘≠“ρΩ…Ρή «______________________________________________ΓΘ
(4)‘Ύ““ Β―ι÷–Θ§»γΙϊΑ―ΝρΥαΜΜ≥…ΝρΥαΆ≠»ή“ΚΘ§«κ–¥≥ωΆ≠ΒγΦΪΒΡΒγΦΪΖ¥”ΠΖΫ≥Χ ΫΦΑΉήΖ¥”ΠάκΉ”ΖΫ≥Χ ΫΘΚΆ≠ΒγΦΪΘΚ __________________Θ§ΉήΖ¥”ΠΘΚ ________________________________ΓΘ
Β±Βγ¬Ζ÷–ΉΣ“Τ0.25 molΒγΉ” ±Θ§œϊΚΡΗΚΦΪ≤ΡΝœΒΡ÷ ΝΩΈΣ________________ (ZnΒΡœύΕ‘‘≠Ή”÷ ΝΩ65)
ΓΨ¥πΑΗΓΩ CΓΔD Μ·―ßΡήΉΣΜ·ΈΣ»»Ρή Μ·―ßΡήΉΣΜ·ΈΣΒγΡή –ΩΤ§≤Μ¥ΩΘ§‘Ύ–ΩΤ§…œΨΆ–Έ≥…‘≠Βγ≥Ί Cu2+ + 2e- = Cu Zn + Cu2+ =Zn2+ +Cu 8.125ΩΥ
ΓΨΫβΈωΓΩΘ®1Θ©AœνΘ§ΦΉ÷–ΟΜ”––Έ≥…±’ΚœΜΊ¬ΖΘ§≤ΜΡήΙΙ≥…‘≠Βγ≥ΊΘ§Ι A¥μΈσΘΜBœνΘ§Ά≠≤ΜΡή”κœΓΝρΥαΖ¥”ΠΘ§Υυ“‘ΦΉ…’±≠÷–Ά≠Τ§±μΟφΟΜ”–Τχ≈ί≤ζ…ζΘ§Ι B¥μΈσΘΜCœνΘ§ΝΫ…’±≠÷–«βάκΉ”ΕΦ≤ΈΦ”Ζ¥”ΠΘ§≈®Ε»ΕΦΦθ–ΓΘ§»ή“ΚΒΡpHΨυ‘ω¥σΘ§Ι C’ΐ»ΖΘΜDœνΘ§““÷–ΙΙ≥…‘≠Βγ≥ΊΘ§Φ”ΩλΝΥΜ·―ßΖ¥”ΠΥΌ¬ Θ§Υυ“‘≤ζ…ζΤχ≈ίΒΡΥΌ¬ ΦΉ÷–±»““÷–¬ΐΘ§Ι D’ΐ»ΖΘΜEœνΘ§ΒγΉ””…ΗΚΦΪΨ≠ΆβΒγ¬ΖΝςœρ’ΐΦΪΘ§ΒγΝςœύΖ¥Θ§““÷–ZnΈΣΗΚΦΪΘ§CuΈΣ’ΐΦΪΘ§Υυ“‘ΒγΝςΖΫœρCuΓζZnΘ§Ι E¥μΈσΘΜFœνΘ§““÷–ΙΙ≥…‘≠Βγ≥ΊΘ§ZnΈΣΗΚΦΪΘ§ ß»ΞΒγΉ”Θ§ΒγΉ”―ΊΆβΒγ¬ΖΝςœρ’ΐΦΪCuΘ§»ή“Κ÷–ΒΡH+œνΆ≠Τ§ΖΫœρ“ΤΕ·Θ§SO42-œρ–ΩΤ§ΖΫœρ“ΤΕ·Θ§Ι F¥μΈσΓΘΉέ…œΘ§―ΓCΓΔDΓΘ
Θ®2Θ©ΦΉΟΜ”–ΙΙ≥…‘≠Βγ≥ΊΘ§ΗΟΖ¥”ΠΖ≈»»Θ§Ι Μ·―ßΡήΉΣΜ·ΈΣ»»ΡήΘΜ““ΙΙ≥…‘≠Βγ≥ΊΘ§Ι Μ·―ßΡήΉΣΜ·ΈΣΒγΡήΓΘ
Θ®3Θ©‘Ύ–ΩΤ§…œ“≤Ω¥ΒΫ”–Τχ≈ί≤ζ…ζΘ§ΥΒΟς–ΩΤ§…œ“≤ΙΙ≥…ΝΥ‘≠Βγ≥ΊΘ§Υυ“‘ΩœΕ® «–ΩΤ§≤Μ¥Ω‘λ≥…ΒΡΓΘ
Θ®4Θ©‘Ύ““ Β―ι÷–Θ§»γΙϊΑ―ΝρΥαΜΜ≥…ΝρΥαΆ≠»ή“ΚΘ§‘ρΖ¥”Π‘≠άμΈΣΘΚZn +Cu2+=Zn2++CuΘ§Φ¥ΈΣΗΟ‘≠Βγ≥ΊΒΡΉήΖ¥”ΠΘΜ»ή“Κ÷–ΒΡΆ≠άκΉ”‘ΎΆ≠ΒγΦΪ…œΜώΒΟΒγΉ”ΖΔ…ζΜΙ‘≠Ζ¥”ΠΘ§ΒγΦΪΖ¥”Π «ΈΣΘΚCu2++2e-=CuΓΘ
Θ®5Θ©ΗΚΦΪΖ¥”ΠΈΣΘΚZn-2e-=Zn2+Θ§Β±Βγ¬Ζ÷–ΉΣ“Τ0.25 molΒγΉ” ±Θ§œϊΚΡ–Ω0.125molΘ§÷ ΝΩΈΣΘΚ0.125molΓΝ65gmol-1=8.125gΓΘ


 ΡήΩΦ ‘ΤΎΡ©≥ε¥ΧΨμœΒΝ–¥πΑΗ
ΡήΩΦ ‘ΤΎΡ©≥ε¥ΧΨμœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷Σ”–“‘œ¬Έο÷ œύΜΞΉΣΜ·
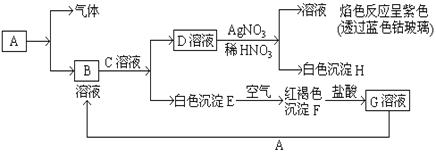
Θ®1Θ©AΉΣΜ·ΈΣBΦΑΤχΧε’β≤ΫΖ¥”Π÷–”ΠΦ”»κΒΡ ‘ΦΝ «_______Θ®ΧνΟϊ≥ΤΘ©ΓΘ
Θ®2Θ©–¥≥ωBΒΡΜ·―ß Ϋ_______ DΒΡΜ·―ß Ϋ_______
Θ®3Θ©–¥≥ω”…EΉΣ±δ≥…FΒΡΜ·―ßΖΫ≥Χ Ϋ_____________________________
Θ®4Θ©–¥≥ωœρG»ή“Κ÷–Φ”»κAΒΡ”–ΙΊάκΉ”Ζ¥”ΠΖΫ≥Χ Ϋ «______________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥≈®H2SO4 ΟήΕ»1.84 g/mLΘ§Έο÷ ΒΡΝΩ≈®Ε»ΈΣ18.4 mol/LΘ§÷ ΝΩΖ÷ ΐΈΣ98%Θ§»Γ10 mL≈®H2SO4ΚΆa mLΥ°ΜλΚœΒΟΈο÷ ΒΡΝΩ≈®Ε»ΈΣc mol/LΘ§÷ ΝΩΖ÷ ΐΈΣb%ΓΘœ¬Ν–ΉιΚœ’ΐ»ΖΒΡ «
(1)»τc=9.2Θ§‘ρa>10 b>49
(2)»τc=9.2Θ§‘ρa>10 bΘΦ49
(3)»τb=49Θ§‘ρa=18.4 cΘΦ9.2
(4)»τb=49Θ§‘ρa=18.4 c>9.2
AΘ°(1)(3) BΘ°(1)(4) CΘ°(2)(3) DΘ°(2)(4)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Έο÷ τ”Ύ¥ΩΨΜΈοΒΡ «Θ® Θ©
A. Ω’ΤχB. ΚΘΥ°C. ΝρΥαΆ≠D. œΓœθΥα
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΓΕΧλΙΛΩΣΈοΓΖ‘ΊΘΚΜΤΖ·Υυ≥ω”÷Τφ…θΘ§ΡΥΦ¥ΝΕ‘μΖ·¬·≤ύΆΝ«ΫΘ§ΙΈ»Γœ¬ά¥ΓΘ»ΨΦ“”Ο÷°Θ§Ϋπ…ΪΒ≠’ΏΆΩ÷ΥΘ§ΝΔ≥…Ήœ≥ύ“≤ΓΘΘ®‘μΖ·FeSO4ΓΛ7H2OΘΜΜΤΖ·Fe2(SO4)3ΓΛ10H2OΘΜ≥ύΖ·Fe2O3Θ©œ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
A. ‘μΖ·Ω…”Ο”ΎΦν–‘Μ®ΡΨΆΝ»ά≤ΙΧζ
B. ‘μΖ·±δΈΣΜΤΖ· « ή»»Ά―Υ°Ιΐ≥Χ
C. ΜΤΖ· ή»»Ζ÷ΫβΩ…“‘ΜώΒΟ≥ύΖ·
D. Ζ· «Κ§ΫαΨßΥ°ΒΡΝρΥα―ΈΩσ ·
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ―«œθΥαΗΤ «“Μ÷÷Ήη–βΦΝΘ§Ω…”Ο”Ύ»ΨΝœΙΛ“ΒΘ§Ρ≥–Υ»Λ–ΓΉιΡβ÷Τ±ΗCa(NO2)2≤ΔΕ‘Τδ–‘÷ Ϋχ––ΧΫΨΩΓΘ
ΓΨ±≥ΨΑΥΊ≤ΡΓΩ
IΘ°Ca(NO2)2Ρή±ΜΥα–‘KMnO4»ή“Κ―θΜ·≥…NO3Θ§MnO4-±ΜΜΙ‘≠ΈΣMn2+ΓΘ
IIΘ°‘ΎΥα–‘ΧθΦΰœ¬Θ§Ca(NO2)2ΡήΫΪIΘ≠―θΜ·ΈΣI2Θ§S2O32ΡήΫΪI2ΜΙ‘≠ΈΣIΓΘ
IIIΘ°HNO2 «ΨΏ”–―θΜ·–‘ΒΡ“Μ‘Σ»θΥα«“AgNO2 «“Μ÷÷Ρ―»ή”ΎΥ°ΒΡΑΉ…ΪΜ·ΚœΈοΓΘ
(1)–Υ»Λ–ΓΉιΆ§―ßΡβάϊ”ΟΆ≠Τ§ΚΆΡ≥≈®Ε»ΒΡœθΥα÷Τ±ΗΈο÷ ΒΡΝΩ÷°±»ΈΣ1:1ΒΡNOΚΆNO2ΒΡΜλΚœΤχΧεΘ§«κ–¥≥ω¥ΥΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ___________________________;
(2)–Υ»Λ–ΓΉιΆ§―ßΡβάϊ”ΟΘ®1Θ©≤ζ…ζΒΡΒΣ―θΜ·Έο÷Τ±ΗCa(NO2)2Θ§ΉΑ÷Ο»γΆΦΓΘ

ΔΌΉΑ÷ΟA÷–ΒΦΙήΡ©ΕΥΫ”“Μ≤ΘΝß«ρΒΡΉς”Ο «___________________________;
ΔΎΉΑ÷ΟBΒΡΉς”Ο «________________ΘΜ
Δέ»τœ÷”–m mol NO2ΚΆn mol NOΉι≥…ΒΡΜλΚœΤχΧεΫχ»κΉΑ÷ΟCΫχ––Έ≤Τχ¥ΠάμΘ§”ϊ”Οa mol/L NaOH»ή“ΚΈϋ ’Θ§÷Ν…Ό–η“Σa mol/L NaOH»ή“ΚΒΡΧεΜΐΈΣ____________…ΐ;
(3)–Υ»Λ–ΓΉιΆ§―ßΡβ≤βΕ®Ca(NO2)2ΒΡ¥ΩΕ»(‘”÷ ≤Μ≤ΈΦ”Ζ¥”Π)Θ§Ω…Ι©―Γ‘ώΒΡ ‘ΦΝΘΚ
AΘ°KIΘ®Υα–‘Θ©»ή“Κ BΘ°ΒμΖέ»ή“Κ
CΘ°Na2S2O3»ή“Κ DΘ°Υα–‘KMnO4»ή“Κ
ΔΌάϊ”ΟCa(NO2)2ΒΡΜΙ‘≠–‘ά¥≤βΕ®Τδ¥ΩΕ»Θ§Ω…―Γ‘ώΒΡ ‘ΦΝ «____________ (ΧνΉ÷ΡΗ);
ΔΎάϊ”ΟCa(NO2)2ΒΡ―θΜ·–‘ά¥≤βΕ®Τδ¥ΩΕ»Θ§Ω…―Γ‘ώΒΡ ‘ΦΝ «____________ (ΧνΉ÷ΡΗ);
(4)–Υ»Λ–ΓΉιΆ§―ß»œΈΣ÷Τ±ΗΒΡCa(NO2)2ΜαΜλ”–Ca(NO3)2Θ§Ρή”Οά¥Φχ±πΕΰ’ΏΒΡ ‘ΦΝΘ®_____Θ©
AΘ°≤β»ή“ΚΒΡPH÷Β BΘ°Φ”ΝρΥαΧζΘ®Υα–‘Θ©»ή“Κ
CΘ°Φ”œθΥα“χ»ή“Κ DΘ°Φ”ΒμΖέΒβΜ·ΦΊΘ®Υα–‘Θ©»ή“Κ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”–ΜζΈοMΓΔNΓΔQΒΡΉΣΜ·ΙΊœΒ»γœ¬ΆΦΥυ ΨΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©

A. MΒΡΟϊ≥ΤΈΣ“λΕΓΆι
B. NΒΡΆ§Ζ÷“λΙΙΧε”–7÷÷(≤ΜΩΦ¬«ΝΔΧε“λΙΙΘ§≤ΜΑϋά®±Ψ…μ)
C. QΒΡΥυ”–ΧΦ‘≠Ή”“ΜΕ®Ι≤Οφ
D. QΡή ΙδεΒΡΥΡ¬»Μ·ΧΦ»ή“ΚΚΆΥα–‘KMnO4»ή“ΚΆ …ΪΘ§Ά …Ϊ‘≠άμœύΆ§
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–άκΉ”ΖΫ≥Χ Ϋ ι–¥’ΐ»ΖΒΡ «
A. Na”κΥ°Ζ¥”ΠΘΚ2Na+2H2O=2Na++2OHΘ≠+H2Γϋ
B. FeCl3Η· ¥Βγ¬ΖΑεΘΚFe3++Cu=Fe2++Cu2+
C. œρMg(OH)2÷–Φ”»κ―ΈΥαΘΚOHΘ≠+H+=H2O
D. Cl2”κΥ°Ζ¥”ΠΘΚCl2+H2O=2H++ClΘ≠+ClOΘ≠
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΙΊ”ΎΨßΧεΥΒΖ®ΒΡ’ΐ»ΖΉιΚœ «ΓΓΓΓΓΓ

ΔΌΖ÷Ή”ΨßΧε÷–ΕΦ¥φ‘ΎΙ≤ΦέΦϋΓΓ
ΔΎ‘ΎΨßΧε÷–÷Μ“Σ”–―τάκΉ”ΨΆ“ΜΕ®”–“θάκΉ”ΓΓ
ΔέΫπΗ’ ·ΓΔSiCΓΔNaFΓΔNaClΓΔH2OΓΔH2SΨßΧεΒΡ»έΒψ“ά¥ΈΫΒΒΆΓΓ
ΔήάκΉ”ΨßΧε÷–÷Μ”–άκΉ”ΦϋΟΜ”–Ι≤ΦέΦϋΘ§Ζ÷Ή”ΨßΧε÷–ΩœΕ®ΟΜ”–άκΉ”ΦϋΓΓ
ΔίCaTiO3ΨßΧε÷–(ΨßΑϊΫαΙΙ»γ…œΆΦΥυ Ψ)ΟΩΗωTi4ΘΪΚΆ12ΗωO2Θ≠ΫτΝΎΓΓ
ΔόSiO2ΨßΧε÷–ΟΩΗωΙη‘≠Ή””κΝΫΗω―θ‘≠Ή”“‘Ι≤ΦέΦϋœύΫαΚœΓΓ
ΔΏΨßΧε÷–Ζ÷Ή”ΦδΉς”ΟΝΠ‘Ϋ¥σΘ§Ζ÷Ή”‘ΫΈ»Ε®ΓΓ
Δύ¬»Μ·ΡΤ»έΜ· ±άκΉ”Φϋ±ΜΤΤΜΒ
AΘ°ΔΌΔΎΔέΔόΓΓΓΓΓΓΓΓ ΓΓΓΓBΘ°ΔΌΔΎΔή
CΘ°ΔέΔίΔΏ DΘ°ΔέΔίΔύ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com