
【题目】(1)根据反应![]() ,回答下列问题:
,回答下列问题:
①用双线桥法标出该反应中电子转移的方向和数目:______。
②该反应中______元素被还原,______元素被氧化。
③在该反应中,若有![]() 电子发生转移,在标准状况下,可生成
电子发生转移,在标准状况下,可生成![]() 的体积为_____L。
的体积为_____L。
(2)配平化学方程式且回答下列问题:
①______ ![]() ______
______![]() ___
___![]() _____
_____![]() ___ Cl2 ___H2O
___ Cl2 ___H2O
②若生成![]() ,则被氧化的HCl是_________mol,
,则被氧化的HCl是_________mol,
(3)已知反应:2H2S+H2SO3=2H2O +3S,若氧化产物比还原产物多![]() ,则同时会生成水的质量为 ______ g。
,则同时会生成水的质量为 ______ g。
【答案】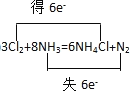 Cl N 1.12 2 16 2 2 5 8 2 1.8
Cl N 1.12 2 16 2 2 5 8 2 1.8
【解析】
(1)①在该反应中,Cl元素的化合价由0降低为-1价,部分N元素的化合价由-3价升高为0价,当3mol氯气和8mol氨气发生反应时,转移电子物质的量为6mol,据此可用双线桥标出电子转移的方向和数目;
②该反应中Cl元素的化合价降低,得电子,被还原,N元素的化合价升高,失电子,被氧化;
③N元素化合价由3价升高为0,当3mol氯气和8mol氨气发生反应生成1mol氮气时,转移电子物质的量为6mol,当反应过程中有0.3mol电子转移时,有0.05mol氮气生成;
(2)①反应中高锰酸钾中+7价锰降为氯化锰中+2价,降价数为5,得到5mol电子,氯化氢中-1价氯化合价升高为氯气中0价,升高为1,生成1mol氯气失去2mol电子,依据氧化还原反应中得失电子守恒、原子个数守恒配平方程式;
②依据方程式2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,生成氯气的氯化氢是被氧化的,生成1mol氯气转移2mol电子,被氧化的氯化氢物质的量为2mol;
(3)反应中H2S中S氧化化合价升高,SO2中S元素化合价降低,氧化产物为2mol,还原产物为1mol,此时氧化产物比还原产物多32g,据此进计算。
(1)①在该反应中,Cl元素的化合价由0降低为-1价,部分N元素的化合价由-3价升高为0价,当3mol氯气和8mol氨气发生反应时,转移电子物质的量为6mol,则用双线桥标出电子转移的方向和数目可为 ;
;
故答案为: ;
;
②该反应中Cl元素的化合价降低,得电子,被还原,N元素的化合价升高,失电子,被氧化;
故答案为:Cl;N;
③N元素化合价由3价升高为0,当3mol氯气和8mol氨气发生反应生成1mol氮气时,转移电子物质的量为6mol,当反应过程中有0.3mol电子转移时,有0.05mol氮气生成,标准状况下的体积为![]() ;
;
故答案为:1.12;
(2)①该反应中,高锰酸钾中+7价锰降为氯化锰中+2价,降价数为5,得到5mol电子,氯化氢中1价氯化合价升高为氯气中0价,升高为1,生成1mol氯气失去2mol电子,依据氧化还原反应中得失电子守恒,高锰酸钾系数为2,氯气系数为5,依据原子个数守恒,氯化锰系数为2,氯化钾系数为2,依据氯原子个数守恒氯化氢系数为16,水分子系数为8,所以方程式:2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O;
故答案为:2;16;2;2;5;8;
②71gCl2物质的量为![]() ,依据方程式2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,生成氯气的氯化氢是被氧化的,则生成1mol氯气转移2mol电子,被氧化的氯化氢物质的量为2mol;
,依据方程式2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,生成氯气的氯化氢是被氧化的,则生成1mol氯气转移2mol电子,被氧化的氯化氢物质的量为2mol;
故答案为:2;
(3)反应2H2S+SO2═3S↓+2H2O中,H2S中S元素化合价由-2升高为0,被氧化,得氧化产物,SO2中S元素化合价由+4降低为0,被还原,得还原产物,S单质既是氧化产物,也是还原产物,生成3molS时,氧化产物为2mol,还原产物为1mol,此时氧化产物比还原产物多32g,同时会生成水2mol,若氧化产物比还原产物多1.6g,同时会生成水0.1mol,质量是1.8g;
故答案为:1.8。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
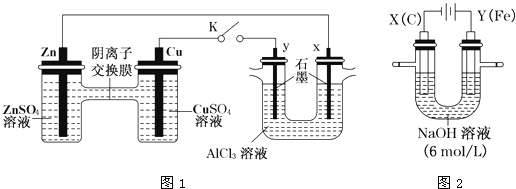
【题目】某课外小组分别用下图所示装置对原电池和电解原理进行实验探究。
请回答:
Ⅰ.用图1所示装置进行第一组实验(K闭合)。
(1)Zn极为________极;实验过程中,SO42-____________(填“从左向右”、“从右向左”或“不”)移动。
(2)反应初期,y极的电极反应现象为________________;检验y极反应产物的方法是________________。
(3)Cu极的电极反应式为____________。
(4)Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。电解过程中,X极的电极反应式为__________。
(5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O和4OH--4e-=2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少________g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2该电池正极发生反应的电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL浓度均为0.1 mol/LHX 和CH3COOH的混合液中滴加0.1 mol·L-1的NH3·H2O,测得混合液的电阻率与加入NH3·H2O 的体积(V)的关系如图所示。已知:物质的电阻率越大,导电能力越弱,CH3COOH的![]() ,NH3·H2O的
,NH3·H2O的![]() 。下列说法错误的是
。下列说法错误的是

A.常温时,0.1 mol/LHX的pH比0.1 mol/LCH3COOH 的pH小
B.a→c过程中水的电离程度先增大后减小
C.c点溶液中:c(CH3COO-)+c(X-)>c(NH4+)
D.d 点有4c(NH4+)+4c(NH3·H2O)=0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴酸镉[Cd(BrO3)2]常用做分析试剂、生产荧光粉等。以镉铁矿(成分为 CdO2、Fe2O3、FeO 及少量的Al2O3 和SiO2)为原料制备[Cd(BrO3)2]的工艺流程如下:

已知 Cd(SO4)2 溶于水,回答下列问题:
(1)为提高镉的浸取率,酸浸时可采取的措施有 ____________(任写两种即可)。
(2)还原镉时,产生能使澄清石灰水变浑浊的气体,发生的离子反应方程式为 ________。
(3)加入H2O2 溶液的目的是_________。
(4)滤渣2 的主要成分为_______________ (填化学式);为检验滤液中是否含有 Fe3+离子,可选用的化学试剂是__________________ 。
(5)实际工业生产中,有时还采用阳离子交换树脂法来测定沉镉后溶液中 Cd2+的含量, 其原理是:Cd2++ 2NaR=2Na++ CdR2 ,其中 NaR 为阳离子交换树脂。常温下,将沉镉后的溶液(此时溶液 pH=6)经过阳离子交换树脂后,测得溶液中的 Na+比交换前增加了 0.0552 g/L,则该条件下Cd(OH)2 的 Ksp 值 为___________。
(6)已知镉铁矿中 CdO2 的含量为 72 %,整个流程中镉元素的损耗率为 10 %,则 2t 该镉铁矿可制得 Cd(BrO3)2(摩尔质量为 368 g/mol)质量为 ________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光伏发电是当今世界利用太阳能最主要的方式之一。某实验小组提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。如图是该方法的装置示意图(其中电解池中隔膜仅阻止气体通过,阴阳两极均为惰性电极,尿素[CO(NH2)2]中氮元素显-3 价)。
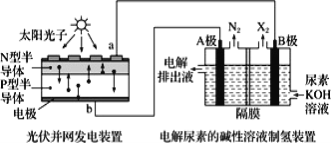
下列叙述正确的是
A.N 型半导体为正极
B.B 极产生的 X2 气体为 O2
C.A 极的电极反应式为 CO(NH2)2-6e-+8OH-=CO32-+N2 ↑+6H2O
D.外电路每转移 0.2 mol 电子,就有 0.2 mol OH-通过隔膜由 A 极区进入 B 极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与3.36LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·L-1NaOH溶液至 Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mLB.120mLC.240mLD.360mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为实验室常用装置。回答下列问题:
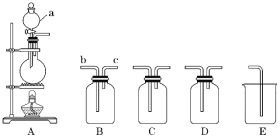
(1)仪器a的名称为____。
(2)利用二氧化锰与浓盐酸反应制备并收集Cl2时,依次连接装置 A、B、C、D、E并加入适当的 试剂。装置B中饱和食盐水的作用是____;利用装置C干燥Cl2,选用的试剂是____;装置E的作用是____。
(3)利用铜和稀硝酸反应制备并收集NO时,连接装置A、B、E并加入适 当的试剂。A中反应的离子方程式为____,A中导气管应连接B的___(填“b”或“c”)端。实验过程中观察到A中出现了红棕色,但收集的气体为无色,原因是____(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求答题
(一)现有下列七种物质:①铝 ②蔗糖 ③CO2 ④H2SO4 ⑤Ba(OH)2 ⑥红褐色的氢氧化铁胶体 ⑦HCl ⑧冰水混合物 ⑨碳酸钙 ⑩CuSO4·5H2O。
(1)上述物质中属于电解质的有__________(填序号)。
(2)向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是________________________。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为______________________________。
(二)(1)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______,R的相对原子质量为__________。
(2)在标准状况下,w L氮气含有x个N2分子,则阿伏加德罗常数为____________(用w,x表示)。
(3)过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的BaCl2溶液;②加入稍过量的NaOH溶液;③加入稍过量的Na2CO3溶液;④滴入稀盐酸至无气泡产生;⑤过滤。正确的操作顺序是________(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com