
 Ⅰ.工业上主要以甲醇为原料进行制备甲醛(HCHO).
Ⅰ.工业上主要以甲醇为原料进行制备甲醛(HCHO).| 物质 | 反应热/kJ•mol-1 |
| CH3OH (g) | -726.5 |
| HCHO (g) | -570.8 |
分析 I.(1)由物质燃烧热数据可知:①CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1,
②HCHO(g)+O2(g)=CO2(g)+H2O(l)△H=-570.8 kJ•mol-1,
根据盖斯定律,①-②可得:CH3OH(g)+$\frac{1}{2}$O2(g)═HCHO(g)+H2O(l),据此计算;
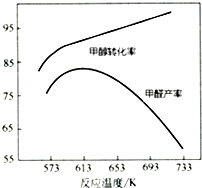
(2)反应的转化率较大,甲醛可被氧化生成CO和水;
(3)反应催化剂的活性与温度有关,较高温度时甲醇的转化率较高,但生成的甲醛存在副反应;
Ⅱ.(4)甲醇在负极被氧化生成二氧化碳和水;
(5)甲醇被氧化生成二氧化碳,C的化合价由-2价升高到+4甲,1mol失去6mol电子,额定输出电压为1.18V,可计算输出能量,结合反应热计算能量转化率.
解答 解:I.(1)由物质燃烧热数据可知:①CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1,
②HCHO(g)+O2(g)=CO2(g)+H2O(l)△H=-570.8 kJ•mol-1,
根据盖斯定律,①-②可得:CH3OH(g)+$\frac{1}{2}$O2(g)═HCHO(g)+H2O(l)△H=-726.5kJ•mol-1-(-570.8 kJ•mol-1)=-155.7kJ•mol-1;
故答案为:-155.7kJ•mol-1;
(2)反应的转化率较大,甲醛可被氧化生成CO和水,存在副反应,故答案为:反应平衡常数大,反应更彻底,但是存在副反应;
(3)反应催化剂的活性与温度有关,反应温度较低时催化剂活性较低,甲醇转化率低,甲醛产率较低,较高温度时甲醇的转化率较高,但生成的甲醛存在副反应,产率反而下降,
故答案为:反应温度较低时催化剂活性较低,甲醇转化率低,甲醛产率较低;反应温度升高后,甲醇转化率提高,但是发生副反应,产率反而下降;
(4)甲醇在负极被氧化生成二氧化碳和水,电极方程式为CH3OH-6e-+H2O═CO2+6H+,故答案为:CH3OH-6e-+H2O═CO2+6H+;
(5)甲醇被氧化生成二氧化碳,C的化合价由-2价升高到+4甲,1mol失去6mol电子,额定输出电压为1.18V,则输出能量为6mol×96500 C•mol-1×1.18V=683220J,而反应热为726.5×103 J,则转化率为$\frac{683220}{726.5×1{0}^{3}}×100%$=94.1%,
故答案为:94.1%.
点评 本题考查较为综合,涉及反应热与焓变、化学平衡的移动以及原电池知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,易错点为(5),注意计算的思路和方法.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 密闭、低温是存放氨水的必要条件 | |
| B. | 实验室常用排饱和食盐水法收集氯气 | |
| C. | 打开汽水瓶时,有大量气泡冒出 | |
| D. | 已知合成氨的反应为N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol,工业上采用较高温度和使用催化剂以提高氨气的产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cu2+、Cl-、SO42- | B. | Fe3+、K+、SO42-、NO3- | ||
| C. | H+、Mg2+、OH-、NO3- | D. | Na+、Ca2+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
温度/K | 298 | 398 | 498 | … |
| 平衡常数(K) | 4.1×105 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
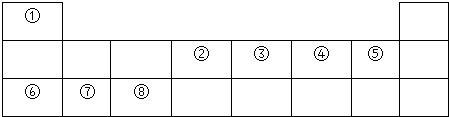
 .
. .
. ,其晶体类型属于分子晶体,④与⑥形成的原子个数比为1:1的化合物的电子式是
,其晶体类型属于分子晶体,④与⑥形成的原子个数比为1:1的化合物的电子式是 ,其晶体类型属于离子晶体.
,其晶体类型属于离子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化学键 | C-H | C-C | C═C | H-H |
| 键能/kJ•mol-1 | 412 | 348 | 612 | 436 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/K | 反应I | 反应Ⅱ | 已知: K1>K2>K1′>K2′ |
| 298 | K1 | K2 | |
| 328 | K1′ | K2′ |

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com