
¡¾̀âÄ¿¡¿Ä³ÖĐѧ»¯Ñ§ÑĐ¾¿ĐÔÑ§Ï°Đ¡×éÀûÓẲÔÏÂ×°ÖĂÖÆÈ¡²¢̀½¾¿°±ÆøµÄĐÔÖÊ£®AÖĐ·¢Éú·´Ó¦µÄ»¯Ñ§·½³̀ʽ£º2NH4Cl+Ca£¨OH£©2![]() CaCl2+2NH3¡ü+2H2O
CaCl2+2NH3¡ü+2H2O
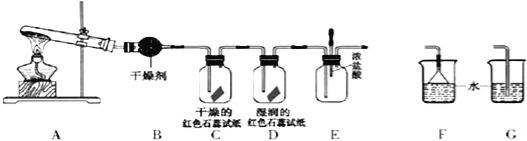
£¨1£©A×°ÖĂ»¹¿ÉÓĂÓÚÖÆÈ¡ Æø̀壨ֻ̀î̉»ÖÖ£©£®
£¨2£©ÈôÓĐ10.7gNH4Cl¹̀̀壬×î¶à¿ÉÖÆÈ¡NH3£¨±ê×¼×´¿ö£©µÄ̀å»ưÊÇ L£®
£¨3£©ÊµÑéỂÊƠ¼¯°±ÆøµÄ·½·¨ÊÇ £®
£¨4£©C¡¢D×°ÖĂÖĐÑƠÉ«»á·¢Éú±ä»¯µÄÊÇ £῭î¡°C¡±»̣¡°D¡±£©
£¨5£©µ±ÊµÑé½øĐĐ̉»¶Îʱ¼äºó£¬¼·Ñ¹E×°ÖĂÖĐµÄ½ºÍ·µÎ¹Ü£¬µÎÈë1¡«2µÎŨÑÎËᣬ¿É¹Û²́µ½µÄÏÖÏóÊÇ £®
£¨6£©Îª·ÀÖ¹¹ưÁ¿°±ÆøỐ³É¿ƠÆøÎÛȾ£¬Đè̉ªÔÚÉÏÊö×°ÖõÄÄ©¶ËÔö¼Ó̉»¸öβÆø´¦Àí×°ÖĂ£¬ºÏÊʵÄ×°ÖĂÊÇ £῭î¡°F¡±»̣¡°G¡±£©£®
¡¾´đ°¸¡¿£¨1£©O2£»£¨2£©4.48£¨3£©Ị̈ÏÂÅÅ¿ƠÆø·¨£¨4£©D£¨5£©ÓĐ°×Ñ̀Éú³É£¨6£©F
¡¾½âÎö¡¿½â£º£¨1£©¸Ă×°ÖĂÊǼÓÈȹ̀̀åÖƱ¸Æø̀åµÄ×°ÖĂ£¬»¹¿ÉÓĂÓÚÖÆÈ¡ÑơÆø£¬ÈçÂÈËá¼ØÔÚ¶₫Ñơ»¯ẰµÄ´ß»¯×÷ÓĂϼÓÈÈÉú³ÉÂÈ»¯¼ØºÍÑơÆø£¬·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ£º2KClO3![]() 2KCl+3O2¡ü£®
2KCl+3O2¡ü£®
¹Ê´đ°¸Îª£ºO2£»
£¨2£©n£¨NH4Cl£©¨T=![]() =0.2mol£¬¸ù¾Ư·´Ó¦·½³̀ʽ2NH4Cl+Ca£¨OH£©2
=0.2mol£¬¸ù¾Ư·´Ó¦·½³̀ʽ2NH4Cl+Ca£¨OH£©2![]() CaCl2+2NH3¡ü+2H2O¿ÉÖª£¬n£¨NH3£©=n£¨NH4Cl£©=0.2mol£¬Ëù̉ÔV£¨NH3£©=nVm=0.2mol¡Á22.4L/mol=4.48L£¬
CaCl2+2NH3¡ü+2H2O¿ÉÖª£¬n£¨NH3£©=n£¨NH4Cl£©=0.2mol£¬Ëù̉ÔV£¨NH3£©=nVm=0.2mol¡Á22.4L/mol=4.48L£¬
¹Ê´đ°¸Îª£º4.48£»
£¨3£©°±Æø̉×ÈÜÓÚË®£¬²»ÄÜÓĂÅÅË®·¨ÊƠ¼¯£¬°±ÆøĂܶȱȿƠÆøĐ¡£¬Ëù̉ÔÓĂỊ̈ÏÂÅÅ¿ƠÆø·¨ÊƠ¼¯£¬
¹Ê´đ°¸Îª£ºỊ̈ÏÂÅÅ¿ƠÆø·¨£»
£¨4£©°±ÆøÓë¸ÉÔïµÄº́ɫʯÈïÊÔÖ½²»±äÉ«£¬°±ÆøÓöË®Éú³É̉»Ë®ºÏ°±£¬µçÀë³öµÄÇâÑơ¸ùÀë×ÓÄÜʹº́ɫʯÈïÊÔÖ½±äÀ¶£¬Ëù̉Ô°±ÆøÄÜʹʪÈóµÄº́ɫʯÈïÊÔÖ½±äÀ¶£¬Ëù̉ÔDÖĐÑƠÉ«·¢Éú±ä»¯£¬
¹Ê´đ°¸Îª£ºD£»
£¨5£©°±ÆøºÍÂÈ»¯Çâ·´Ó¦Éú³É¹̀̀åÂÈ»¯ï§£¬½«Á½Ö§·Ö±đƠºÈ¡Å¨°±Ë®ºÍŨÑÎËáµÄ²£Á§°ô¿¿½ü£¬Å¨°±Ë®»Ó·¢³öµÄ°±ÆøºÍŨÑÎËá»Ó·¢³öµÄÂÈ»¯ÇâÏàÓö·´Ó¦£¬¿É̉Ô¹Û²́µ½²£Á§°ôÖ®¼ä³öÏÖ´óÁ¿°×Ñ̀£»
¹Ê´đ°¸Îª£ºÓĐ°×Ñ̀Éú³É£»
£¨6£©̣̉Ϊ°±Æø¼«̉×ÈÜÓÚË®£¬Ëù̉ÔÎüÊƠ°±Æøʱ̉ªÓĂ·Àµ¹Îü×°ÖĂ£¬Fµ¹¿ÛµÄ©¶·¾ßÓĐÇ̣Đβ¿·ÖÆđ»º³å×÷ÓĂ£¬ÄÜ·ÀÖ¹µ¹Îü£¬
¹Ê´đ°¸Îª£ºF£®


 ÖÇ»ÛĐ¡¸´Ï°ÏµÁĐ´đ°¸
ÖÇ»ÛĐ¡¸´Ï°ÏµÁĐ´đ°¸
| Ä꼶 | ¸ßÖĐ¿Î³̀ | Ä꼶 | ³ơÖĐ¿Î³̀ |
| ¸ß̉» | ¸ß̉»Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ở» | ³ở»Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ß¶₫ | ¸ß¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ơ¶₫ | ³ơ¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ßÈư | ¸ßÈưĂâ·Ñ¿Î³̀ÍƼö£¡ | ³ơÈư | ³ơÈưĂâ·Ñ¿Î³̀ÍƼö£¡ |
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ÈổªÊ¹0.5mol¼×ÍéºÍCl2·¢ÉúÈ¡´ú·´Ó¦£¬·´Ó¦ºóCH4ÓëCl2¾ùÎ̃Ê£Ó࣬²¢Éú³ÉµÄËÄÖÖÈ¡´ú²úÎïµÄÎïÖʵÄÁ¿̉À´ÎÔö¼Ó0.05mol£¬ỘĐè̉ªCl2µÄÎïÖʵÄÁ¿Îª£¨ £©
A£®1.75mol B£®2mol C£®1.25mol D£®1.5mol
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿¸ù¾ƯËùѧ֪ʶ£¬Çë»Ø´đÏÂÁĐÎỀ⣺
£¨1£©ÓĂÀë×Ó·½³̀ʽ±íʾ³ưÈ¥̀ú·ÛÖĐ»́ÓеÄÂÁ·Û ¡£
£¨2£©¼́²âFe2(SO4)3ÈÜ̉ºÖĐÊÇ·ñº¬ÓĐÉÙÁ¿µÄFeSO4µÄ²Ù×÷·½·¨ÊÇ__________________¡£
£¨3£©ÓĂH2O2ºÍÏ¡H2SO4µÄ»́ºÏÈÜ̉º¿ÉÈܳöÓ¡Ë¢µç·°å½đÊô·ÛÄ©ÖеÄÍ£¬ÇëĐ´³ö±íʾ¸Ă¹ư³̀µÄÀë×Ó·½³̀ʽ ¡£
£¨4£©¹¤̉µÖƱ¸´Ö¹èµÄ»¯Ñ§·½³̀ʽ ¡£
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ÏÂÁĐ˵·¨»̣ÍÆÀíƠưÈ·µÄÊÇ
A. ½«Fe(N03)2ÑùÆ·ÈÜÓÚÏ¡H2SO4ºó£¬µÎ¼ÓKSCNÈÜ̉º£¬ÈÜ̉º±äº́£¬ỘFe(N03)2¾§̀å̉ÑÑơ»¯±äÖÊ
B. ³£ÎÂÏ£¬pH¶¼Îª11µÄÇâÑơ»¯ÄÆÈÜ̉ººÍ°±Ë®¾ù¼ÓˮϡÊÍ100±¶£¬pH¶¼±äΪ9
C. 25¡æʱ£¬Ksp(BaCO3£©>Ksp(BaCrO4)£¬Ộ³ÁµíË®̀åÖеÄBa2+Ñ¡ÔñNa2CrO4±ÈNa2CO3ºĂ
D. ½«CH3CH2BrÓëNaOHÈÜ̉º¹²ÈÈ£¬ÀäÈ´ºóÈ¡³öÉϲăÈÜ̉º£¬¼ÓÈëAgNO3ÈÜ̉º£¬²úÉú³Áµí£¬ỘCH3CH2BrÔÚNaOHÈÜ̉ºÖĐ·¢ÉúÁËË®½â
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿£¨10·Ö)´¼ËáÊ÷Ö¬ÈỬ×¹̀»¯³ÉĤ£¬³ÉĤºóÓĐ¹âÔóºÍÈÍĐÔ£¬¸½×ÅÁ¦Ç¿£¬¾®¾ßÓĐÁ¼ºĂµÄÄÍÄ¥ĐԺ;øÔµĐÔµÈĐÔÄÜ£¬ÏÂĂæÊÇ̉»ÖÖ´¼ËáÊ÷Ö¬MµÄºÏ³É·Ïߣº

̉ÑÖª£º¢ÙÓĐ»úÎïCµÄºË´Å¹²ƠñÇâÆ×ÏÔʾֻÓĐÁ½ÖÖ²»Í¬»¯Ñ§»·¾³µÄÇâ
¢Ú
°´̉ªÇó»Ø´đÎỀ⣺
(1)FÖĐ¹ÙÄÜÍŵÄĂû³ÆΪ_______£¬̉ÑÖª̀ơ¼₫ÖĐ¢ÚµÄ·´Ó¦ÀàĐÍΪ_______
(2)BµÄ½á¹¹¼̣ʽΪ_______¡£
(3)Đ´³öC+F¡úMµÄ»¯Ñ§·½³̀ʽ£º_______¡£
(4)·ûºÏÏÂÁĐ̀ơ¼₫µÄ ͬ·Ö̉́¹¹̀åÓĐ______ÖÖ¡£
ͬ·Ö̉́¹¹̀åÓĐ______ÖÖ¡£
A£®ÄÜÓëŨäåË®·´Ó¦²úÉú°×É«³Áµí£¬Ç̉1mol¸ĂÎïÖÊ¿ÉÏûºÄ2molBr2
b£®ÄÜ·¢ÉúÏûÈ¥·´Ó¦
(5)Éè¼Æ̉Ô¼×È©ºÍ±ûȩΪÔÁÏÖƱ¸![]() µÄºÏ³É·Ïß(ÓĂÁ÷³̀ͼ±íʾ£¬Î̃»úÊÔ¼ÁÈÎÑ¡)×¢£ººÏ³É·ÏßµÄÊéĐ´¸ñʽ²ÎƠƠÈçÏÂʵÀư£º
µÄºÏ³É·Ïß(ÓĂÁ÷³̀ͼ±íʾ£¬Î̃»úÊÔ¼ÁÈÎÑ¡)×¢£ººÏ³É·ÏßµÄÊéĐ´¸ñʽ²ÎƠƠÈçÏÂʵÀư£º
![]()
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿̉ÑÖªÍÓëÏ¡ÏơËá·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ£º3Cu+8HNO3£¨Ï¡£©¨T3Cu£¨NO3£©2+2NO¡ü+4H2OÏÖ½«9.60gµÄ͵¥ÖʼÓÈëµ½¹ưÁ¿µÄ8.40%µÄÏ¡ÏơËáÖĐ£¬³ä·Ö·´Ó¦ºó£¬ÊÔÇó£º
£¨1£©±ê×¼×´¿öÏÂÉú³ÉNO¶àÉÙL£¿
£¨2£©ƠâЩ͵¥ÖÊÄÜÓë¶àÉÙgÉÏÊöÏ¡ÏơËáÇ¡ºĂÍêÈ«·´Ó¦£¿
£¨3£©·´Ó¦ÖĐÓжàÉÙmolHNO3±»»¹Ô£¿
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿Èç±íÊÇÔªËØÖÜÆÚ±íµÄ̉»²¿·Ö£¬°´̉ªÇó̀î¿Ơ£¨ ̀îÔªËØ·ûºÅ»̣»¯Ñ§Ê½£©£º
×å | ¢ñA | ¢̣A | ¢óA | ¢ôA | ¢ơA | ¢öA | ¢÷A | 0 |
2 | ¢Ù | ¢Ú | ¢Û | ¢Ü | ||||
3 | ¢Ư | ¢̃ | ¢ß | ¢à | ¢á | ¢â |
£¨1£©Đ´³ö¢ÙÔªËصÄÔªËØĂû³Æ £®
£¨2£©Đ´³ö¢âÔªËصÄÔªËØ·ûºÅ £®
£¨3£©¢áÔÚÔªËØÖÜÆÚ±íÖеÄλÖĂ£ºµÚ ÖÜÆÚ£¬µÚ ×壮
£¨4£©ÔÚƠâĐ©ÔªËØÖĐ£¬ ÊÇ×î»îÆĂµÄ½đÊôÔªËØ£» ÊÇ×î»îÆĂµÄ·Ç½đÊôÔªËØ£» ÊÇ×î²»»îÆõÄÔªËØ£®£¨ÓĂÔªËØ·ûºÅ̀îĐ´£©
£¨5£©ÄÜĐγÉÆø̀¬Ç⻯ÎÇ̉Æø̀¬Ç⻯Îï×îÎȶ¨µÄÊÇ £®£¨ÓĂ»¯Ñ§Ê½̀îĐ´£©
£¨6£©ƠâĐ©ÔªËصÄ×î¸ß¼ÛÑơ»¯Îï¶ÔӦˮ»¯ÎïÖĐ×îÇ¿µÄËáÊÇ £»×îÇ¿µÄ¼îÊÇ £»¾ßÓĐÁ½ĐÔµÄÇâÑơ»¯ÎïÊÇ £®£¨ÓĂ»¯Ñ§Ê½̀îĐ´£©
£¨7£©´Ó¢Ưµ½µÄÔªËØÖĐ£¬ Ô×Ӱ뾶×îĐ¡£®£¨ÓĂÔªËØ·ûºÅ̀îĐ´£©
£¨8£©±È½Ï¢ƯÓë¢̃µÄ»¯Ñ§ĐÔÖÊ£¬ ¸ü»îÆĂ£¨ÓĂÔªËØ·ûºÅ̀îĐ´£©£¬ÊÔÓĂʵÑéÖ¤Ă÷´ËÏÖÏ󣨼̣ÊöʵÑé²Ù×÷¡¢ÏÖÏóºÍ½áÂÛ£© £®
£¨9£©Óõç×Óʽ±íʾԪËØ¢ÜÓë¢̃ĐγɵĻ¯ºÏÎ £¬¸Ă»¯ºÏÎïÊôÓÚ £῭î¡°¹²¼Û¡±»̣¡°Àë×Ó¡±£©»¯ºÏÎ
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ÏÂÁĐĐÔÖÊ¿É̉ÔÖ¤Ă÷ij»¯ºÏÎïÄÚ̉»¶¨´æÔÚÀë×Ó¼üµÄÊÇ£¨¡¡¡¡£©
A.¿ÉÈÜÓÚË®
B.ÈÛÈÚ×´̀¬Äܵ¼µç
C.Ë®ÈÜ̉ºÄܵ¼µç
D.¾ßÓĐ½Ï¸ßÈÛµă
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
¡¾̀âÄ¿¡¿ö©ö©ÔÚ×Ôѧ̀¼ËáÄÆĐÔÖÊʱ£¬²éµ½ÁË̉ÔÏÂ×ÊÁÏ£º
¢Ù CO2+ Na2CO3+ H2O === 2NaHCO3£¬CO2ͨÈë±¥ºÍ̀¼ËáÄÆÈÜ̉º»á²úÉú°×É«³Áµí£¬CO2²»ÈÜÓÚ±¥ºÍ̀¼ËáÇâÄÆÈÜ̉º¡£
¢Ú ̀¼ËáÄÆ¡¢̀¼ËáÇâÄÆÔÚ²»Í¬Î¶ÈϵÄÈܽâ¶È
0¡æ | 10¡æ | 20¡æ | 30¡æ | |
Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
¡¾½øĐĐʵÑé1¡¿ÑéÖ¤CO2ͨÈë±¥ºÍ̀¼ËáÄÆÈÜ̉º»á²úÉú°×É«³Áµí
¢Ù ÅäÖÆ̀¼ËáÄÆÈÜ̉º£ºÈ¡100 g 20¡æµÄË®£¬¼ÓÈë35 g̀¼ËáÄƹ̀̀壬½Á°èºó£¬¾²ÖĂ£¬È¡ÉϲăÇå̉º¡£
¢Ú ÀûÓĂ×°ÖẲ»½øĐĐʵÑ飬Á¬Đø5·ÖÖÓỊ̈ĐÂÖÆµĂµÄ̀¼ËáÄÆÈÜ̉ºÖĐͨÈëCO2¡£

¡¾·¢ÏÖÎỀ⡿ʵÑéÖĐ£¬Ê¼ÖƠĂ»ÓĐ¿´µ½³ÁµíÏÖÏó£¬Ộ̉ÊÇÊ²Ă´ÄØ£¿ö©ö©½øĐĐÁË̉ÔÏÂʵÑé̀½¾¿¡£
¡¾½øĐĐʵÑé2¡¿
ʵÑé²Ù×÷ | ʵÑéÏÖÏó |
¢Ù È¡100 g 20¡æµÄË®£¬¼ÓÈë35 g̀¼ËáÄƹ̀̀壬½Á°èºó£¬¾²ÖĂ£¬È¡ÉϲăÇå̉º ¢Ú ÀûÓĂ×°Öö₫½øĐĐʵÑ飬Á¬Đø5·ÖÖÓỊ̈ĐÂÖÆµĂµÄ̀¼ËáÄÆÈÜ̉ºÖĐͨÈëCO2 | Ă»ÓĐ³öÏÖ°×É«³Áµí |
£¨1£©ÔÚ0¡æ~30¡æ£¬Na2CO3ºÍNaHCO3µÄÈܽâ¶ÈÊÜζȱ仯ӰḮ½Ï´óµÄÊÇ ¡£
£¨2£©´óÀíʯÓëÏ¡ÑÎËá·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ ¡£
£¨3£©×°Öö₫Öб¥ºÍ̀¼ËáÇâÄÆÈÜ̉ºµÄ×÷ÓĂÊÇ ¡£
¡¾½øĐĐʵÑé3¡¿
ʵÑé²Ù×÷ | ʵÑéÏÖÏó |
¢Ù È¡100 gÈÈ¿ªË®£¬¼ÓÈë35 g̀¼ËáÄƹ̀̀壬ÍêÈ«Èܽ⣬ÔÙ½µÎÂÖÁ20¡æ£¬È¡ÉϲăÇå̉º ¢Ú ÀûÓĂ×°ÖẲ»ºÍ×°Öö₫·Ö±đ½øĐĐʵÑ飬Á¬Đø3·ÖÖÓỊ̈ĐÂÖÆµĂµÄ̀¼ËáÄÆÈÜ̉ºÖĐͨÈëCO2 | ×°ÖẲ»ºÍ×°Öö₫ÖеÄ̀¼ËáÄÆÈÜ̉ºÖĐ¾ù³öÏÖ°×É«³Áµí |
£¨4£©ö©ö©ÔÚ×î³ơµÄʵÑéÖĐĂ»ÓĐ¿´µ½³ÁµíÏÖÏóµÄỘ̉ÊÇ ¡£
£¨5£©CO2ͨÈë±¥ºÍ̀¼ËáÄÆÈÜ̉º»á²úÉú°×É«³ÁµíµÄỘ̉ÊÇ ¡£
£¨6£©ÇëÄẳÀ¾ỪâÖĐĐÅÏ¢£¬Đ´³ö̉»ÖÖÄܹ»Çø·Ö̀¼ËáÄƺÍ̀¼ËáÇâÄƹ̀̀åµÄʵÑé·½°¸ ¡£
²é¿´´đ°¸ºÍ½âÎö>>
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com