
【题目】为了探究木炭与浓H2SO4反应的产物中是否存在CO2,某同学选用下图所示装置进行实验:
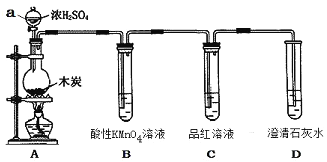
(1)仪器a的名称为:___________;在组装好上述实验装置后,在装入药品之前必需的实验操作是___________。
(2)写出A中发生反应的化学方程式_______________。
(3)装置B的作用是_______;该装置中发生的化学反应可说明SO2具有_______________性。
(4)已知SO2也可以使澄清的石灰水变浑浊,则能说明产物中一定存在CO2气体的实验现象为______________,____________。
【答案】 分液漏斗 检查装置的气密性 C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 吸收SO2 还原性 品红溶液不褪色 澄清的石灰水变浑浊
CO2↑+2SO2↑+2H2O 吸收SO2 还原性 品红溶液不褪色 澄清的石灰水变浑浊
【解析】试题分析:本题考查碳与浓硫酸的反应,通过实验探究C与浓硫酸反应的产物中是否存在CO2。
(1)根据仪器的特点,仪器a的名称为分液漏斗。由于实验与气体有关,在组装好实验装置后,装入药品之前必需的实验操作是:检查装置的气密性。
(2)在装置A中C与浓硫酸共热反应生成CO2、SO2和H2O,反应的化学方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(3)用澄清石灰水检验CO2,由于SO2也能使澄清石灰水变浑浊,所以检验CO2之前必须除尽SO2。装置B中酸性KMnO4用于除去SO2,B中的现象是紫红色溶液褪色,发生的反应为5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4,该反应表明SO2具有还原性。
(4)装置C中品红溶液的作用是检验SO2是否除尽,能说明产物中一定存在CO2的实验现象是:品红溶液不褪色,澄清的石灰水变浑浊。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】如图为反应2X(g)+Y(s)2Z(g)的反应过程和能量关系图,下列说法正确的是( ) 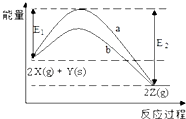
A.曲线a和b表示两个反应过程的反应热不同
B.曲线a一定表示反应是在无催化剂时的反应过程
C.增大压强,X的转化率一定增大
D.反应达平衡,升高温度,平衡常数K值一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.某学生在实验室利用如图的实验装置制备乙酸乙酯并研究其反应条件. 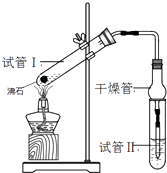
物质 | 沸点/°C | 密度/gcm﹣3 |
乙醇 | 78.0 | 0.79 |
乙酸 | 117.9 | 1.05 |
乙酸乙酯 | 77.5 | 0.90 |
异戊醇 | 131 | 0.8123 |
乙酸异戊酯 | 142 | 0.8670 |
实验步骤如下:
①配制反应混合液:2mL浓H2SO4、3mL乙醇、2mL乙酸
②按图连接实验装置并检验气密性
③分别在试管1、试管2中加入反应液
④用酒精灯微热3min,再加热使之微微沸腾3min
⑤分离提纯乙酸乙酯
(1)在试管1中加入物质分别是:(按着加入的先后顺序写出名称),乙醇过量的目的是:;
(2)该反应的平衡常数表达式K=;
(3)试管Ⅱ中所盛试剂为 , 欲将其物质分离使用的仪器为 , 在充分振荡的过程中,发生的反应为;
(4)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用右图所示装置进行了以下四个实验,实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
实验编号 | 试管Ⅰ中的试剂 | 测得有机层的厚度/cm |
A | 2mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 | 5.0 |
B | 3mL乙醇、2mL乙酸 | 0.1 |
C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 |
D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.实验D中应加入盐酸的体积和浓度分别是mL和mol/L;
②分析实验(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率.浓硫酸的吸水性能够提高乙酸乙酯产率的原因是
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是;
(5)若利用该装置制备乙酸异戊酯,产物将主要在装置中的得到,那么产率会(“较高”或“偏低”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断一个反应是否为氧化还原反应的标准是( )
A.是否有氧元素参加反应
B.是否为置换反应
C.元素的化合价在反应前后是否发生变化
D.是否为化合反应或分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)已知拆开1molH2、1molO2和液态水中1molO﹣H键使之成为气态原子所需的能量分别为436kJ、496kJ和462kJ;CH3OH(g)的燃烧热为627kJmol﹣1则CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=kJmol﹣1
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(l)
①该反应平衡常数表达式K=;
(3)已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示.该反应的△H0(填“>”或“<”),若温度不变,减小反应投料比[ ![]() ],则K将(填“增大”、“减小”或“不变”).
],则K将(填“增大”、“减小”或“不变”). 
(4)某温度下,向体积一定的密闭容器中通入CO2(g)与H2(g)发生上述反应,当下列物理量不再发生变化时,能表明上述可逆反应达到化学平衡的是;
A.二氧化碳的浓度
B.容器中的压强
C.气体的密度
D.CH3OCH3与H2O的物质的量之比.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,用电火花引爆 H2 和 Cl2 所组成的混合气体,反应停止后再恢复到原来的温度和压强, 测得气体体积与发生反应前恰好相等.则下列叙述合理的是( )
A. 与原混合气体中 H2 和 Cl2 的体积配比无关
B. 原混合气体中 H2 的体积一定大于 Cl2 的体积
C. 原混合气体中 H2 的体积一定小于 Cl2 的体积
D. 原混合气体中 H2 的体积恰好与 Cl2 的体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电解质中,①NaCl; ②NaOH;③NH3H2O; ④CH3COOH; ⑤BaSO4⑥H2O
(1)是弱电解质(填序号);
(2)pH相同的NaOH溶液与氨水,加水稀释相同的倍数后,pH大的是
(3)有pH均为2的盐酸、硫酸和醋酸三种溶液:盐酸和醋酸的浓度大小顺序为:
C(HCl)(CH3COOH)(填<、>或=),若分别用这三种酸中和含等物质的量的NaOH的溶液,所需酸的体积分别为a、b、c,则他们的关系是 .
(4)25℃时,有0.01mol/L的醋酸溶液,CH3COOH的电离方程式醋酸的电离平衡常数表达式 , 达平衡时溶液中氢离子的浓度(25℃,醋酸的电离常数为1.6×10﹣5;醋酸的电离程度很小,可近似认为醋酸的浓度不变).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com