
(14分)已知:CH3COOH CH3COO-+H+达到电离平衡时,电离平衡常数可以表示为Ka=
CH3COO-+H+达到电离平衡时,电离平衡常数可以表示为Ka= ;CH3COO-+H2O
;CH3COO-+H2O CH3COOH+OH-达到水解平衡时,水解平衡常数可以表示为Kh=
CH3COOH+OH-达到水解平衡时,水解平衡常数可以表示为Kh= (式中各粒子浓度均为平衡时浓度)。
(式中各粒子浓度均为平衡时浓度)。
(1)对于任意弱电解质来讲,其电离平衡常数Ka、对应离子的水解常数Kh以及水的离子积常数Kw的关系是_______________,由此可以推断,弱电解质的电离程度越小,其对应离子的水解程度____________。如在25 ℃时碳酸的K1 草酸的K1(填“大于”、“等于”或“小于”),所以,在相同条件下,碳酸氢钠的溶液显 性,而草酸氢钠溶液显酸性。
(2)由于CH3COOH的电离程度很小,计算时可将CH3COOH的平衡浓度看成是CH3COOH溶液的浓度,则c mol·L-1的CH3COOH溶液中c(H+)=_________(不为0)。
(3)现用某未知浓度(设为c′)的CH3COOH溶液及其他仪器、药品,通过实验测定一定温度下CH3COOH的电离平衡常数,需测定的数据有(用简要的文字说明):
①实验时的温度;②______________;③用____________(填一种实验方法)测定溶液浓度c′。
(14分)
(1)Ka·Kh=Kw 越大 小于 碱
(2) mol·L-1
mol·L-1
(3)②溶液的pH ③酸碱中和滴定
【解析】
试题分析:(1)已知CH3COOH CH3COO-+H+达到电离平衡时,电离平衡常数可以表示为Ka=
CH3COO-+H+达到电离平衡时,电离平衡常数可以表示为Ka= ;CH3COO-+H2O
;CH3COO-+H2O CH3COOH+OH-达到水解平衡时,水解平衡常数可以表示为Kh=
CH3COOH+OH-达到水解平衡时,水解平衡常数可以表示为Kh= ,水的离子积常数Kw=c(H+)·c(OH-),所以对于任意弱电解质来讲,其电离平衡常数Ka、对应离子的水解常数Kh以及水的离子积常数Kw的关系是Ka·Kh=Kw,根据三者之间的关系式可知,弱电解质的电离程度越小,其对应的离子水解程度越大,因为碳酸的酸性小于草酸的酸性,所以在25 ℃时碳酸的K1小于草酸的K1 ,在碳酸氢钠溶液中,HCO3- 的水解程度大于其电离程度,碳酸氢钠的溶液显碱性。
,水的离子积常数Kw=c(H+)·c(OH-),所以对于任意弱电解质来讲,其电离平衡常数Ka、对应离子的水解常数Kh以及水的离子积常数Kw的关系是Ka·Kh=Kw,根据三者之间的关系式可知,弱电解质的电离程度越小,其对应的离子水解程度越大,因为碳酸的酸性小于草酸的酸性,所以在25 ℃时碳酸的K1小于草酸的K1 ,在碳酸氢钠溶液中,HCO3- 的水解程度大于其电离程度,碳酸氢钠的溶液显碱性。
(2)由于醋酸电离出的醋酸根离子与氢离子浓度近似相等,平衡时醋酸又可以看成是醋酸溶液的浓度,又知KwW=c(H+)·c(OH-),所以(H+)=  mol·L-1
mol·L-1
(3)根据Ka= 知,要测定电离平衡常数,则必须知道氢离子浓度和醋酸浓度,要想知道氢离子浓度必须测定溶液的pH值,要想知道醋酸浓度则必须利用酸碱中和滴定的方法测定,所以需测定的数据有:②溶液的pH ③用酸碱中和滴定测定溶液的浓度.
知,要测定电离平衡常数,则必须知道氢离子浓度和醋酸浓度,要想知道氢离子浓度必须测定溶液的pH值,要想知道醋酸浓度则必须利用酸碱中和滴定的方法测定,所以需测定的数据有:②溶液的pH ③用酸碱中和滴定测定溶液的浓度.
考点:考查电解质溶液中平衡常数的关系,溶液中离子浓度的计算,平衡常数的测定等知识。
考点分析: 考点1:弱电解质的电离 试题属性

科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
已知一个SO2分子的质量为n kg,一个SO3分子的质量为m kg(设两种分子中S、O原子分别具有相同的中子数),若以硫原子质量的1/32作标准,SO2的相对分子质量为
A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三第二次模拟理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A. 的分子式为C17H24O3
的分子式为C17H24O3
B.结构为…—CH=CH—CH=CH—CH=CH—CH=CH—…的高分子化合物,其单体是乙炔
C.有机硅聚醚( )可由单体
)可由单体 和
和 缩聚而成
缩聚而成
D.等质量的甲醇、甲醛、甲醚完全燃烧时的耗氧量依次递增
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三下学期初考试理综化学试卷(解析版) 题型:填空题
氮元素的化合物应用十分广泛。请回答:
(1)火箭燃料液态偏二甲肼(C2H8N2)是用液态N2O4作氧化剂,二者反应放出大量的热,生成无毒、无污染的气体和水。已知室温下,1 g燃料完全燃烧释放出的能量为42.5 kJ,则该反应的热化学方程式为 。
(2)298 K时,在2 L固定体积的密闭容器中,发生可逆反应:
2NO2(g) N2O4(g) ΔH=-a kJ·mol-1(a>0)
N2O4(g) ΔH=-a kJ·mol-1(a>0)
N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:

① 298k时,该反应的平衡常数为 L·mol-1(精确到0.01)。
②下列情况不是处于平衡状态的是 :
A.混合气体的密度保持不变;
B.混合气体的颜色不再变化;
C.气压恒定时。
③若反应在398K进行,某时刻测得n(NO2)=0.6 mol,n(N2O4)=1.2 mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。
现向100 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.1 mol·L-1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,

①b点时,溶液中发生水解反应的离子是______;
②在c点,溶液中各离子浓度由大到小的排列顺序 。
③d、e点对应溶液中,水电离程度大小关系是d e(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三下学期初考试理综化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.将过量的CO2通入Ca(ClO)2溶液中:H2O+CO2+Ca +2ClO
+2ClO =CaCO3↓+2HClO
=CaCO3↓+2HClO
B.将少量NaOH溶液加入到NH4HCO3溶液中:OH-+HCO =CO
=CO +H2O
+H2O
C.Fe3O4与稀HNO3反应:Fe3O4+8H =Fe
=Fe +2Fe
+2Fe +4H2O
+4H2O
D.向NaHCO3溶液中加入少量Ca(OH)2:HCO +Ca
+Ca +OH
+OH =CaCO3↓+H2O
=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广西玉林市博白县高三下学期返校调研考试化学试卷(解析版) 题型:选择题
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。如图为RFC工作原理示意图,有关说法正确的是

A.转移0.1 mol电子时,a电极产生1.12 L H2
B.b电极上发生还原反应
C.酸性电解质溶液中H+移向c电极
D.d电极上发生的电极反应是:O2+4H++4e- = 2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省汕头市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
(16分)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。
(1)在一定条件下,CH4和CO2以镍合金为催化剂,发生反应:CO2(g)+CH4(g)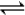 2CO(g)+2H2(g),其平衡常数为K,在不同温度下,K 的值如下:
2CO(g)+2H2(g),其平衡常数为K,在不同温度下,K 的值如下:

①从上表可以推断:该反应的逆反应是 (填“吸”、“放”)热反应。
②此温度下该反应的平衡常数表达式为K=__________________。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是_________。

②为了提高该反应中CH4的转化率,可以采取的措施是 。
③将Cu2Al2O4溶解在稀硝酸中的离子方程式为 。
(3)Li2O、Na2O、MgO均能吸收CO2。
①如果寻找吸收CO2的其他物质,下列建议合理的是________。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
②Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是__________________ _________。
查看答案和解析>>
科目:高中化学 来源:2015年期中备考总动员高三化学模拟卷【福建】3(解析版) 题型:推断题
【改编】[化学——有机化学基础](13分)香豆素是一种重要香料,以下是两种常见香豆素。

(1)关于香豆素和双香豆素,下列说法正确的是 (填序号)。
A.分子中碳碳双键
B.都属于芳香烃
C.香豆素和双香豆素都能发生取代、加成、酯化反应
D.1 mol双香豆素含羟基数为2NA(NA为阿伏加德罗常数的值)
(2)以甲苯为原料生产香豆素流程如下:

已知:(ⅰ)B可与FeCl3溶液发生显色反应;
(ⅱ)同一个碳原子上连两个羟基通常不稳定,易脱水形成羰基。
①C的结构简式是 。
②A的命名为__________________。B→C的反应类型是 。
③ 与乙酸酐(
与乙酸酐( )反应,除生成
)反应,除生成 外,另一种产物是 _____ 。(写出结构简式),这种产物与Na2CO3反应的方程式为________________________。
外,另一种产物是 _____ 。(写出结构简式),这种产物与Na2CO3反应的方程式为________________________。
④异香豆素与香豆素互为同分异构体,具有以下特点:
(a)含有苯环;
(b)含有与香豆素相似的两个六元环;
(c)1 mol异香豆素与足量NaOH溶液反应时消耗1 mol NaOH。
写出异香豆素的结构简式 _______ 。写出异香豆素与NaOH溶液反应的方程式为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com