
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
【题目】甲、乙两位同学分别按图1所示装置进行实验,甲同学在虚线框内接一个电流计,乙同学在虚线框内没有做连接,请回答下列问题:
(1)以下叙述正确的是______
A.甲同学实验中,石墨棒上无气泡产生
B.甲、乙两同学实验中的铁片都是负极
C.甲同学实验中,电子在溶液中没有迁移
D.甲、乙同学在实验中都发现有气泡生成,产生气泡的速率甲比乙慢
(2)甲同学观察到电流计指针发生偏转,根据实验中的发现,绘制了图2,X轴表示实验时流入正极的电子的物质的量,则Y轴可能表示______
A.石墨棒的质量B.铁棒的质量C.c(H+)D.c(SO42-)E.c(Fe2+)
(3)采用甲同学装置,实验时把稀硫酸换成硫酸铜溶液,请写出铁电极电极反应式:______,石墨电极观察到的现象______,发生了______反应(填“氧化”、“还原”或“非氧化还原”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是
A.氨遇硫酸冒白烟
B.氨在一定条件下能与氧气反应生成一氧化氮和水
C.氨是一种极易溶于水,且易液化的气体
D.氨能使酚酞试液变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:

(1)b极上的电极反应式为__,甲电池的总反应化学方程式是__。
(2)在粗铜的电解过程中,图中c电极的材料是__(填“粗铜板”或“纯铜板”);在d电极上发生的电极反应为__;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是__,电解一段时间后,电解液中的金属离子有__。
(3)如果要在铁制品上镀镍(二价金属,相对原子质量59),则f电极的材料是__(填“铁制品”或“镍块”,下同),e电极的材料是__。
(4)若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。试运用所学知识,回答下列问题:
Ⅰ.已知反应:①CH4(g)+H2O (g) ![]() CO(g)+3H2(g) ΔH=+206 kJ·mol-1
CO(g)+3H2(g) ΔH=+206 kJ·mol-1
②C(s)+H2O (g) ![]() CO(g)+ H2(g) ΔH=+131 kJ·mol-1
CO(g)+ H2(g) ΔH=+131 kJ·mol-1
(1)工业制取炭黑的方法之一是将甲烷隔绝空气加热到1300℃进行裂解。填写空白。CH4(g) ![]() C(s)+2H2(g) ΔH=________kJ·mol-1。
C(s)+2H2(g) ΔH=________kJ·mol-1。
(2)若800℃时,反应①的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=4.0 mol·L-1; c(H2O)=5.0 mol·L-1;c (CO)=1.5 mol·L-1;c(H2)=2.0 mol·L-1,则此时该可逆反应的状态是_______(填序号)
a.达到平衡 b.向正反应方向移动 c.向逆反应方向移动
Ⅱ.甲醇是一种可再生能源,工业上用CO与H2来合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g),回答下列问题:
CH3OH(g),回答下列问题:
(1)一定条件下,将CO与H2以物质的量之比1:1置于恒容密闭容器中发生以上反应,平衡时,下列说法正确的是_______。
A.v(H2)正=v(CH3OH)逆 B.2v(CO)=v(H2)
C.CO与H2转化率相等 D.CO与H2的物质的量之比不再改变
(2)图是该反应在不同温度下CO的转化率随时间变化的曲线。温度T1和T2大小关系是T1____T2(填“>”、“<”或“=”),对应温度的平衡常数大小关系是K1____K2(填“>”、“<”或“=”)。
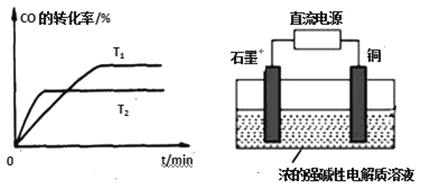
(3)用甲醇燃料电池作为直流电源,设计如图2装置制取Cu2O,写出铜电极的电极反应式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 是常见的几种元素,其相关信息如表:
元素 | 相关信息 |
X | 原子核外有 3 个电子层,最外层比次外层少 1 个电子 |
Y | 食盐中添加少量 Y 的一种化合物预防 Y 元素缺乏 |
Z | Z 与钾的一种合金可用于快中子反应堆作热交换剂 |
W | W 的一种核素质量数为 24,中子数为 12 |
(1)元素 X 在海水中含量非常高,海水中含 X 元素的主要化合物是_____。工业上制取 X单质的化学方程式为_____。
(2)设计实验证明某水溶液中存在 Y 单质_____。
(3)Z 的元素符号为_____,其原子结构示意图为_____。
(4)W 与空气中含量最高的气体反应的产物化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题
(1)写出漂白粉有效成分的化学式_____。水玻璃的主要成分化学式是_____。
(2)写出醋酸在水溶液中的电离方程式_____。
(3)炼铁、制水泥、玻璃,需要共同的原料是________。
(4)写出镁在二氧化碳中燃烧的化学方程式___________________。
(5)写出二氧化硅与焦炭反应的化学方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学知识与生产、生活密切相关。下列说法错误的是
A.SiO2是将太阳能转变为电能的常用材料B.Al(OH)3胶体具有吸附性,可用作净水剂
C.硫酸钡可用于胃肠X射线造影检查D.铝合金大量用于高铁建设
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com