
【题目】工业上以钒炉渣(主要含V2O3,还有少量SiO2、P2O5等杂质)为原料可以制备氧钒碱式碳酸铵晶体[(NH4)5(VO)6(CO3)4(OH)9·10H2O],其生产工艺流程如下。
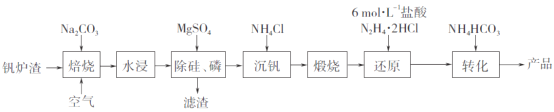
(1)焙烧过程中V2O3转化为可溶性NaVO3,该反应的化学方程式为_________________________________。
(2)滤渣的主要成分是________________(写化学式)。
(3)“沉钒”得到偏钒酸铵(NH4VO3),若滤液中c(VO3-)=0.1mol·L-1,为使钒元素的沉降率达到98%,至少应调节c(NH4+)为____mol·L-1。[已知Ksp(NH4VO3)=1.6×10-3]
(4)“还原”V2O5过程中,生成VOC12和一种无色无污染的气体,该反应的化学方程式为_______________________。用浓盐酸与V2O5反应也可以制得VOC12,该方法的缺点是____________________________。
(5)称量a g产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol·L-1KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知滴定反应为VO2++Fe2++2H+==VO2++Fe3++H2O)
①KMnO4溶液的作用是______________。
②粗产品中钒的质量分数表达式为________(以VO2计)。
③若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果_____(填“偏高”、“偏低”或“无影响”)。
【答案】V2O3+Na2CO3+O2![]() 2NaVO3+CO2 Mg3(PO4)2、MgSiO3 0.8 N2H42HCl+2V2O3+6HCl=4VOCl2+N2↑+6H2O 有氯气生成,污染空气 将VO2+氧化为VO2+
2NaVO3+CO2 Mg3(PO4)2、MgSiO3 0.8 N2H42HCl+2V2O3+6HCl=4VOCl2+N2↑+6H2O 有氯气生成,污染空气 将VO2+氧化为VO2+ ![]() 偏高
偏高
【解析】
钒炉渣(主要含V2O3,还有少量SiO2、P2O5等杂质),加入碳酸钠通入空气焙烧,产物加水溶解,向溶液中加入硫酸镁除去硅磷过滤,滤渣的主要成分为Mg3(PO4)2、MgSiO3.滤液中加入氯化铵沉钒生成NH4VO3,其受热分解生成V2O5,再用盐酸酸化的N2H42HCl还原V2O5生成VOCl2,最后再向反应后溶液中加入NH4HCO3,即可得到产品氧钒碱式碳酸铵晶体[(NH4)5(VO)6(CO3)4(OH)9·10H2O];
(5)①测定氧钒碱式碳酸铵晶体粗产品中钒的含量的原理为:氧钒碱式碳酸铵晶体溶解后,加0.02mol/LKMnO4溶液至稍过量,氧化其中+4价钒为VO2+,再加入NaNO2溶液除去过量的KMnO4,防止后续对标准液的消耗干扰试验,最后用(NH4)2Fe(SO4)2标准溶液滴定VO2+;
②根据钒元素的质量守恒,根据滴定反应为:VO2-+Fe2++2H+=VO2++Fe3++H2O,则钒元素的物质的量n=n((NH4)2Fe(SO4)2)=cmol/L×b×10-3L=cb×10-3mol,据此计算;
③若(NH4)2Fe(SO4)2标准溶液部分变质,则还原能力降低,滴定时消耗的标准液体积偏高,由此判断误差;
(1)将钒炉渣和碳酸钠在空气流中焙烧将V2O3转化为可溶性NaVO3,同时得到二氧化碳,发生反应的化学方程式为V2O3+Na2CO3+O2![]() 2NaVO3+CO2;
2NaVO3+CO2;
(2)焙烧时SiO2、P2O5分别与碳酸钠生成可溶于水的Na2SiO3和Na3PO4,除硅、磷时加入硫酸镁溶液生成Mg3(PO4)2、MgSiO3沉淀,则过滤时得到的滤渣的主要成分为Mg3(PO4)2、MgSiO3;
(3)已知Ksp(NH4VO3)=c(NH4+)c(VO3-)=1.6×10-3, 若滤液中c(VO3-)=0.1mol·L-1,为使钒元素的沉降率达到98%,则溶液中剩余c(VO3-)=0.1mol·L-1×2%=0.002 mol·L-1,此时c(NH4+)=![]() mol·L-1=0.8mol·L-1;
mol·L-1=0.8mol·L-1;
(4)用盐酸酸化的N2H42HCl还原V2O5生成VOCl2和一种无色无污染的气体,根据质量守恒定律,此气体应为N2,则发生反应的化学方程式为N2H42HCl+2V2O3+6HCl=4VOCl2+N2↑+6H2O;若改用浓盐酸与V2O5反应也可以制得VOC12,但同时得到的氧化产物为Cl2,此气体有毒,会污染环境;
(5)①根据分析,KMnO4溶液的作用是将+4价的钒氧化为VO2+;
②根据钒元素的质量守恒,根据滴定反应为:VO2-+Fe2++2H+=VO2++Fe3++H2O,则钒元素的物质的量n=n[(NH4)2Fe(SO4)2]=cmol/L×b×10-3L=cb×10-3mol,粗产品中钒的质量分数的表达式为![]() =
=![]() ;
;
③若(NH4)2Fe(SO4)2标准溶液部分变质,则还原能力降低,滴定时消耗的标准液体积偏高,根据滴定反应为:VO2-+Fe2++2H+=VO2++Fe3++H2O,可知会使测定结果偏高。


科目:高中化学 来源: 题型:
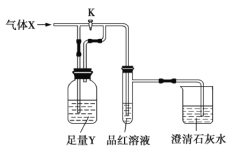
【题目】如图是一套检验气体性质的实验装置。请回答下列问题。
A | B | C | D | |
X | 氯气 | 二氧化硫 | 二氧化碳 | 氯化氢 |
Y | Na2SO3溶液 | 饱和NaHCO3溶液 | Na2SO3溶液 | 饱和NaHSO3溶液 |
(1)向装置中缓缓通入少量气体X,若关闭活塞K,则品红溶液褪色。据此判断气体![]() 和洗气瓶内的溶液Y可能的组合是_________(填表中序号,下同)。
和洗气瓶内的溶液Y可能的组合是_________(填表中序号,下同)。
(2)若打开活塞K,品红溶液褪色,同时澄清石灰水变浑浊,则气体X和洗气瓶内液体Y可能的组合是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下图实验装置进行实验。

(1)为了实现绿色环保的目标,能否用上图A2代替A1装置______(填“能”或“否”)。
(2)B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为____________
C中反应的离子方程式为__________________________,D中反应的化学方程为___________________。
(3)氨水吸收过量SO2的反应的离子方程式为__________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、W、M五种短周期元素,它们满足如下关系:①原子序数依次增大;②ZX4++WX-=ZX3+X2W,且反应物和产物中各微粒的电子总数与M+相等,均为10个;③Z2与YW分子中质子数相等。回答下列问题:
(1)YW2的电子式:______________;实验室中MWX溶液的保存方法是:________
(2)由X、Y、Z、W四种元素共同组成的离子化合物A,其原子个数比为5:1:1:3,则A的水溶液与足量的MWX溶液反应的离子方程式为:_________________________
(3)M2W2投入足量Na2S溶液中,生成浅黄色沉淀的离子方程式为:_______________
(4)与M同族的元素B和B2W共n 克投入到足量的X2W中完全反应,生成物蒸干后得1.25n 克化合物BWX,B是________(填元素名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的综合利用对促进“低碳经济”的发展有重要意义。
(1)工业上以CO2、NH3为原料生产尿素[CO(NH2)2],反应实际为两步进行:
I:2NH3(g)+CO2(g)![]() H2NCOONH4(s) △H1=-272kJ·mol-1
H2NCOONH4(s) △H1=-272kJ·mol-1
II:H2NCOONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+138kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2=+138kJ·mol-1
已知:H2O(l)==H2O(g) △H3=+44kJ·mol-1
①请写出以NH3、CO2为原料,合成尿素和液态水的热化学方程式______________。
②T1℃时,在1L的密闭容器中充入CO2和NH3模拟工业生产,n(NH3)/n(CO2)=x,如图是CO2平衡转化率(![]() )与x的关系。求图中A点NH3的平衡转化率
)与x的关系。求图中A点NH3的平衡转化率![]() =________%。
=________%。
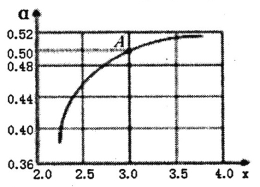
③当x=1.0时,若起始的压强为p0kPa,水为液态,平衡时压强变为起始的1/2。则该反应的平衡常数Kp=_______(kPa)-3(KP为以分压表示的平衡常数)。
(2)用CO2和H2合成甲醇:3H2(g)+CO2(g)![]() CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下:
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下:
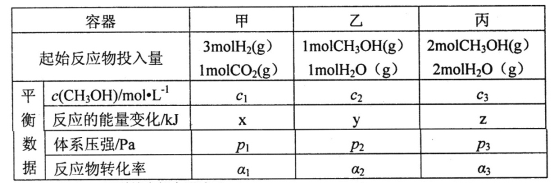
①甲容器10s达到平衡时测得x=39.2,则甲中CO2的平均反应速率____________。
②下列说法正确的是________(填字母编号)。
A.2c1<c3 B.z<2y C.p3>2p2 D.α1+α3>1
(3)用NaOH溶液做碳捕捉剂可获得化工产品Na2CO3。常温下若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=_____[K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11],溶液中c(Na+)_____c(HCO3-)+2c(CO32-)(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)若电解食盐水时消耗NaCl的质量为234 g,则在理论上最多可得氯气的体积为________升(标准状况)。
(2)若将2 mol的氯气通入足量石灰乳中,理论上可得到次氯酸钙________克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物的转化过程如图所示,下列分析合理的是

A. 催化剂a表面发生了极性共价键的断裂和形成
B. 在催化剂b表面形成氮氧键时,不涉及电子转移
C. N2与H2反应生成NH3的原子利用率为100%
D. 催化剂a、b能提高反应的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2是重要的耐温材料,可用作陶瓷遮光剂。天然锆英石(ZrSiO4)含有铁、铝、铜等金属元素的氧化物杂质,工业以锆英石为原料制备ZrO2的工艺流程如下: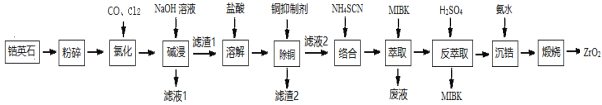
已知:①锆英石中锆元素的化合价为+4 ,“氯化”过程中除C、O元素外,其他元素均转化为最高价氯化物 ②SiCl4极易水解;ZrCl4易溶于水 ③Fe(SCN)3难溶于有机溶剂MIBK; Zr(SCN)4在水中溶解度不大,易溶于有机溶剂MIBK。
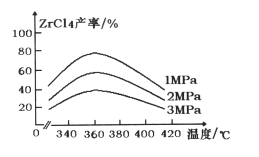
(1) “氯化”过程中,锆英石发生的主要反应的化学方程式为:______________________________,ZrC14的产率随温度变化如图所示,由图可知氯化的最佳条件是_____________;
(2)“滤液1”中含有的阴离子除OH- 、Cl-,还有___________________;
(3)常用的铜抑制剂有Na2S、H2S、NaCN等,本流程使用NaCN除铜,不采用Na2S、H2S的原因是__________。
(4)实验室进行萃取和反萃取的玻璃仪器是_______。流程中萃取与反萃取的目的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸广泛应用在稀有金属的湿法冶金、漂染工业、金属加工、无机药品及有机药物的生产等领域中。HCl极易溶于水,工业上用HCl气体溶于水的方法制取盐酸。
(1)用密度为1.2g/mL,质量分数为36.5%的浓盐酸配制250mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为__mL。
(2)溶液配制中需要的玻璃仪器有烧杯、玻璃棒、量筒、__、__。
(3)实验过程中,下列操作会导致最终所配溶液浓度偏高的是__。
A.量取浓盐酸时俯视刻度线
B.实验前,容量瓶中有少量残留蒸馏水
C.定容时俯视刻度线
D.转移时,未洗涤烧杯和玻璃棒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com