
【题目】ZrO2是重要的耐温材料,可用作陶瓷遮光剂。天然锆英石(ZrSiO4)含有铁、铝、铜等金属元素的氧化物杂质,工业以锆英石为原料制备ZrO2的工艺流程如下: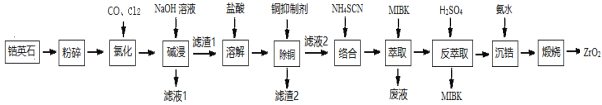
已知:①锆英石中锆元素的化合价为+4 ,“氯化”过程中除C、O元素外,其他元素均转化为最高价氯化物 ②SiCl4极易水解;ZrCl4易溶于水 ③Fe(SCN)3难溶于有机溶剂MIBK; Zr(SCN)4在水中溶解度不大,易溶于有机溶剂MIBK。
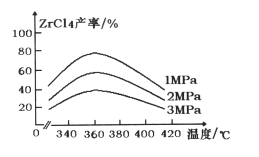
(1) “氯化”过程中,锆英石发生的主要反应的化学方程式为:______________________________,ZrC14的产率随温度变化如图所示,由图可知氯化的最佳条件是_____________;
(2)“滤液1”中含有的阴离子除OH- 、Cl-,还有___________________;
(3)常用的铜抑制剂有Na2S、H2S、NaCN等,本流程使用NaCN除铜,不采用Na2S、H2S的原因是__________。
(4)实验室进行萃取和反萃取的玻璃仪器是_______。流程中萃取与反萃取的目的是_________。
【答案】)ZrSiO4+4CO+4Cl2 ![]() ZrCl4 +SiCl4+4CO2 360℃、1MPa AlO2- 、SiO32- S2-会将Fe3+还原成Fe2+,影响下一步除铁,同时可能会产生污染性气体 分液漏斗、烧杯 除去铁元素杂质
ZrCl4 +SiCl4+4CO2 360℃、1MPa AlO2- 、SiO32- S2-会将Fe3+还原成Fe2+,影响下一步除铁,同时可能会产生污染性气体 分液漏斗、烧杯 除去铁元素杂质
【解析】
根据流程:天然锆石的主要成分是ZrSiO4(还常含有Fe、Al、Cu的氧化物杂质),将粉碎后的天然锆石用CO、Cl2氯化得到ZrCl4、SiCl4、AlCl3、FeCl3、CuCl2;用NaOH溶液碱浸时,SiCl4、AlCl3溶解为硅酸钠、偏铝酸钠,ZrCl4、FeCl3、CuCl2反应为Zr(OH)4、Fe(OH)3、Cu(OH)2沉淀,即为滤渣1;用盐酸溶解滤渣1得到ZrCl4、FeCl3、CuCl2;加入铜抑制剂除去铜[铜抑制剂可以为NaCN,生成沉淀为Cu(CN)2],滤渣2为Cu(CN)2;向滤液2加入NH4SCN与ZrCl4、FeCl3发生配合反应得到Fe(SCN)3、Zr(SCN)4,加入 有机溶剂MIBK萃取,Fe(SCN)3难溶于MIBK,分液,Zr(SCN)4在有机层,将含有Zr(SCN)4的有机层用硫酸反萃取将Zr(SCN)4与MIBK分离;通入氨气沉锆,经过煅烧得到ZrO2,据此分析作答。
(1) 氯化过程中ZrSiO4与CO、Cl2在高温下反应生成ZnCl4、SiCl4和CO2,反应的化学方程式为:ZrSiO4+4CO+4Cl2![]() ZnCl4+SiCl4+4CO2;由图可知,360℃、1MPa时,ZrCl4产率最高,此为氯化最佳条件;
ZnCl4+SiCl4+4CO2;由图可知,360℃、1MPa时,ZrCl4产率最高,此为氯化最佳条件;
(2)由流程分析可知,“滤液1”中含有的阴离子除OH- 、Cl-,还有AlO2- 、SiO32-;
(3)三价铁具有氧化性,S2-会将Fe3+还原成Fe2+,发生的反应为2Fe3++H2S=2Fe2++S+2H+(2Fe3++S2-=2Fe2++S),影响下一步除铁,同时可能会产生污染性H2S气体,故本流程使用NaCN除铜,不采用Na2S、H2S;
(4)实验室进行萃取和反萃取的玻璃仪器是分液漏斗、烧杯;根据已知信息“生成的Fe(SCN)3难溶于MIBK,Zr(SCN)4在水中的溶解度小于在MIBK中的溶解度”可知,流程中萃取与反萃取的目的是除去铁元素杂质。


科目:高中化学 来源: 题型:
【题目】工业水合碱碳酸镁简称轻质碳酸镁【3MgCO3.Mg(OH)2.3H2O】,相对密度小,质轻而松,广泛用于橡胶制品、防火保湿材料和日货用品中等。一种以富含氯化镁。硫酸镁的卤水和白云石【CaMg(CO3)2】为原料的卤水碳化法生产轻质碳酸镁的工艺流程如下:
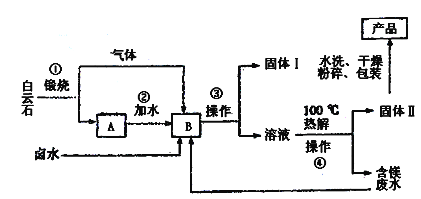
已知:MgCO3比CaCO3更易与CO2反应生成可溶性盐。
(1)为了使第①步白云石煅烧得更充分,常常要对矿石进行__预处理。
(2)第③步和第④步操作的名称是__,在实验室进行该操作时需要的玻璃仪器有
__。
(3)固体I的主要成分为____,固体II的主要成分为____。水洗固体II时,如何判断已经洗净,请简述其过程:____。
(4)写出第④步反应的化学方程式:____。
(5)该流程中能同体现提高效益、减少废物排放思想的两项设计是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钒炉渣(主要含V2O3,还有少量SiO2、P2O5等杂质)为原料可以制备氧钒碱式碳酸铵晶体[(NH4)5(VO)6(CO3)4(OH)9·10H2O],其生产工艺流程如下。
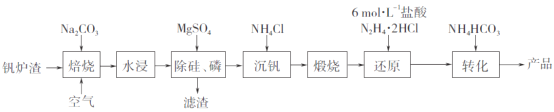
(1)焙烧过程中V2O3转化为可溶性NaVO3,该反应的化学方程式为_________________________________。
(2)滤渣的主要成分是________________(写化学式)。
(3)“沉钒”得到偏钒酸铵(NH4VO3),若滤液中c(VO3-)=0.1mol·L-1,为使钒元素的沉降率达到98%,至少应调节c(NH4+)为____mol·L-1。[已知Ksp(NH4VO3)=1.6×10-3]
(4)“还原”V2O5过程中,生成VOC12和一种无色无污染的气体,该反应的化学方程式为_______________________。用浓盐酸与V2O5反应也可以制得VOC12,该方法的缺点是____________________________。
(5)称量a g产品于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol·L-1KMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知滴定反应为VO2++Fe2++2H+==VO2++Fe3++H2O)
①KMnO4溶液的作用是______________。
②粗产品中钒的质量分数表达式为________(以VO2计)。
③若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果_____(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的氧化物,用7.0 mol/L的盐酸100 mL在一定条件下恰好完全溶解,所得溶液中再通入0.56L标况下的Cl2时,刚好使溶液中的Fe2+全部转化为Fe3+,则该氧化物中Fe2+与Fe3+的物质的量之比为
A.1:4B.2:1C.4:1D.3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硫酸铝、硫酸钾和明矾的混合溶液中,硫酸根离子的浓度为0.4mol·L-1,当加入等体积0.4mol·L-1氢氧化钾溶液时,生成的沉淀恰好完全溶解。则反应后溶液中钾离子的浓度约为( )
A.0.225mol·L-1B.0.25mol·L-1C.0.45mol·L-1D.0.9mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯水是实验室常需临时配制的一种试剂。图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀,可用于向瓶中鼓入空气的仪器)(已知常温下KMnO4固体与浓盐酸反应产生氯气)。

(1)氯水中含有七种粒子,其中的分子为__(化学式);需临时配制的原因是__(用化学方程式表示)。
(2)图甲所示装置中,烧杯内的液体是__,烧杯中发生反应的化学方程式是__。
(3)用图乙所示装置中配制氯水时,操作步骤如下:
①关闭活塞2,打开分液漏斗上口的玻璃塞,再打开活塞1,将少量浓盐酸注入大试管内。
②关闭活塞1,盖上分液漏斗上口玻璃塞。浓盐酸和大试管内的高锰酸钾粉末反应产生氯气。
③轻轻摇动瓶A,使氯气不断溶入水中。
用图乙装置能在较短时间内得到饱和氯水。除了在摇动过程中增大了气体和水的接触面以外,另一个重要原因是__。
分液漏斗中的浓盐酸应分数次加入试管内。若一次加入太多的浓盐酸,可能引起的后果是__。
(4)配制氯水完成后,不必拆卸装置即可从瓶A中取用少量氯水,方法是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种有机物,请回答下列问题:
A. | B. | C. |
D.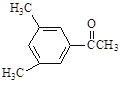 E.
E.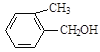 F.
F.![]()
(1)A物质中含有的官能团名称为_____________、______________。
(2)B的分子式为_________________。
(3)D的一氯代物最多有________________种。
(4)上述化合物中互为同分异构体的是_____;互为同系物的是____。(填字母)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组在T1温度下,容积为1 L的恒容密闭容器中,同时通入0.1 mol CO(g)和0.1 mol H2O(g),发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=a kJ· mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
CO2(g)+H2(g) △H=a kJ· mol-1。测得CO2的物质的量浓度随时间的变化关系如图所示。
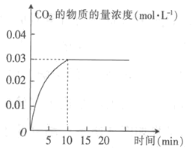
(1)0~10min内,CO的平均反应速率为_______________。
(2)T1温度下,该反应的平衡常数K为________(用分数表示)。
(3)①已知:
I.H2的燃烧热△H=-285.8 kJ· mol-1;
II.CO的燃烧热△H=-283 kJ· mol-1;
III.H2O(g)=H2O(l) △H=-44 kJ· mol-1。
则a=_______。
②反应达到平衡后,下列措施能使平衡向正反应方向移动的是__________(填字母)。
A 升高温度 B 增大压强 C 通入H2O(g) D 移走CO2(g)
(4)T1温度下,某时刻另一实验小组测得反应容器中有关数据为c(CO)=0.6 mol·L-1、c(H2O)=1.6 mol·L-1,c(H2)=0.4 mol·L-1,c(CO2)=0.4 mol·L-1,则该反应在下-时刻将____(填“向正反应方向进行”“向逆反应方向进行”或“达到平衡”),判断依据是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物 A 的相对分子质量为 62。为进一步测定 A 的化学式,现取 6.2 g A 完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重5.4 g 和 8.8 g(假设每步反应完全)。
(1)该有机物的实验式是_____;分子式是_____。
(2)红外光谱显示有“C—C”键和“O—H”键的振动吸收,若核磁共振氢谱只有 2 个吸收峰且峰面积之比为 1∶2,推断该有机物的结构简式是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com