
����Ŀ����ҵˮ�ϼ�̼��þ�������̼��þ��3MgCO3.Mg(OH)2.3H2O��������ܶ�С��������ɣ��㷺��������Ʒ������ʪ���Ϻ��ջ���Ʒ�еȡ�һ���Ը����Ȼ�þ������þ��±ˮ�Ͱ���ʯ��CaMg(CO3)2��Ϊԭ�ϵ�±ˮ̼������������̼��þ�Ĺ����������£�
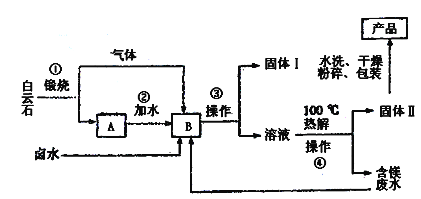
��֪��MgCO3��CaCO3������CO2��Ӧ���ɿ������Ρ�
��1��Ϊ��ʹ�ڢٲ�����ʯ���յø���֣�����Ҫ�Կ�ʯ����__Ԥ������
��2���ڢ۲��͵ڢܲ�������������__����ʵ���ҽ��иò���ʱ��Ҫ�IJ���������
__��
��3������I����Ҫ�ɷ�Ϊ____������II����Ҫ�ɷ�Ϊ____��ˮϴ����IIʱ������ж��Ѿ�ϴ�������������̣�____��
��4��д���ڢܲ���Ӧ�Ļ�ѧ����ʽ��____��
��5������������ͬ�������Ч�桢���ٷ����ŷ�˼������������____��
���𰸡� ���� ���� ©�����ձ��������� CaCO3 3MgCO3��Mg(OH)2��3H2O ȡ����ϴ��Һ���Թ��У�����HNO3�ữ��AgNO3��Һ����û�а�ɫ�������ɣ�����ϴ������֮��δϴ�� 4Mg(HCO3)2![]() 3MgCO3��Mg(OH)2��3H2O+5CO2�� �����հ���ʯ������CO2�ͺ�þ��ˮ����B��
3MgCO3��Mg(OH)2��3H2O+5CO2�� �����հ���ʯ������CO2�ͺ�þ��ˮ����B��
��������������Ҫ�������±ˮ̼������������̼��þ�Ĺ������̵����ۡ�
��1��Ϊ��ʹ�ڢٲ�����ʯ���յø���֣�����Ҫ�Կ�ʯ���з���Ԥ������
��2���ڢ۲��͵ڢܲ������õ��������Һ���������ǵ������ǹ��ˣ���ʵ���ҽ��иò���ʱ��Ҫ�IJ���������©�����ձ�����������
��3��MgCO3��CaCO3������CO2��Ӧ���ɿ������Σ�����I����Ҫ�ɷ�ΪCaCO3������II����Ҫ�ɷ־��Dz�Ʒ����Ҫ�ɷ�Ϊ3MgCO3��Mg(OH)2��3H2O������II��������±ˮ������Cl����![]() �����ӣ��ж�ˮϴ����II�Ƿ��Ѿ�ϴ���������ж�������Cl����
�����ӣ��ж�ˮϴ����II�Ƿ��Ѿ�ϴ���������ж�������Cl���� ![]() �Ƿ��Ѿ�ϴ�������Լ���Cl��������̣�ȡ����ϴ��Һ���Թ��У�����HNO3�ữ��AgNO3��Һ����û�а�ɫ�������ɣ�����ϴ������֮��δϴ����
�Ƿ��Ѿ�ϴ�������Լ���Cl��������̣�ȡ����ϴ��Һ���Թ��У�����HNO3�ữ��AgNO3��Һ����û�а�ɫ�������ɣ�����ϴ������֮��δϴ����
��4���ڢܲ���Ӧ�Ļ�ѧ����ʽ��4Mg(HCO3)2![]() 3MgCO3��Mg(OH)2��3H2O+5CO2����
3MgCO3��Mg(OH)2��3H2O+5CO2����
��5������������ͬʱ�������Ч�桢���ٷ����ŷ�˼�����������ǰ����հ���ʯ������CO2�ͺ�þ��ˮ����B�С�


 �żӾ���ϵ�д�
�żӾ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������������У��ȴ����ڶ���ϸ�����ִ�����ֲ��ϸ���ڵ��ǣ� ��
A. ���ۺͺ���
B. �����ǡ����Ǻ���ѿ��
C. ���ǡ��������Ǻ�������
D. ��ԭ�����ǡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̣���ѧ���ļ������γɣ����1mol��ѧ��ʱ�ͷţ������գ�������������֪����P4O6�ķ��ӽṹ����ͼ��ʾ�����ṩ���»�ѧ���ļ��ܣ�kJmol��1��P��P��198 P��O��360 O�TO��498��ӦP4�����ף�+3O2��P4O6�������仯Ϊ�� �� 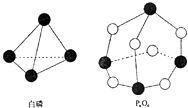
A.�ͷ�1638kJ������
B.����1638kJ������
C.�ͷ�126kJ������
D.����126kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ݻ�Ϊ2L���ܱ������У�����0.8mol��A2�����0.6mol B2���壬һ�������·������·�Ӧ��A2��g��+B2��g��2AB��g����H��0����Ӧ�и����ʵ�Ũ����ʱ��ı仯�����ͼ��ʾ������˵������ȷ���ǣ� �� 
A.ͼ��a���ֵΪ0.15
B.�÷�Ӧ��ƽ�ⳣ��K=0.03
C.�¶����ߣ�ƽ�ⳣ��Kֵ��С
D.ƽ��ʱA2��ת����Ϊ62.5%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ���仯�����������������й㷺Ӧ�ã�ͭ�ڻ������еij������ϼ���+l��+2����֪Cu2O��ϡ���ᷴӦ����Һ����ɫ��
��1����ҵ�Ͽ���Cu2S+O2 ![]() 2Cu+SO2��Ӧ��ȡ��ͭ������32gCu2S����ʱ������ת����Ŀ�� ��
2Cu+SO2��Ӧ��ȡ��ͭ������32gCu2S����ʱ������ת����Ŀ�� ��
��2��������ͭ˿����������ϡ�����У��¶ȿ�����50�棬����H2O2 �� ��Ӧһ��ʱ������µ�60�棬�ٷ�Ӧһ��ʱ�����Ƶ�����ͭ���¶ȿ�����50�橁60�������ԭ����˼ӿ췴Ӧ�����⣬���� �� ��CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ���ȣ�����CuCl������д������CuCl�����ӷ���ʽ ��
��3��ijС��ͬѧ����ͭ��Ũ���ᷴӦ��ʵ��ʱ������ͭƬ�����к�ɫ�������ɣ�
�ټ�ͬѧ���룺��ɫ������δ���ü��ܽ������CuO���������û�ѧ����ʽ��ʾΪ��Cu+H2SO4 ![]()
����ͬѧ��Ϊ����ɫ�����CuO����ܺ���Cu2S��CuS�������ɿ�����������ĸ��
a Cu2S��CuS���Ǻ�ɫ��
b ͭ��Ũ�����ڼ��������·�Ӧ�������ܷų�O2
c Ũ��������������ͭ�ǻ�ԭ����Cu�Ļ��ϼ�������S�Ļ��ϼ��½��ж��ֿ���
��4������Cu��Cu2O��CuO��ɵĻ�����У�����1L 0.6mol/L HNO3��Һǡ��ʹ������ܽ⣬ͬʱ�ռ���2240mL NO���壨��״������Cu2O��ϡ���ᷴӦ�����ӷ���ʽ �� ���������������������H2���Ȼ�ԭ�����õ����������Ϊg����������к�0.1mol Cu�����û������ϡ�����ַ�Ӧ����������H2SO4�����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������AlON����һ������Ӳ�ȷ������ϣ������ɷ�ӦAl2O3+C+N2 ![]() 2AlON+CO�ϳɣ������й�˵����ȷ���ǣ� ��
2AlON+CO�ϳɣ������й�˵����ȷ���ǣ� ��
A.���������е��Ļ��ϼ��ǩ�3
B.��Ӧ����������ͻ�ԭ��������ʵ���֮����2��1
C.��Ӧ��ÿ����5.7g AlON ͬʱ����1.12 L CO
D.��Ӧ�е�������ԭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ֱ������������ӵ���Һ��ͨ������NO2���壬��Ŀ������ٵ���
A.SO32-B.CH3COO-C.Fe2+D.Al3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǿ��淴Ӧ 2Y2Z2 �ڷ�Ӧ�����еķ�Ӧ���ʣ�v����ʱ�䣨t���Ĺ�ϵ���ߣ�����������ȷ���ǣ� �� 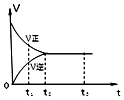
A.t1ʱ��ֻ��������Ӧ
B.t2��t3 �� ��Ӧ���ٷ���
C.t2��t3 �� �����ʵ�Ũ�Ⱦ�û�з����仯
D.t2ʱ����Ӧ�����ȣ�����Ӧ���淴Ӧ��������ҵ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com