
【题目】化学在生活中有着广泛的应用,下列对应关系正确的是()
选项 | 化学性质 | 实际应用 |
A | Al2(SO4)3和苏打Na2CO3溶液反应 | 泡沫灭火器灭火 |
B | 油脂在酸性条件下的水解反应 | 工业生产中制取肥皂 |
C | 醋酸具有酸性 | 食醋除水垢 |
D | SO2具有漂白性 | 可用于食品增白 |
A.AB.BC.CD.D
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】已知:①C(s)+ ![]() O2(g)═CO(g);△H=﹣110.5kJmol﹣1
O2(g)═CO(g);△H=﹣110.5kJmol﹣1
②C(s)+O2(g)═CO2(g);△H=﹣393.51kJmol﹣1
则反应C(s)+CO2(g)═2CO(g)的△H为( )
A.﹣283.01 kJmol﹣1
B.+172.51 kJmol﹣1
C.+283.01 kJmol﹣1
D.﹣172.51 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3 、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3 + CO2 + H2O = NH4HCO3 ; NH4HCO3 + NaCl = NaHCO3↓+ NH4Cl ; 2NaHCO3 = Na2CO3 + CO2↑+ H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是__________ (填标号)。
A.碳酸氢钠难溶于水 B.碳酸氢钠受热易分解
C.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。

试回答下列有关问题:
(Ⅰ)乙装置中的试剂是___________;
(Ⅱ)丁装置中稀硫酸的作用是_____________________________________。
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是__________ (填分离操作的名称)。
②另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从____管通入_______ 气体,再从_____管中通入________气体。
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq) + Cu(s) = Cu2+(aq) + 2Ag(s)设计的原电池如图所示,请回答下列问题:
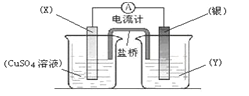
(1)电极X的材料是:________(填化学式);电解质溶液Y是:_________;
(2)银电极为电池的_______极,发生的电极反应为:___________________,X电极上发生的电极反应为:_____________________________________;
(3)外电路中的电子是从_________电极流出(填“X”或“银”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应式为:Zn﹣2e﹣+2OH﹣=Zn(OH)2
B.放电时每转移3mol电子,正极有1 mol K2FeO4被还原
C.充电时阴极附近溶液的碱性增强
D.放电时正极反应式为:Fe(OH)3﹣3e﹣+5OH﹣=FeO42﹣+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HBr被O2氧化依次由如下Ⅰ、Ⅱ、Ⅲ、三步反应组成,1molHBr被氧化为Br2放出12.67kJ热量,其能量与反应进程曲线如图所示。
(Ⅰ)HBr(g)+O2(g)==HOOBr(g)
(Ⅱ)HOOBr(g)+ HBr(g)==2HOBr(g)
(Ⅲ)HOBr(g)+ HBr(g)== H2O(g)+ Br2(g)
下列说法正确的是

A. 三步反应均为放热反应
B. 步骤(I)的反应速率最慢
C. HOOBr比HBr和O2稳定
D. 热化学方程式为4HBr(g)+O2(g)==2H2O(g)+2Br2(g) △H=-12.675kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 镁常用于制造信号弹和焰火
B. 碘化银和干冰常用于人工降雨
C. 二氧化硅常用于制造太阳能电池
D. 钠不慎着火时,不能用泡沫灭火剂灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙、丁四种短周期元素,它们的原子序数依次增大,其中甲和丙、乙和丁分别是同主族元素,甲的一种常见氧化物常温下呈液态,又知乙和丁两元素的原子核中质子数之和是甲和丙两元素原子核中质子数和的2倍,这四种元素的单质中气体和固体各两种.按要求回答下列问题:
(1)写出元素名称:甲 , 乙;
(2)丙在周期表中的位置:;
(3)丁的气态氢化物的电子式 .
(4)在由甲、乙、丙、丁四种元素两两组成的常见化合物中,其结构存在非极性键的离子化合物有;其结构中存在非极性键的共价化合物有;(各填写一种物质的化学式)
(5)写出两种均含有甲、乙、丙、丁四种元素的常见化合物:、;这两种物质的水溶液与KOH溶液反应的离子方程式分别是:、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法正确的是
A.除去CO2中少量的SO2气体:将气体通过饱和碳酸钠溶液
B.除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后静置
C.除去SiO2中的Al2O3:加入稍过量的NaOH溶液充分反应后过滤
D.除去NO2气体中少量的NH3:将气体通过水溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com