
【题目】同温同压下相同体积的两种气体12C18O和14N2,下列判断正确的是( )
A.分子数目相等B.中子数相等
C.密度之比为14:15D.电子数之比为2:3
【答案】A
【解析】
A.同温同压下,其体积之比=物质的量之比=分子个数之比,相同体积的两种气体12C18O和14N2含有相同的分子数,故A正确;
B.每个12C18O和14N2分子中中子数分别是16、14,相同体积的两种气体12C18O和14N2含有相同的分子数,因为其分子中中子数之比为8:7,所以其总中子数不等,故B错误;
C.同温同压下,气体摩尔体积相等,两种气体12C18O和14N2的摩尔质量分别是30 g/mol、28g/mol,根据![]() 知,其密度之比等于摩尔质量之比,二者的摩尔质量之比为15:14,所以其密度之比为15:14,故C错误;
知,其密度之比等于摩尔质量之比,二者的摩尔质量之比为15:14,所以其密度之比为15:14,故C错误;
D.同温同压下,其体积之比=物质的量之比=分子个数之比,每个12C18O和14N2分子中电子数都是14个,所以二者的电子数相等,故D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】三支体积相等的试管分别充满相同状态下气体:①氨气;②体积比为4:l的NO2和O2气体;③NO2气体;将他们分别倒立于盛有足量水的水槽中,液面恒定后(假设试管内液体不扩散),则下列结论正确的是( )
A.①和③试管内溶液体积不等,溶质物质的量浓度也不相等
B.因为它们都可溶于水,所以液面都上升到试管顶部
C.三支试管中,试管②中溶液中溶质的物质的量浓度最小
D.试管②和试管③中溶液的溶质的物质的量浓度一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前很多工厂实现了烟气的脱硫脱硝和氨氮废水的无害化处理,回答下列问题:
(1)某小组同学在实验室里尝试模拟工厂处理氨氮废水(主要含NH![]() )的不同方法,过程如下:①甲同学采用Ca(ClO)2作为氧化剂。将废水中的NH
)的不同方法,过程如下:①甲同学采用Ca(ClO)2作为氧化剂。将废水中的NH![]() 转化为无毒气体。他在实验中发现其他条件相同时,Ca(ClO)2的浓度越大碱性越强,处理后的废水中亚硝酸盐(NO
转化为无毒气体。他在实验中发现其他条件相同时,Ca(ClO)2的浓度越大碱性越强,处理后的废水中亚硝酸盐(NO![]() )的浓度也随之变大,写出该反应的离子方程式:___。
)的浓度也随之变大,写出该反应的离子方程式:___。
②乙同学在实验室模拟工业上的“吹脱法”测定废水的含氮量,设计了以下实验:精确称取wg废水样品,注入如所图示的仪器中,然后逐滴加入足量10%NaOH溶液,通入水蒸气。将样品液中的氨全部蒸出,用V1mLc1mol·L-1盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2molL-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
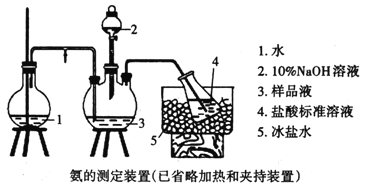
NH4Cl的电子式为___。盛放样品液的仪器是___(填名称);圆底烧瓶中长玻璃导管的作用是___;冰盐水的作用是___。
(2)某工厂利用NaClO2/(NH4)2CO3溶液脱除烟气中的SO2和NO。①保持溶液中NaClO2的浓度不变,研究(NH4)2CO3的浓度对NO和SO2脱除效率的影响[已知:(NH4)2CO3溶液显碱性;NaClO2的氧化性随pH增加而下降,酸性条件下会生成ClO2]。实验结果如图所示,随着(NH4)2CO3溶液浓度的增大造成NO脱除效率下降的主要原因是___。
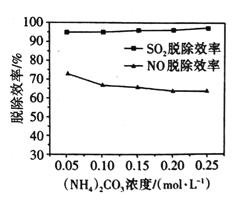
②NO脱除效率总是小于SO2脱除效率的主要原因是___。(写出一点)
(3)某工厂采用微生物硝化法处理氨氮废水,过程如图:
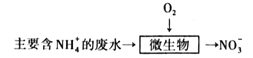
下列有关说法正确的是___(填标号)。
①微生物硝化法处理废水后会导致水体的pH升高
②若微生物保持活性的pH范围为7~9,则适宜用来调节水体pH的是CO2
③不能采用电解法在阴极将NH![]() 直接转化为NO
直接转化为NO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向一密闭容器中充入一定量的NH3,反应2NH3(g)![]() N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是

A. 压强:p1>p2
B. b、c两点对应的平衡常数:Kc>Kb
C. a点:2v(NH3)正=3v(H2)逆
D. a点:NH3的转化率为1/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化一定属于化学变化的是( )
①金属导电 ②燃烧 ③煤的干馏 ④焰色反应 ⑤无水硫酸铜吸水 ⑥工业制氧气 ⑦白磷转变成红磷 ⑧久置浓硝酸变黄 ⑨丁达尔现象 ⑩煤旳液化
A.①④⑨B.⑥⑧⑩C.②⑥⑦D.②③⑤⑦⑧⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A.使pH试纸显深蓝色的溶液中:S2-、NO![]() 、Br-、SO
、Br-、SO![]()
B.与铝粉反应放出H2的无色溶液中:Cl-、Al3+、Na+、SO![]()
C.氯化钠溶液中:Ag+、NH![]() 、Ca2+、ClO-
、Ca2+、ClO-
D.稀硫酸溶液中:Fe2+、NO![]() 、Na+、K+
、Na+、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中离子在水溶液中能大量共存且满足相应要求的是( )
选项 | 离子 | 要求 |
A | K+、NO | c(K+)<c(Cl-) |
B | Na+、NO | 逐滴滴加盐酸立即有气体产生 |
C | Na+、Al3+、Mg2+、SO | 逐滴滴加氨水立即有沉淀产生 |
D | NH | 滴加NaOH浓溶液立刻有气体产生 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用H2C2O4(草酸)作助溶剂,酸浸提取硫酸烧渣(主要含Fe2O3、FeO、SiO2等)制备铁红并回收副产物硫酸铵的工艺流程如图:
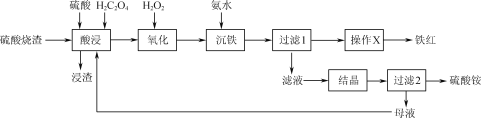
已知:H2C2O4可沉淀Ca2+、Fe2+等金属离子,可与Fe3+生成[Fe(C2O4)3]3-,在硫酸作用下可热分解生成CO和CO2。
(1)用50%的硫酸“酸浸”时,反应液的温度、H2C2O4的加入量对铁浸取率的影响分别如图1、图2所示:
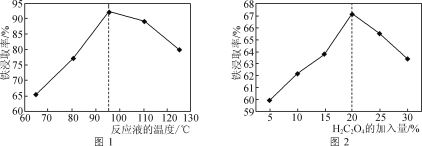
①“硫酸烧渣”中Fe2O3与H2SO4反应的化学方程式为___。
②图1中,反应液的温度高于95℃时,铁浸取率开始降低,其原因是___。
③图2中,H2C2O4加入量在5~20%时,铁浸取率随加入量的增大而增大,其原因是__;H2C2O4加入量超过20%时,铁浸取率反而开始降低,其原因是___。
(2)“沉铁”时发生的主要反应的离子方程式为____。
(3)由“过滤1”的滤渣制备铁红的“操作X”为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知由金属钠制得氧化钠,可用多种方法:a.4Na+O2===2Na2O,b.4Na+CO2===2Na2O+C,c.2NaNO2+6Na===4Na2O+N2↑。
①在上述三种方法中,最好的方法是________(填序号),原因是________________。
②上述反应c中NaNO2作________剂,当有1 mol NaNO2反应时,电子转移的数目是________________________________________________________________________。
(2)现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如下。回答下列问题(注:Na2O2可以与H2O、CO2反应):
①装置Ⅳ中盛放的药品是________,其作用是____________________________。


②若规定气体的气流方向从左到右,则组合实验装置时各仪器接口的标号字母(a、b……)顺序:空气进入________,________接________,________接________,________接________。
③装置Ⅱ的作用____________________________________________________。
④操作中通空气和加热的顺序为________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com