

分析 (1)根据题中各物质转化关系,若C为淡黄色化合物,D是一种强碱,则C为Na2O2,D为NaOH,E为O2,A、B分别为氧气、Na中的一种;
(2)若E为18电子微粒,且E的水溶液呈弱酸性,D是既能溶于强酸、又能溶于强碱的化合物,则C为Al2S3,E为H2S,D为Al(OH)3,A、B分别为Al、S中的一种;
(3)若C是一种气体,D是一种强酸,则C为NO2,D为HNO3,E为NO,据此解答.
解答 解:(1)若C为淡黄色化合物,D是一种强碱,C为Na2O2,D为NaOH,E为O2,A、B分别为氧气、Na中的一种,故答案为:Na2O2;
(2)若E为18电子微粒,且E的水溶液呈弱酸性,D是既能溶于强酸、又能溶于强碱的化合物,C为Al2S3,E为H2S,D为Al(OH)3,A、B分别为Al、S中的一种,则:
①用电离方程式解释D既能溶于强酸、又能溶于强碱的原因:H++H2O+AlO2-?Al(OH)3?Al3++3OH-,
故答案为:H++H2O+AlO2-?Al(OH)3?Al3++3OH-;
②H2S与NaOH溶液反应生成正盐为Na2S,溶液中硫离子水解,用电荷守恒的等式表示溶液中所有离子的浓度之间的关系为:c(Na+)+c(H+)═2c(S2-)+c(HS-)+c(OH-),
故答案为:c(Na+)+c(H+)═2c(S2-)+c(HS-)+c(OH-);
(3)若C是一种气体,D是一种强酸,C为NO2,D为HNO3,E为NO,则:
①C与水反应的化学方程式为:3NO2+H2O═2HNO3+NO,故答案为:3NO2+H2O═2HNO3+NO;
②常温下物质A与物质B生成1mol气体C的△H为-57kJ•mol-1,则:
反应的热化学方程式为:①2NO(g)+O2(g)=2NO2(g)△H=-114kJ•mol-1,
1mol气体C与H2O反应生成D溶液和E气体的△H为-46kJ•mol-1,
反应的热化学方程式为:②3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)△H=-138 kJ•mol-1,
则①×3+②×2得4NO(g)+3O2(g)+2H2O(1)=4HNO3 (aq),△H=3×(114kJ•mol-1)+2×(-138 kJ•mol-1)=-618kJ•mol-1,
故答案为:4NO(g)+3O2(g)+2H2O(1)=4HNO3 (aq)△H=-618kJ•mol-1.
点评 本题考查无机物的推断,属于开放性题目,需要学生熟练掌握元素化合物知识,题目难度中等.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 前者大 | B. | 前者小 | C. | 相等 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使溴的四氯化碳溶液褪色 | |
| B. | 与银氨溶液反应析出银 | |
| C. | 与新制Cu(OH)2反应 | |
| D. | 与乙醇在浓硫酸催化下发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,0.1 mol/L HF溶液中pH=1 | |
| B. | Ksp(CaF2)随温度和浓度的变化而变化 | |
| C. | 该体系中,Ksp(CaF2)=$\frac{1}{{K}_{a}HF}$ | |
| D. | 该体系中有CaF2沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
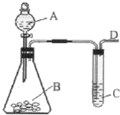 某同学用如图所示装置探究SO2的性质及其有关实验.
某同学用如图所示装置探究SO2的性质及其有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.08 mol/(L•s) | B. | 0.8 mol/(L•s) | C. | 1.6mol/(L•s) | D. | 2.4 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 咖啡酸(如图)存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别是对内脏的止血效果较好.下列关于咖啡酸的说法正确的是( )
咖啡酸(如图)存在于许多中药中,如野胡萝卜、光叶水苏、荞麦、木半夏等.咖啡酸有止血作用,特别是对内脏的止血效果较好.下列关于咖啡酸的说法正确的是( )| A. | 咖啡酸的分子式为C9H5O4 | |
| B. | 咖啡酸的某种同分异构体,其苯环上可能连有4个羟基 | |
| C. | 1 mol咖啡酸最多可以和2 mol NaOH反应 | |
| D. | 可以用高锰酸钾或溴水检验咖啡酸分子中所含的碳碳双键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com