
【题目】由熔盐电解法获得的粗铝含有一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝,工艺流程如下:
(已知:NaCl熔点为801℃;AlCl3在181℃升华;固体直接变为气体叫做升华)

(1)把NaCl和AlCl3的固体混合物置于下图所示的装置的一端,加热到_______(最低温度)℃,即可分离NaCl和AlCl3
![]()
(2)将Cl2连续通入坩埚中的粗铝熔体里,杂质随气泡上浮除去气泡的主要成分除Cl2外还含有_______;固态杂质黏附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在的物质是_______
(3)用废碱液处理气体A的过程中,所发生反应的离子方程式有:
①H++OH![]() H2O,
H2O,
②________
(4)镀铝电镀池中,金属铝为____极,熔融盐电镀池中存在Na+K+AlCl4-Al2Cl7-等离子钢材表面(电极)的电极反应式为AlCl4-+3e-![]() Al+4Cl-或_________
Al+4Cl-或_________
(5)钢材镀铝后,在表面氧化成致密的_____________,避免钢材接触空气而防止钢材被腐蚀
【答案】181 HCl、AlCl3 NaCl Cl2 + 2OH-== Cl- + ClO- + H2O 阳 Al2Cl7-+6e-=2Al +7Cl- 氧化铝膜
【解析】
(1)AlCl3在181℃升华,故加热到181℃,即可分离NaCl和AlCl3
(2)粗铝熔体里含有Na和H2,通Cl2后会生成NaCl和HCl,另外温度过高AlCl3易升华,因此气泡里还有HCl及AlCl3,固体浮渣中应该有NaCl。
(3)气体A的成份为HCl和Cl2,用NaOH吸收时发生反应的离子方程式是:
② Cl2 + 2OH-== Cl- + ClO- + H2O
(4)镀铝电镀池中,镀层金属作阳极,金属铝为阳极;待镀的钢材为阴极,表面(电极)的电极反应式:
Al2Cl7-+6e-="=2Al" +7Cl-
(5)铝能防腐就是表面能氧化生成致密的A12O3膜的缘故。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】以氮气和水蒸气为原料,电化学合成氨装置(电极不参与反应)示意图如下。下列说法不正确的是
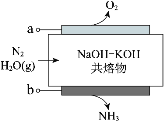
A.电极 a 连接电源的正极
B.OH向电极 a 迁移
C.总反应:2N2+6H2O(g)![]() 4NH3+3O2
4NH3+3O2
D.电极 b 的电极反应:N2+6e+6H+==2NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6 mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
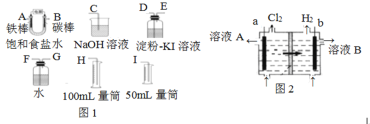
(1)试从上图图1中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接______,B接______。
(2)碳棒上发生的电极反应为_______。
(3)能说明氯气具有氧化性的实验现象是_______。
(4)假定装入的饱和食盐水为50 mL(电解前后溶液体积变化可忽略),当测得的氢气为5.6 mL(已折算成标准状况)时,溶液的pH为____。
(5)工业上采用离子交换膜法电解饱和食盐水,如上图图2,该离子交换膜是__(填“阳离子”或“阴离子”)交换膜,溶液A是_______(填溶质的化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化钪![]() 广泛应用在合金电光源,催化剂,激活剂等领域,下列流程图是用钪精矿生产氧化钪的方法之一:
广泛应用在合金电光源,催化剂,激活剂等领域,下列流程图是用钪精矿生产氧化钪的方法之一:![]() 钪精矿主要成分是钪的氧化物,硅铁等氧化物
钪精矿主要成分是钪的氧化物,硅铁等氧化物![]()

回答下列问题:
![]() 滤渣I是______
滤渣I是______![]() 填化学式
填化学式![]() 。在实验室里,操作Ⅰ必要的玻璃仪器有烧杯、______。
。在实验室里,操作Ⅰ必要的玻璃仪器有烧杯、______。
![]() 调pH的目的是______,如何检验含钪粗液中不含
调pH的目的是______,如何检验含钪粗液中不含![]() 离子______。
离子______。
![]() 写出制取草酸钪饼的化学方程式______。
写出制取草酸钪饼的化学方程式______。
![]() 写出草酸钪饼在空气中灼烧的化学方程式______,每生成
写出草酸钪饼在空气中灼烧的化学方程式______,每生成![]() ,转移的电子数为______。
,转移的电子数为______。
![]() 某工厂用
某工厂用![]() 的钪精矿制备纯氧化钪,得到纯产品
的钪精矿制备纯氧化钪,得到纯产品![]() ,则钪精矿中钪的质量分数是______
,则钪精矿中钪的质量分数是______![]() 假设Sc的利用率为
假设Sc的利用率为![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示(6s时反应已达到平衡状态),对该反应的推断正确的是( )

A.该反应的化学方程式为3B+4D6A+2C
B.反应进行到1s时,v(A)=v(C)
C.反应进行到6s时,B和D的物质的量浓度均为0.4molL﹣1
D.反应进行到6s时,B的平均反应速率为0.05mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式不正确的是
A. 次氯酸钙溶液中通入过量二氧化硫:Ca2+ + 2ClO-+ H2O + SO2=CaSO3↓+ 2HClO
B. 硫酸型酸雨放置一段时间溶液的pH下降:2H2SO3+O2=2H2SO4
C. 纯碱液可以清洗油污的原因:CO32+H2O![]() HCO3+OH
HCO3+OH
D. 向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72—+H2O![]() 2CrO42—+2H+
2CrO42—+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇广泛存在于食物(例如桑甚、花生,尤其是葡萄)中,它可能具有抗癌性。能够与1 mol该化合物发生反应的Br2和H2的最大用量分别是( )
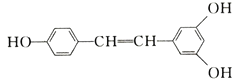
A.1mol、1molB.3.5mol、7mol
C.3.5mol、6molD.6mol、7mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解物质的量浓度相同、体积比为1∶3的 CuSO4和 NaCl的混合溶液,可能发生的反应有( )
①2Cu2++2H2O![]() 2Cu+4H++O2↑
2Cu+4H++O2↑
②Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
③2Cl-+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
④2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
A. ①②③B. ①②④C. ②③④D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法错误的是( )
A.1 L 0.1 mol·L-1 NH4Cl溶液中,NH4+的数目为0.1NA
B.质量均为1.7 g的OH-和—OH,所含质子数目均为0.9NA
C.1.0 mol Na2O2和1.0 mol Na2S混合后阴离子总数为2NA
D.60 g SiO2晶体中,含有SiO4四面体结构单元的数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com