
科目: 来源: 题型:选择题
| A. | 离子化合物中一定不含共价键,共价化合物中一定不含离子键 | |
| B. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| C. | 碳原子之间可形成碳碳单键、碳碳双键或碳碳叁键 | |
| D. | 分子间作用力越大,分子的热稳定性就越大 |
查看答案和解析>>
科目: 来源: 题型:解答题
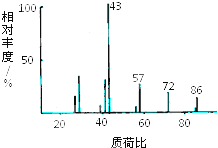 某有机物含有C、H、O三种元素,其质谱如图所示.将4.3g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7g,碱石灰增重8.8g,则:
某有机物含有C、H、O三种元素,其质谱如图所示.将4.3g该有机物在O2中充分燃烧,使生成物依次通过足量浓硫酸和碱石灰,浓硫酸增重2.7g,碱石灰增重8.8g,则:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH2O、C2H4O2、C6H12O6 | B. | CH2=CH2,C2H5OH、HOCH2CH2COOH | ||
| C. | C6H6O、C5H10、C7H6O2 | D. | H2、CO、CH3OH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ①③④ | C. | ③④ | D. | ①②③④ |
查看答案和解析>>
科目: 来源: 题型:解答题
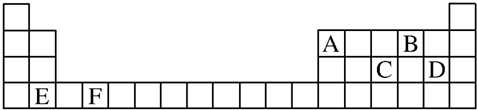
查看答案和解析>>
科目: 来源: 题型:解答题
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
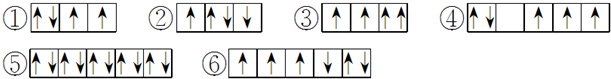
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 处于最低能量的原子叫做基态原子 | |
| B. | 3s2表示3s能级有两个轨道 | |
| C. | 同一原子中,1s、2s、3s电子的能量逐渐减小 | |
| D. | 同一原子中,3d、4d、5d能级的轨道数依次增多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com