
科目: 来源: 题型:填空题
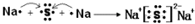 其所含化学键类型为离子键
其所含化学键类型为离子键 ,C与D形成的具有强氧化性的化合物的电子式为
,C与D形成的具有强氧化性的化合物的电子式为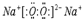

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 25℃101 kPa时,2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1此反应的反应热为221 kJ•mol-1 | |
| B. | 氢气的燃烧热为285.8 kJ•mol-1,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ•mol-1 | |
| C. | 已知2SO2(g)+O2(g)═2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 | |
| D. | 稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1稀硝酸与稀Ba(OH)2溶液反应的中和热为57.3 kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
 (1)实验室可用如图装置制取乙炔图中A管的作用是调节水面的高度来控制反应的发生和停止,制取乙炔的化学反应方程式为CaC2+2H2O→C2H2↑+Ca(OH)2
(1)实验室可用如图装置制取乙炔图中A管的作用是调节水面的高度来控制反应的发生和停止,制取乙炔的化学反应方程式为CaC2+2H2O→C2H2↑+Ca(OH)2查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH3CH2CH2CH2CH3 | B. |  | C. | 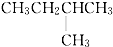 | D. | 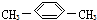 |
查看答案和解析>>
科目: 来源: 题型:解答题
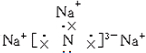 ,该化合物由离子键形成.
,该化合物由离子键形成.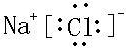 ,
, .
.查看答案和解析>>
科目: 来源: 题型:解答题
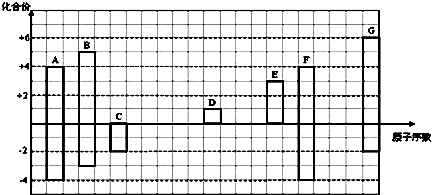
 分析图,回答以下问题:
分析图,回答以下问题:查看答案和解析>>
科目: 来源: 题型:解答题

 ;
;查看答案和解析>>
科目: 来源: 题型:解答题
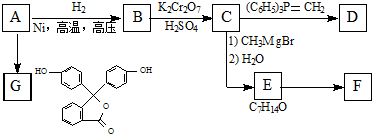
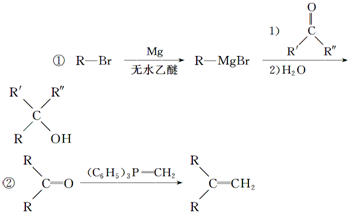 (R表示烃基,R和R表示烃基或氢)
(R表示烃基,R和R表示烃基或氢) .
.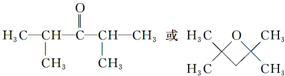 (任写一种).
(任写一种).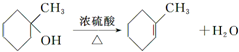 .
.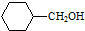 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2+CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C═CH2+CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 要提纯的物质 (少量杂质) | 溴乙烷 (乙醇) | 乙醇 (水) | 乙酸乙酯 (乙酸) | 苯 (苯酚) |
| (1)选用试剂 | ||||
| (2)分离方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com