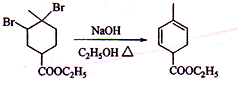
(2012?海南)(1)下列有关元素锗及其化合物的叙述中正确的是
BD
BD
A.锗的第一电离能高于碳而电负性低于碳
B.四氯化锗与四氯化碳分子都是四面体构型
C.二氧化锗与二氧化碳都是非极性的气体化合物
D.锗和碳都存在具有原子晶体结构的单质
(2)铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.回答下列问题:
①铜原子基态电子排布式为
1s22s22p63s23p63d104s1
1s22s22p63s23p63d104s1
;
②用晶体的x射线衍射法可以测得阿伏加德罗常数.对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm.又知铜的密度为9.00g?cm
-3,则镉晶胞的体积是
4.7×10-23
4.7×10-23
cm
3、晶胞的质量是
4.23×10-22
4.23×10-22
g,阿伏加德罗常数为
6.01×1023mol-1
6.01×1023mol-1
(列式计算,己知Ar(Cu)=63.6);
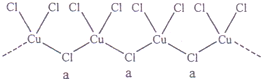
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为
sp3
sp3
.已知其中一种化合物的化学式为KCuCl
3,另一种的化学式为
K2CuCl3
K2CuCl3
;
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
过氧化氢为氧化剂,氨与Cu2+形成配离子,两者相互促进使反应进行
过氧化氢为氧化剂,氨与Cu2+形成配离子,两者相互促进使反应进行
,反应的化学方应程式为
Cu+H2O2 +4NH3=Cu(NH3)42++2OH-
Cu+H2O2 +4NH3=Cu(NH3)42++2OH-
.