
科目: 来源: 题型:填空题
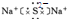 .
. 查看答案和解析>>
科目: 来源: 题型:填空题
| 性质 | 试剂 | 化学方程式 |
| 漂白性 | ||
| 氧化性 | ||
| 还原性 | ||
| 酸性氧化物 |
查看答案和解析>>
科目: 来源: 题型:填空题
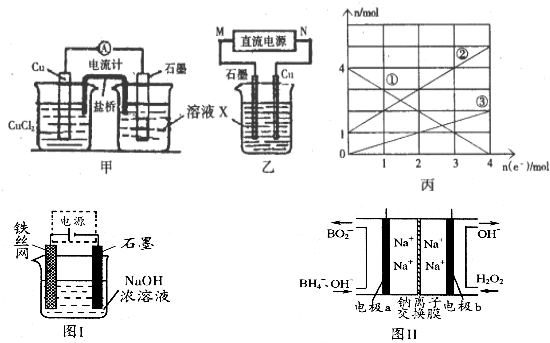
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 转移的电子数是1.204×1022 | B. | 阳极上产生112 mL O2(标准状况) | ||
| C. | 溶液的浓度变化为0.08 mol•L-1 | D. | 反应中有0.01 mol Ag被氧化 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 X、Y、Z、Q、W、N核电荷数依次增大的六种元素中,Y原子核外的L层电子数是K层的两倍,Q原子核外的L层中只有两个未成对电子,X与Y、Q可以以原子个数2:1或1:1形成化合物.W与Q同主族,元素N的第三能层共有5对成对电子.请回答下列问题:
X、Y、Z、Q、W、N核电荷数依次增大的六种元素中,Y原子核外的L层电子数是K层的两倍,Q原子核外的L层中只有两个未成对电子,X与Y、Q可以以原子个数2:1或1:1形成化合物.W与Q同主族,元素N的第三能层共有5对成对电子.请回答下列问题: ;
;查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 283.5kJ/mol | B. | 172.5kJ/mol | C. | -172.5kJ/mol | D. | -504 kJ/mol |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com