
科目: 来源: 题型:
| 卤代烃或醇 | 相应产物及其产率 |
 |
  81% 19% |
 |
  80% 20% |
 |
  80% 20% |
 |
  90% 10% |





查看答案和解析>>
科目: 来源: 题型:
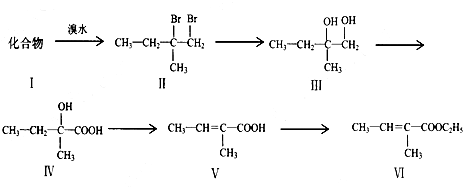
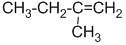
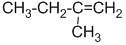
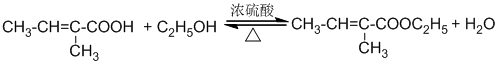

查看答案和解析>>
科目: 来源: 题型:阅读理解
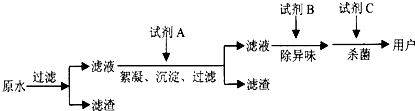
查看答案和解析>>
科目: 来源: 题型:阅读理解
查看答案和解析>>
科目: 来源: 题型:
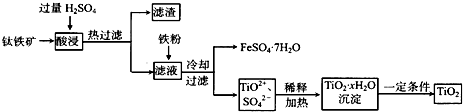
| ||
查看答案和解析>>
科目: 来源: 题型:
| ||
| 实验操作 | 预期现象和结论 |
| 步骤1: | 粉末减少,说明粉末国可能含有Al2O3 粉末减少,说明粉末国可能含有Al2O3 |
| 步骤2: | 有白色沉淀产生然后沉淀又溶解,说明粉末中含有Al2O3 有白色沉淀产生然后沉淀又溶解,说明粉末中含有Al2O3 |
| 步骤3: | 有红色固体生成,说明粉末中含有Fe 有红色固体生成,说明粉末中含有Fe |
| 步骤4: | 固体部分溶解,溶液变血红色,说明粉末中含有Fe2O3 固体部分溶解,溶液变血红色,说明粉末中含有Fe2O3 |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 组别 | C(NaOH)/mol?L-1 | 时间/min | ||||||||
| 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| 1 | 0.5 | 10.0 | 9.0 | 8.0 | 7.5 | 7.0 | 6.5 | 6.5 | 6.5 | 6.5 |
| 2 | 1.0 | 10.0 | 8.5 | 7.0 | 6.0 | 5.0 | 4.5 | 4.5 | 4.5 | 4.5 |
| 3 | 2.0 | 10.0 | 8.0 | 6.0 | 4.5 | 3.0 | 2.0 | 1.5 | 1.5 | 1.5 |
查看答案和解析>>
科目: 来源: 题型:
| ||

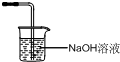

查看答案和解析>>
科目: 来源: 题型:
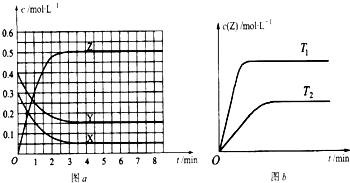 (2009?广州二模)已知可逆反应X(g)+Y(g)?Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是( )
(2009?广州二模)已知可逆反应X(g)+Y(g)?Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是( )查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com