
科目: 来源: 题型:
【题目】Cu及其化合物在科学研究和工业生产中具有许多用途。请回答以下问题:
(1)向CuSO4浓溶液中滴加氨水至深蓝色的透明溶液.再向其中加入适量乙醇,发生的离子反应方程式__________________________;
(2)硫酸铜溶液中滴入氨基乙酸钠(H2N—CH2COONa)即可得到配合物A,其结构如图:
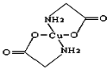
①SO42-中S原子的轨道杂化类型是________________;
②A中碳原子的轨道杂化类型为________________;
③1mol氨基乙酸钠含有δ键的数目为_________。
(3)元素金(Au)处于周期表中的第六周期,与Cu同族。一种铜合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,该合金中每一层均为_________(填“密置层”、“非密置层”);该晶体中,原子之间的作用力是_________。
(4)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的晶胞结构结构相似,该晶体储氢后的化学式应为_________,若Cu原子与Au原子的距离为acm,则该晶体储氢后的密度为_________。(含a的表达式)
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸。请填写以下空白。

(1)A、B、C、D的化学式分别是___________、___________、___________、___________。
(2)A→B的化学方程式是________________________________________________________。
(3)C→D的离子方程式是________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁、戊是由四种短周期元素中的两种或三种组成的5种化合物,其中乙、丙、戊均由两种元素组成,丙是导致温室效应的主要气体,戊是天然气的主要成分,乙和丁都既能与酸反应,又能与强碱溶液反应。上述5种化合物涉及的四种元素的原子序数之和等于28;甲由一种金属元素和两种非金属元素组成,其原子个数比为1︰3︰9,所含原子总数等于其组成中金属元素的原子序数。它们之间的反应关系如下图:

请回答下列问题:
(1)物质甲的化学式是 ,写出乙的一种用途是 。
(2)甲与足量H2O溶液反应的化学方程式 。
(3)将过量的丙通入某种物质的水溶液中可以生成丁,该反应的离子方程式为 。
(4)乙溶于某强碱溶液的离子方程式为 。
(5)在200 mL 1.5 mol·L-1NaOH溶液中通入标准状况下4.48 L 丙气体,完全反应后所得溶液中,各种离子浓度由大到小的顺序是 。
(6)丁是一种难溶物质,其溶度积常数为1.25×10-33。将0.01 mol 丁投入1 L某浓度的盐酸中,为使丁完全溶解得到澄清透明溶液,则盐酸的浓度至少应为 (体积变化忽略不计,结果保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是由4个碳原子结合成的6种有机物(氢原子没有画出)。


(1)写出有机物(a)的系统命名法的名称__________。
(2)有机物(a)有一种同分异构体,试写出其结构简式__________。
(3)上述有机物中与(c)互为同分异构体的是__________ (填代号).
(4)任写一种与(e)互为同系物的有机物的结构简式__________。
(5)上述有机物中不能与溴水反应但能使其褪色的有__________(填代号)。
(6) (a) (b) (c)三种物质中,4个碳原子一定处于同一平面的有________ (填代号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫以及铁的化合物。
Ⅰ.近年来,湿法炼铜有了新进展,某工厂以一种叫Thibacillus ferroxidans的细菌为基体生产铜和绿矾的工艺流程如下:

(1)试剂a为________,试剂b为_______(写名称)。
(2)反应1的化学方程式为 。
Ⅱ.以CuFeS2精矿为原料在沸腾炉中和O2(空气)反应,生成物冷却后经溶解、除铁、结晶,得到CuSO4·5H2O。沸腾炉的温度与生成物主要成分的水溶性和酸溶性实验结果如图。

(3)沸腾炉生成物中的含铁物质主要成分为___________。
(4)为获得最高的水溶性Cu(%),沸腾炉的温度应控制在______ ℃左右,高于该温度生成物中的水溶性Cu(%)下降,可能原因是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】由N、B等元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造,由第二周期元素组成的与BCl3互为等电子体的阴离子为_________(填离子符号,填一个)。
(2)氮硼烷化合物(H2N→BH2)和Ti(BH4)3均为广受关注的新型化学氮化物储氢材料。
①H2N→BH2中N原子的杂化类型为_________;
②Ti(BH4)3由TiCl3和LiBH4反应制得。基态Ti3+的未成对电子数有____个,BH4-的立体构型是_________;写出该制备反应的化学方程式_________;
③氮硼烷可由六元环状化合物(HB=NH)3通过如下所对应制得:
3CH4+2(HB=NH)3+6H2O═3CO2+6H3BNH3与上述化学方程式有关的叙述不正确的是_________;.(填标号)
A.氮硼烷中存在配位键
B.第一电离能:N>O>C>B
C.反应前后碳原子的轨道杂化类型不变
D.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
(3)磷化硼(BP)是受到高度关注的耐麿材料;如图1为磷化硼晶胞。
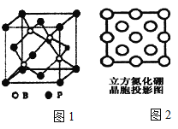
①磷化硼晶体属于________晶体(填晶体类型),________(填是或否)含有配位键。
②晶体中B原子的配位数为_______。
(4)立方氮化硼是一种新型的超硬、耐麿、耐高温的结构材料,其结构和硬度都与金刚石相似,但熔点比金刚石低,原因是________。图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和画“×”分别标明B与N的相对位置。
查看答案和解析>>
科目: 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)H3PO2是一元中强酸,写出其电离方程式_______________________。
(2)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为___________(填化学式);
②NaH2PO2为___________(填“正盐”或“酸式盐”)。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________。
(4)H3PO2也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):

①写出阳极的电极反应式_________________ ___________________;
②分析产品室可得到H3PO2的原因__________________ _________________;
③早期采用“三室电渗析法”制备H3PO2:将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中混有 杂质,该杂质产生的原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】右下表为元素周期表的一部分。X、Y、Z、W为短周期元素,其中X元素的原子最外层电子数是其内层电子数的2倍。下列说法正确的是()

A. 根据元素周期律,可以推测存在T3Y4、TZ2和TW4
B. X氢化物的沸点一定比Y氢化物的沸点高
C. XZ2、XW4与YW3都是非极性分子
D. W的氧化物的水化物酸性一定比Z的强
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用浓硫酸和乙醇制取乙烯时,常会看到烧瓶中液体变黑,制得的乙烯中混有CO2、SO2等杂质。某课外小组设计了如下装置,证明乙烯中混有CO2、SO2并验证乙烯的性质。
回答下列问题:

(1)装置A是乙烯的发生装置。图中一处明显的错误是__________,烧瓶中碎瓷片的作用是__________。
(2)若要检验A中所得气体含有SO2,可将混合合气体直接通入__________(填代号,下同)装置;若要检验,A中所得气体含有CH2=CH2,可将混合气体先通入B装置,然后通入__________装置。
(3)写出实验室制取乙烯的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知咖啡酸的结构如图所示。关于咖啡酸的描述正确的是()

A.与该芳香族化合物分子式相同、官能团种类及数目均相同且苯环上的一氯代物只有两种的有机物的结构有4种(不考虑空间异构)
B.咖啡酸只能加聚成高分子化合物
C.咖啡酸最多可与5mol氢气发生加成反应
D.1mol该物质与足量的Na2CO3溶液反应,能消耗3 mol CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com