
科目: 来源: 题型:
【题目】3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成。一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃) / g·cm-3 | 溶解性 |
甲醇 | 64. 7 |
| 0. 7915 | 易溶于水 |
乙醚 | 34. 5 |
| 0. 7138 | 微溶于水 |
3,5-二甲氧基苯酚 |
| 33-36 |
| 易溶于甲醇、乙醚,微溶于水 |
反应结束后,先分离出甲醇,再加入乙醚进行萃取。
(1)①分离出甲醇的操作是的 。
②萃取用到的分液漏斗使用前需 并洗净,分液时有机层在分液漏斗的 填(“上”或“下”)层。
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤。用饱和NaHCO3 溶液洗涤的目的是 ;用饱和食盐水洗涤的目的是 。
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是 (填字母)。
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为________________。

(2)以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2molL﹣1的KOH溶液,电池总反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为 ;每消耗3.4g NH3转移的电子数目为_________。
(3)用NH3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L。

查看答案和解析>>
科目: 来源: 题型:
【题目】Cyrneine A对治疗神经系统疾病有着很好的疗效。可用香芹酮经过多步反应合成:
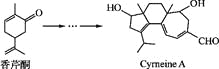
下列说法不正确的是( )
A. 香芹酮的分子式为C10H14O
B. Cyrneine A可以发生加成反应、消去反应和氧化反应
C. 香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色
D. 与香芹酮互为同分异构体,分子中有4种不同化学环境的氢原子的酚类化合物共有3种
查看答案和解析>>
科目: 来源: 题型:
【题目】己二酸 是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
![]()

可能用到的有关数据如下:

实验步骤如下:
I、在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
II、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
III、当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
IV、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
V、粗产品经提纯后称重为5.7g。
请回答下列问题:
(1) 仪器b的名称为__________。
(2) 向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则.可能造成较严重的后果,试列举一条可能产生的后果:____________________。
(3) 已知用NaOH溶液吸收尾气时发生的相关反应方程式为:
2NO2+2NaOH=NaNO2+NaNO3+H2O 、NO+NO2+2NaOH =2NaNO2+H2O ;如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为:____________ _________、___________________。
(4)为了除去可能的杂质和减少产品损失,可分别用冰水和 洗涤晶体。
(5)粗产品可用 法提纯(填实验操作名称)。本实验所得到的己二酸产率为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】DDT又叫滴滴涕,化学名为双对氯苯基三氯乙烷,化学式(ClC6H4)2CH(CCl3)。名称从英文缩写DDT而来,为白色晶体,不溶于水,溶于煤油,可制成乳剂,是有效的杀虫剂。DDT进入食物链,是导致一些食肉和食鱼的鸟接近灭绝的主要原因。因此从70年代后滴滴涕逐渐被世界各国明令禁止生产和使用。其结构为: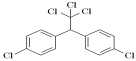 ,下列有关说法正确的是 ( )
,下列有关说法正确的是 ( )
(手性碳原子为饱和碳原子所连的4个原子或原子团不同)
A.属于烃类 B.DDT完全燃烧后只产生CO2和H2O两种物质
C.分子无手性碳 D.氢核磁共振谱图中有5种位置峰
查看答案和解析>>
科目: 来源: 题型:
【题目】将甲烷设计成燃料电池,其利用率更高,如图所示(A, B为多孔性碳棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL,则下列说法错误的是()

A.通入CH4的一端为原电池的负极,溶液中OH-向负极区移动
B.当0<V ≤22.4L时,电池总反应式为CH4+2O2+2KOH=K2CO3+3H2O
C.当22.4L<V≤44.8L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-
D.当V=33.6L时,溶液中阴离子浓度大小关系为c(CO32-)>c(HCO3-)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如表:
元素编号 | 元素特征信息 |
A | 最高正价和最低负价的绝对值之差为2 |
B | 和E同主族 |
C | lmo1C单质能与冷水反应,在标准状况下生成11.2LH2 |
D | 原子最外层电子数等于其周期序数 |
E | 负一价阴离子的电子层结构与Ar原子相同 |
(1) A在周期表中的位置为 。
(2)B和C形成的化合物的电子式为 。
(3)B和D简单离子的半径大小为 。
(4)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中不可行的是 (填序号)。
A.比较两种单质的颜色
B.比较两种单质与H2化合的难易程度
C.依据两元素在周期表中的位置
D.比较对应阴离子的还原性
e.比较最高价氧化物对应水化物的酸性
(5)E元素能与另外四种元素中的一种元素形成共价化合物,分子中的原子个数比为1∶3,相对分子质量为120.5,则该物质的化学式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】【加试题】硝酸铝[Al(NO3)3]是一种常用媒染剂。工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3·9H2O]的流程如下:

(1)写出反应Ⅰ的离子方程式: (任写一个)。
(2)若在实验室中完成反应Ⅱ,为避免铝的损失,需要解决的问题是 ,可采取的措施为 。
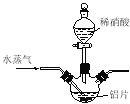
(3)温度高于200℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4:1),该反应的化学方程式是 。
(4)若用右图所示实验装置制取Al(NO3)3,通入水蒸气的作用是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】肉桂酸异戊酯G(![]() )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下:

已知以下信息:
①![]() ;
;
②C为甲醛的同系物,相同条件下其蒸气与氢气的密度比为22。
回答下列问题:
(1)A的化学名称为 。
(2)B和C反应生成D的化学方程式为 。
(3)F中含有官能团的名称为 。
(4)E和F反应生成G的化学方程式为 ,反应类型为 。
(5)F的同分异构体中不能与金属钠反应生成氢气的共有 种(不考虑立体异构),其中核磁共振氢谱只有两组峰,且峰面积比为3:1的为 (写结构简式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾天气肆虐给人类健康带来了严重影响。燃煤和汽车尾气 是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)![]() 2C02(g)+N2 (g) △H <0 。
2C02(g)+N2 (g) △H <0 。
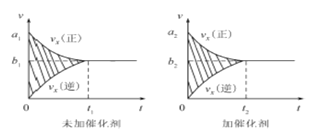
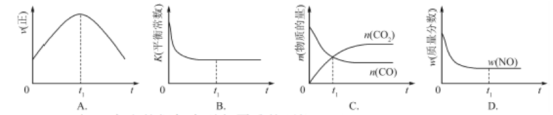
①该反应的速率时间图像如右图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,则其速率时间图像如右图中右图所示。以下说法正确的是 (填对应字母)。
A.a1>a2 B.b1 <b2 C.t1>t2
D.右图中阴影部分面积更大 E.左图中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。已知:CH4(g)+2N02(g) = N2(g)+C02(g)+2H20(g) △H=-867 kJ/mol
2N02(g)= N204(g) △H= - 56.9 kJ/mol H20(g) = H20(l) △H = - 44.0 kJ/mol
写出CH4催化还原N204 (g)生成N2和H20(1)的热化学方程式: 。
(3)CH4和H20(g)在催化剂表面发生反应CH4 + H20 = C0 + 3H2 ,该反应在不同温度下的化学平衡常数如下表:
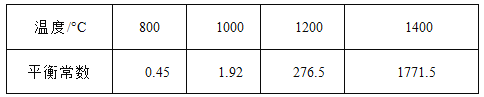
①该反应是 反应(填“吸热”或“放热 ”)。
②T℃时,向1L密闭容器中投入1mol CH4 和1mol H20(g),平衡时C(CH4)=0.5 mol·L-1 , 该温度下反应CH4 + H20 = CO+3H2的平衡常数K= 。
(4)甲烷燃料电池可以提升能量利用率。如图是利用甲烷燃料电池电解100mL lmol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24 L(设电解后溶液体积不变)。
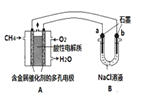
①甲烷燃料电池的负极反应式: 。
②电解后溶液的pH = , (忽略氯气与氢氧化钠溶液反应)。
③阳极产生气体的体积在标准状况下是 L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com