
科目: 来源: 题型:
【题目】已知25℃ Ksp(Ag2S)=6.3×10-50、Ksp(AgCl)=1.5×10-16。沙市中学某研究性学习小组探究
AgCl、Ag2S沉淀转化的原因。
步 骤 | 现 象 |
Ⅰ.将NaCl与AgNO3溶液混合 | 产生白色沉淀 |
Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
Ⅲ.滤出黑色沉淀,加入NaCl溶液 | 较长时间后,沉淀变为乳白色 |
(1)Ⅰ中的白色沉淀是 。
(2)Ⅱ中能说明沉淀变黑的的离子方程式是 ,沉淀转化的主要原因是 。
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl。用浓HNO3溶解,产生红棕色气体,部分沉淀未溶
解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y中滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是 。
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀_____ _。
(4)该学生通过如下对照实验确认了步骤Ⅲ中 乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化。

现 象 | B:一段时间后,出现乳白色沉淀 |
C:一段时间后,无明显变化 |
①A中产生的气体是_________。
②C中盛放的物质W是_________。
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S + ![]() +
+ ![]() + 2H2O
+ 2H2O ![]() 4AgCl +
4AgCl + ![]() + 4NaOH
+ 4NaOH
④从平衡移动的角度,解释B中NaCl的作用: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.下列实验方案合理的是________。
A.在检验醛基配制银氨溶液时,在一定量氨水中,加入AgNO3溶液
B.在检验醛基配制Cu(OH)2悬浊液时,在一定量NaOH溶液中,滴加入少量CuSO4溶液
C.验证RX为碘代烃时,把RX与烧碱水溶液混合加热,将溶液冷却后直接加入硝酸银溶液
D.用电石与饱和食盐水反应时,将制得的气体先通入NaOH溶液,再通入酸性高锰酸钾溶液,可检验制得的气体是否为乙炔
E.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
F.除去混在苯中的少量苯酚,加入过量溴水,过滤
G.实验室制取乙烯时必须将温度计的水银球插入反应液中,测定反应液的温度
II.现有通式为(CH2O)n的五种有机物,性质如下:
① 甲是无色有刺激性气味的气体,可以发生银镜反应;
② 乙、丙、丁的相对分子质量均为甲的2倍,戊的相对分子质量是甲的3倍;
③ 乙、戊的水溶液均可使紫色石蕊试液变红,还可以与乙醇在一定条件下酯化,且两分子戊可以形成六元环酯;
④ 丙既能水解,又能发生银镜反应;丁既能与钠反应放出H2,又能与新制Cu(OH)2悬浊液加热反应产生红色沉淀。
(1) 推断各物质的结构,写出其结构简式。
甲_________ ,乙_________ ,丙_________ ,丁_________ ,戊_________ 。
(2) 等物质的量的戊,分别与足量Na反应产生的气体和与足量NaHCO3反应产生的气体体积之比是______________( 在相同条件下测定)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示几种无机物之间的转换关系。其中A、B均为黑色粉末,B为非金属单质,C为无色无毒气体,D为金属单质,E是红棕色气体,G是具有漂白性的气体,H的水溶液呈蓝色。

请回答下列问题:
(1)A的化学式是 ,C的电子式是 ,Y的名称是 。
(2)反应1的化学方程式为 。
(3)19.2g的D与足量的一定浓度X的溶液反应,将所得到的气体与 LO2(标准状况下)混合,恰好能被水完全吸收。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,甲醚可作燃料电池的燃料。
(1)甲醚(CH3OCH3)与 (填结构简式)互为同分异构体。
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)![]() CH3OCH3(g)+3H2O(g),反应放热。
CH3OCH3(g)+3H2O(g),反应放热。
I.一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应到达化学平衡状态的是 (选填编号,注意大小写)
a. c(H2)与c(H2O)的比值保持不变
b. 单位时间内有2molH2消耗时有1molH2O生成
c. 容器中气体密度不再改变
d. 容器中气体压强不再改变
II.温度升高,该化学平衡逆向移动后到达新平衡,混合气体的平均相对分子质量将 (填“变大”、“变小”或“不变”)
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,该燃料电池的负极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(普通)醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:

可能用到的有关数据如下:

合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置a的名称是 。
(2)加入碎瓷片的作用是 ;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是 (填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并 ;在本实验分离过程中,产物应该从分液漏斗的 (填“上口倒出”或“下口放出”)。
(4)分离提纯过程中加入无水氯化钙的目的是 。
(5)在环己烯粗产物蒸馏过程中,可能用到的仪器有 (填正确答案标号)。
A圆底烧瓶 B温度计 C漏斗 D玻璃棒 E接收器
(6)本实验中最容易产生的副产物的结构简式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA 为阿伏加德罗常数的值。下列说法正确的是
A.0.1mol的白磷(P4)或CCl4中所含的共价键数均为0.4NA
B.S2和S8的混合物共6.4g,其中所含的电子数一定为3.2NA
C.5.4gAl分别于含溶质0.2mol的NaOH溶液、盐酸反应,生成H2分子数均为0.3NA
D.在H2O2+Cl2=2HCl+O2反应中,每生成32gO2,转移4 NA个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】手持技术的氧电化学传感器可用于测定O2含量.下图为某种氧电化学传感器的原理示意图,已知在测定O2含量过程中,电解质溶液的质量保持不变。一定时间内,若通过传感器的待测气体为a L(标准准状况),某电极增重了bg。下列说法正确的是

A. Pt上发生氧化反应 B. Pb上的电极反应式为4OH--4e-=O2↑+2H2O
C. 反应过程中转移OH-的物质的量为0.25bmol D. 待测气体中氧气的体积分数为0.7b/a
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:

(1)写出A、B、C、D的结构简式:
A________,B________,C________,D________。
(2)写出、、、④四步反应的化学方程式,并注明反应类型
____________________,反应类型________。
____________________,反应类型________。
____________________,反应类型________。
④____________________,反应类型________。
(4)烃A的燃烧反应方程式___________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物的反应往往伴随副反应发生,因此 需要分离提纯。有一种水果香精的合成步骤如下:
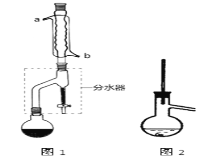
Ⅰ合成:
在干燥的圆底烧瓶中加入11.5 mL(9.3 g,0.125 mol)正丁醇、7.2 mL(7.5 g,0.125 mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00 mL水,其水面低于分水器回流支管下沿3~5 mm,然后用小火加热,反应大约40 min。
Ⅱ分离提纯:
① 将烧瓶中反应后的混合物冷却后与分水器中的酯层合并,转入分液漏斗,依次用10 mL水、10 mL 10% 碳酸钠溶液洗至中性,充分振荡后静置,分去水层。
② 将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥。
③ 将乙酸正丁酯粗产品转入50 mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。
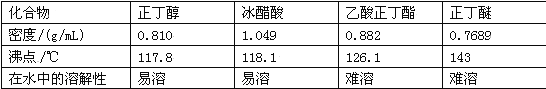
主要试剂及产物的物理常数如下:
制备过程中还可能有的副反应:
2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
(1)合成和分离过程中均使用沸石,其作用________________________ 。
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从______(填a或b)管口通入。
(3)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先_______(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中,如果蒸馏装置如图2所示,则收集到的产品中可能混有___________杂质。
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃)
C.沙子 D.石蜡油(沸点200~300℃)
(5)如何根据装置中的实验现象判断该合成反应达到了终点_______________ 。
(6)反应结束后,若放出的水为6.98 mL(水的密度为1g/mL),则正丁醇的利用率约为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(I)有机物M(分子式:C6H4S4)是隐形飞机上吸波材料的主要成分。某化学兴趣小组为验证其组成元素,进行了如下实验:将少量样品放入A的燃烧管中,通入足量O2,用电炉加热使其充分燃烧,并将燃烧产物依次通入余下装置。(右图中的夹持仪器的装置已略去)
(1)装置B的目的是验证有机物中含氢元素,则B中盛装的试剂名称为 ________;
(2)能证明有机物含碳元素的现象是__________;
(3)指出装置F中的错误: ________。
(II)苯甲酸的重结晶实验基本操作如下:①将粗苯甲酸1g加到100mL的烧杯中,再加入50mL蒸馏水,在石棉网上边搅拌边加热,使粗苯甲酸溶解,②全溶后再加入少量蒸馏水并搅拌.③然后,使用短颈玻璃漏斗趁热将溶液过滤到另一100mL烧杯中,将滤液静置,使其缓慢冷却结晶.④滤出晶体。
回答下列问题:
(1)上述四步操作过程中需用到玻璃棒的步骤有____________;
(2)步骤②的目的是____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com