
科目: 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种新型能源,利用二氧化碳合成新能源已成为环保化学家研究的热门课题。
(1)几种共价键的键能如表所示:
化学键 | C=O | H-H | C-H | C-O | H-O |
键能/kJ·mol-1 | 803 | 436 | 414 | 326 | 464 |
2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ![]() _______________。
_______________。
(2)“人工光合作用”技术备受瞩目,该技术模拟事物的光合作用,利用太阳光将H2O和CO2直接合成燃料和化工原料。科研人员模拟光合作用,设计如图甲所示装置制备二甲醚。能量转化形式为太阳能![]() 电能
电能![]() 化学能、
化学能、
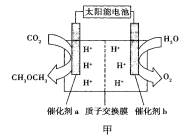
①催化剂b的电极名称是_________________。
②若释放11.2L氧气(标准状况下),有___________mol H+___________(填质子的迁移方向)。
③催化剂a上的电极反应式为______________。
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图乙所示:
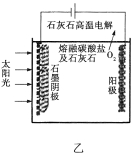
①生产过程中能量的转化形式是__________________。
②电解反应在温度小于900![]() 时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为_______________,阴极的电极反应式为______________。
时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为_______________,阴极的电极反应式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,该条件下向100 mL的CaSO4饱和溶液中,加入400 mL 0.01 mol·L-1的Na2SO4溶液,针对此过程的下列叙述正确的是(忽略混合过程中的体积变化)
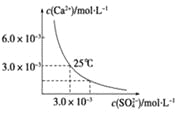
A. 溶液中析出CaSO4沉淀,最终溶液中c(SO42-)较原来大
B. 溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C. 溶液中析出CaSO4沉淀,溶液中c(Ca2+)、c(SO 42-)都变小
D. 溶液中无沉淀析出,但最终溶液中c(SO42-)较原来大
查看答案和解析>>
科目: 来源: 题型:
【题目】四苯基乙烯(TPE)及其衍生物具有聚集诱导发光特性,在光电材料等领域应用前景广阔。以下是TPE的两条合成路线(部分试剂和反应条件省略):
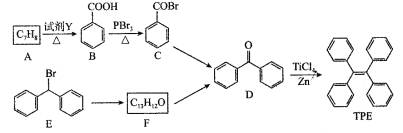
(1)A的名称是___________。
(2)B![]() C的反应类型是____________; D中官能团的名称是_____________。
C的反应类型是____________; D中官能团的名称是_____________。
(3)E![]() F的化学方程式是____________。
F的化学方程式是____________。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(![]() )的一元取代物;②存在羟甲基(—CH2OH)。写出W所有可能的结构简式_____________。
)的一元取代物;②存在羟甲基(—CH2OH)。写出W所有可能的结构简式_____________。
(5)下列说法正确的是__________
a.B的酸性比苯酚强
b.D不能发生还原反应
c.E含有3种不同化学环境的氢
d.TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目: 来源: 题型:
【题目】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图:
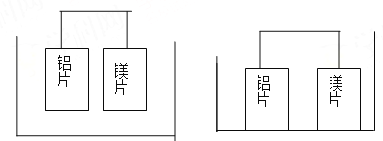
甲(H2SO4溶液) 乙(NaOH溶液)
(1)写出甲池中正极的电极反应式: ,负极的电极反应式: 。
(2)写出乙池中负极的电极反应式: ,乙池中总反应的离子方程式: 。
(3)如果甲和乙同学均认为,“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出 活动性更强。
(5)丙同学依据甲、乙同学的思路,设计如下实验:将铝片和铜片用导线相连.一组插入浓硝酸中,一组插入稀NaOH溶液中,分别形成了原电池。
①在这两个原电池中,负极分别为________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
②写出插入浓硝酸中形成原电池的总反应化学方程式__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)基态钛原子的价电子排布图为
(2)已知TiCl4在通常情况下是无色液体,熔点为﹣37℃ ,沸点为136℃ ,可知TiCl4为 晶体.
(3)硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示。该阳离子Ti与O的原子数之比为 。
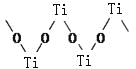
(4)Co的一种氧化物的晶胞如图所示,在该晶体中与一个钴原子等距离且最近的钴原子有 个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成是 。


(5)由C、Mg、Ni三种元素组成的一种简单立方结构的化合物具有超导性,其晶胞中C位于体心位置,Mg位于顶角,Ni占据面心位置,该化合物的化学式为 ,晶体中Mg原子周围距离最近的Ni原子有 个,该新型超导材料晶胞参数a=0.38nm,计算该晶体的密度 (gcm﹣3)(保留三位有效数字)
(6)金属钛晶胞结构如图所示,设钛原子的半径为r,则该晶胞体积的表达式为

查看答案和解析>>
科目: 来源: 题型:
【题目】根据化学反应中的能量变化关系回答下列问题:
(1)断开1molH-H键,1molN-H键,1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,求:
①1molN2生成NH3需______(填“吸收”或“放出”)能量______kJ;
②1molH2生成NH3需______(填“吸收”或“放出”)能量______kJ。
(2)航天飞船可用肼(N2H4)作动力源。已知1mol液态肼和足量的液态过氧化氢反应生成氮气和水蒸气时放出641.6kJ热量,化学方程式如下:N2H4+2H2O2===N2↑+4H2O。
①该反应中肼作 (填氧化或还原)剂;
②该反应的反应物总能量 (填高于或低于)生成物的总能量;
③此情况下,液态肼燃烧生成0.5molN2时放出的热量为 kJ;
④肼(N2H4)分子中存在的化学键有 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某优质甜樱桃中含有一种羟基酸(用M表示),M的碳链结构无支链,分子式为C4H6O5;1.34 g M与足量的碳酸氢钠溶液反应,生成标准状况下的气体0.448 L。M在一定条件下可发生如下转化:M![]() A
A![]() B
B![]() C(M、A、B、C分子中碳原子数目相同)。下列有关说法中不正确的是( )
C(M、A、B、C分子中碳原子数目相同)。下列有关说法中不正确的是( )
A. M的结构简式为HOOC—CHOH—CH2—COOH
B. B的分子式为C4H4O4Br2
C. 与M的官能团种类、数量完全相同的同分异构体还有1种
D. C物质不可能溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B═H++HB-;HB-![]() H++B2-,回答下列问题:
H++B2-,回答下列问题:
(1)NaHB溶液显___________(填“酸性”、“中性”或“碱性”或“酸碱性无法确定”),理由是___________。
(2)某温度下,向0.1mol/L的NaHB溶液中滴入0.1mol/LKOH溶液至中性,此时溶液中以下关系一定正确的是___________(填字母).
A.c(H+)c(OH-)═1×10-14 mol2/L2
B.c(Na+)+c(K+)═c(HB-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)═0.05mol/L
(3)已知常温下H2B的钙盐(CaB)饱和溶液中存在以下平衡:CaB(s) ![]() Ca2+(aq)+B2-(aq)△H>0.
Ca2+(aq)+B2-(aq)△H>0.
①温度升高时,Ksp ___________(填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+)___________,原因是___________(用文字和离子方程式说明)。
(4) 已知0.1molL-1NaHB溶液的pH=2,则0.1molL-1H2B溶液中氢离子的物质的量浓度可能是___________0.11molL-1(填“<”、“>”、或“=”); 理由是___________。
(5)0.1 mol/L NaHB溶液中各种离子浓度由大到小的顺序是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铜、氯化亚铜是重要的化工原料,广泛用作有机合催化剂。
已知:氯化铜容易潮解.

I.实验室用如图所示装置,用还原铜粉和氯气来制备氯化铜。
(1)石棉绒的作用是 ;B装置中的试剂是 。E和F装置及试剂可用_______ 替换(填装置及所装试剂)。
(2)当Cl2排尽空气后,加热D。则D中发生反应的化学方程式为 。
(3) 若实验测得CuCl2质量分数为90.0%,则其中可能含有的杂质是 (一种即可)。
Ⅱ.另取纯净CuC l2固体用于制备CuCl。

(4)溶解时加入HCl溶液的目的主要是 (结合离子方程式回答)。
(5)若接上述操作用10. 0mol/L的HCl代替0.2mol/L HCl,通人SO2后,200. 00mL黄绿色溶液颜色褪去,但无白色沉淀。对此现象:
甲同学提出假设:c(H+)过大。
为验证此假设,可取75.00g CuCl2固体与100mL0.2mol/LHCl及 mL9. 8mol/LH2SO4配制成200. 00mL溶液再按上述操作进行实验。
乙同学查阅资料:体系中存在平衡2Cl-(aq)+CuCl(s)=CuCl32-(aq)。则出现此现象另一可能的原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在酸式介质中,负极反应的物质为 ,正极反应的物质为 ,酸式电池的电极反应:
负极: ,正极: 。
电解质溶液pH的变化 (填“变大”,“变小”,“不变”)。
(2)在碱式介质中,碱式电池的电极反应:
负极: ,正极: 。
电解质溶液pH的变化 (填“变大”,“变小”,“不变”)。
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是________。
A.太阳光催化分解水制氢气比电解水气氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH为介质的氢氧燃料电池的总反应式相同
(4)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
①该电池放电时负极反应式为_________________。
②放电时每转移3 mol电子,正极有________ mol K2FeO4被还原。
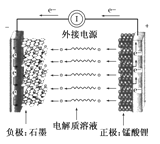
锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。
电池反应式为:Li1-xMnO4+Lix ![]() LiMnO4,下列有关说法不正确的是________。
LiMnO4,下列有关说法不正确的是________。
A.放电时电池的正极反应式为:Li1-xMnO4+xLi++xe-===LiMnO4
B.放电过程中,石墨没有得失电子
C.该电池也能在KOH溶液的环境中正常工作
D.充电时电池上标有“-”的电极应与外接电源的负极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com