
科目: 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)d在元素周期表的位置是__________。
(2)d、e、f常见简单离子的半径由大到小为___________(用化学式表示,下同);y、f、g、h的最高价氧化物对应的水化物的酸性由强到弱是:______________________________。
(3)用电子式表示由x和g两种元素形成的化合物的形成过程____________________。由x、y、d三种元素形成的相对分子质量最小的化合物可作为燃料电池的燃料,以KOH溶液为电解质溶液,写出负极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国产铜主要取自黄铜矿(CuFeS2),随着矿石品味的降低和环保要求的提高,湿法炼铜的优势日益突出。该工艺的核心是黄铜矿的浸出,目前主要有氧化浸出、配位浸出和生物浸出三种方法。
I.氧化浸出
(1)在硫酸介质中用双氧水将黄铜矿氧化,测得有SO42-生成。
①该反应的离子方程式为 。
②该反应在25—50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,试分析其原因为 。
Ⅱ.配位浸出
反应原理为:![]()
(2)为提高黄铜矿的浸出率,可采取的措施有 (至少写出两点)。
(3)为稳定浸出液的pH,生产中需要向氨水中添加NH4C1,构成NH3·H2O-NH4Cl缓冲溶液。某小组在实验室对该缓冲体系进行了研究:25℃时,向amol·L-l的氨水中缓慢加入等体积0.02 mol·L-l的NH4C1溶液,平衡时溶液呈中性。则NH3·H2O的电离常数Kb= (用含a的代数式表示);滴加NH4C1溶液的过程中水的电离平衡 (填“正向”、“逆向”或“不”)移动。
Ⅲ.生物浸出
在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
(4)在微生物的作用下,可以循环使用的物质有 (填化学式),微生物参与的离子反应方程式为____ (任写一个)。

(5)假如黄铜矿中的铁元素最终全部转化为Fe3+,当有2 mol SO42-生成时,理论上消耗O2的物质的量为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用化学知识解决生活中的问题,下列家庭小实验或说法不合理的是
A. 用米汤检验食盐中是否含碘酸钾(KIO3)
B. 用食醋除去暖水瓶中的薄层水垢
C. 医用酒精的浓度通常为75%,可用于杀菌消毒
D. 用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物
查看答案和解析>>
科目: 来源: 题型:
【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。

发生的反应如下:
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0g Na2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,并说明理由 。
(2)加入沸石的作用是 。若加热后发现未加沸石,应采取的正确方法 是 。
(3)上述装置图中,B的名称是 ,D仪器的名称是 。
(4)B仪器使用前必须进行的操作是 。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分液时,正丁醛在 层(填“上”或“下”)
(6)反应温度应保持在90—95℃,其原因是 ,为更好的控制温度,可以采取的改进措施是 。
(7)本实验中,正丁醛的产率为 %。
查看答案和解析>>
科目: 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是( )

A.工业生产中常选用NaOH作为沉淀剂
B.粗盐可采用溶解、过滤和重结晶等过程进一步提纯
C.向苦卤中通入Cl2是为了提取溴
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目: 来源: 题型:
【题目】以乙烯为原料合成化合物C的流程如图所示:

(1)B中含有的官能团名称为___________。
(2)写出A的结构简式:_______________________________。
(3)①、④的反应类型分别为__________反应、__________反应。
(4)写出反应②和④的化学方程式:
②________________________________________________________________;
④________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】 O2F2可以发生反应:H2S+4O2F2→SF6+2HF+4O2,下列说法正确的是( )
A.氧气是氧化产物 B.若生成4.48 L HF,则转移0.8 mol电子
C.O2F2既是氧化剂又是还原剂 D.还原剂与氧化剂的物质的量之比为1:4
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是A、B、C、D、E、F等几种常见有机物之间的转化关系图.其中A是面粉的主要成分;C和E反应能生成F,F具有香味.
![]()
在有机物中,凡是具有﹣CHO结构的物质,具有如下性质:
(1)与新制的氢氧化铜悬浊液反应,产生砖红色的沉淀;
(2)在催化剂的作用下,﹣CHO被氧气氧化为﹣COOH,即:
2R﹣CHO+O2 ![]() 2R﹣COOH
2R﹣COOH
根据以上信息及各物质的转化关系完成下列各题:
(1)A的分子式为 ,B中含有的官能团有 ,与B互为同分异构体的一种物质的名称 。
(2)A→F中,能与新制氢氧化铜悬浊液产生砖红色的沉淀的物质有 (填名称)。
(3)E与小苏打溶液反应的离子方程式为 。
(4)C→D的化学方程式为
反应类型为 反应。
(5)C+E→F的化学方程式为 。
(6)写出符合下列条件的F的所有同分异构体的结构简式
①与F具有相同的官能团
②没有支链。
查看答案和解析>>
科目: 来源: 题型:
【题目】向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是
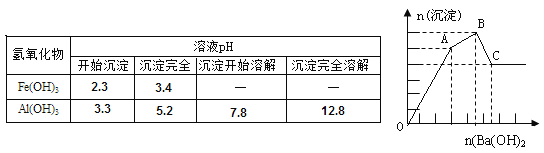
A.AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-=2BaSO4↓+Al(OH)3↓
B.C点的沉淀为Fe(OH)3
C.OA段可能发生的反应是:3Ba2++6OH-+3SO42-+Fe3++Al3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓
D.据图计算原溶液中c(Cl-)>c(SO42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com