
科目: 来源: 题型:
【题目】美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示)。下列有关该工艺的说法错误的是

A.该过程中,能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金与水反应的化学方程式为2Al+3H2O![]() Al2O3+3H2↑
Al2O3+3H2↑
D.总反应式为2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】七水硫酸镁(MgSO47H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣﹣硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 | ||||||
pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 | ||||||
表2 两种盐的溶解度(单位为g/100g水)
温度/℃ | 10 | 30 | 40 | 50 | 60 | ||||||||||||
CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 | ||||||||||||
MgSO47H2O | 30.9 | 35.5 | 40.8 | 45.6 | / | ||||||||||||
硼镁泥制取七水硫酸镁的工艺流程如下:
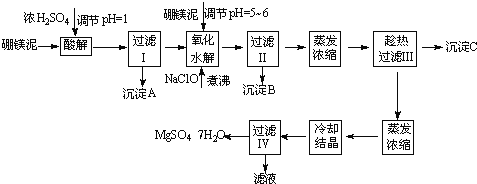
根据以上流程图并参考表格pH数据和溶解度数据,试回答下列问题:
(1)过滤I的滤液中加入硼镁泥,调节溶液的pH=5~6,再加入NaClO溶液加热煮沸,将溶液中的Mn2+氧化成MnO2,反应的离子反应方程式为 .加热煮沸的主要目的是 。
(2)沉淀B中除MnO2、SiO2外还含有 (填化学式)等物质。
(3)检验过滤Ⅱ后的滤液中是否含有Fe3+的实验方法是 。
(4)沉淀C的化学式是 .过滤Ⅲ需趁热过滤的理由是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某原电池装置如下图所示,电池总反应为2Ag+Cl2===2AgCl。下列说法正确的是( )

A. 正极反应为AgCl+e-===Ag+Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目: 来源: 题型:
【题目】碘及其化合物在生产、生活和科技等方面都有着重要的应用。回答下列问题:
(1)碘不宜溶于水,但易溶于碘化钾溶液并生成多碘离子,反应如下:
①I2(s)+I-(aq)![]() I3-(aq) △H<0;②I2(s)+2I-(aq)
I3-(aq) △H<0;②I2(s)+2I-(aq)![]() I42-(aq)。反应②的平衡常数的表达式为K=___________。温度升高时,反应①的平衡常数将____________(填“增大”“减小”或“不变”)
I42-(aq)。反应②的平衡常数的表达式为K=___________。温度升高时,反应①的平衡常数将____________(填“增大”“减小”或“不变”)
(2)碘与钨在一定温度下,可发生如下可逆反应:W(s)+I2(g)![]() WI2(g)。现准确称取0.508g碘和0.736g金属钨放置于50.0mL的密闭容器中,并加热使其反应。如图是混合气体中的WI2蒸气的物质的量随时间变化关系的图象[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃。
WI2(g)。现准确称取0.508g碘和0.736g金属钨放置于50.0mL的密闭容器中,并加热使其反应。如图是混合气体中的WI2蒸气的物质的量随时间变化关系的图象[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃。
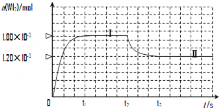
①该反应△H__________0(填“>”或“<”)。
②反应从开始到t1(t1= 3 min)时间内的平均速率v(I2)= 。
③在450℃时,该反应的平衡常数K=______________。
④能够说明上述反应已经达到平衡状态的有 (填选项字母)。
A.I2与WI2的浓度相等
B.单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等
C.容器内混合气体的密度不再改变
D.容器内气体压强不发生变化
(3)I2O5是白色粉末状固体,可用作氧化剂使H2S、CO、HC1等氧化,在合成氨工业中常用I2O5来定量测量CO的含量。已知:①2I2(s)+5O2(g)=2I2O5(s) ΔH=-75.56kJmol-1②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJmol-1 。写出CO(g)与I2O5(s)反应析出固态I2的热化学方程式:__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中错误的是:( )
①化学性质相似的有机物是同系物
②分子组成相差一个或几个CH2原子团的有机物是同系物
③若烃中碳.氢元素的质量分数相同,它们必定是同系物
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似.
A.①②③④ B.只有②③ C.只有③④ D.只有①②③
查看答案和解析>>
科目: 来源: 题型:
【题目】由反应物X转化为Y和由反应物X转化为Z的能量变化如图所示。下列说法正确的是
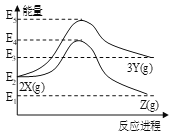
A. 2X(g)![]() 3Y(g)反应的ΔH=E5E2
3Y(g)反应的ΔH=E5E2
B. 2X(g)![]() Z(g)反应的ΔH<0
Z(g)反应的ΔH<0
C. 增大压强有利于提高Y的产率
D. 升高温度有利于提高Z的产率
查看答案和解析>>
科目: 来源: 题型:
【题目】金属(M)—空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n。已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能。下列说法不正确的是
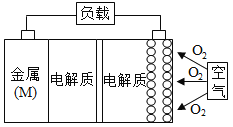
A.采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B.比较Mg、Al、Zn三种金属—空气电池,Al—空气电池的理论比能量最高
C.M—空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne-=4M(OH)n
D.在M—空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。设起始
CO(g)+3H2(g)。设起始![]() =Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法正确的是
=Z,在恒压下,平衡时CH4的体积分数φ(CH4)与Z和T(温度)的关系如图所示,下列说法正确的是

A.该反应的焓变 △H>0
B.图中Z的大小为 a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后φ(CH4)减小
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2等。利用该固体废渣制取Cu (NO3)2的部分工艺流程如图所示:

(1)Cu2O与稀硝酸反应的离子方程式为 。
(2)酸溶时,反应温度不宜超过70℃,其主要原因是 ,若保持反应温度为70℃,欲加快反应速率可采取的措施为 (写出一种即可)。
(3)过滤后所得废渣的主要成分的化学式为 。
(4) Cu(NO3)2晶体受热易分解成CuO,同时产生NO2和O2,该反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量。已知白磷和P4O6。分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198 P—O:360 O===O:498

若生成1 mol P4O6,则反应P4(白磷)+3O2===P4O6中的能量变化为
A.吸收1 638 kJ能量
B.放出126 kJ能量
C.吸收126 kJ能量
D.放出1 638 kJ能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com