
科目: 来源: 题型:
 在密闭容器中进行如下反应:mA(g)+nB(g)?pC(g),反应经5min达到平衡,测得此时A的浓度减小了a mol?L-1,而C的浓度增加了
在密闭容器中进行如下反应:mA(g)+nB(g)?pC(g),反应经5min达到平衡,测得此时A的浓度减小了a mol?L-1,而C的浓度增加了| 2 |
| 3 |
| c2(C) |
| c3(A)?c(B) |
| c2(C) |
| c3(A)?c(B) |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
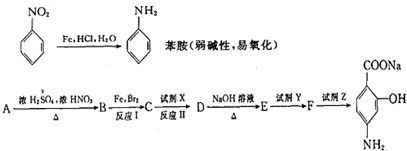
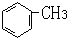
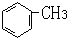


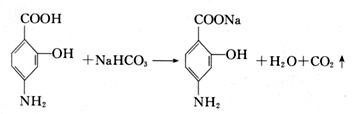

查看答案和解析>>
科目: 来源: 题型:阅读理解
 (2011?濮阳二模)A、B、C、D、E五种元素都是36号以前元素,原子序数依次增大,其相关信息如下表
(2011?濮阳二模)A、B、C、D、E五种元素都是36号以前元素,原子序数依次增大,其相关信息如下表| 元素 | 相关信息 |
| A | A的第一电离能低于同周期相邻元素 |
| B | B原子中成对电子数等于未成对电子数的2倍 |
| C | C原子p轨道和s轨道中的电子数相等,与非金属的原子结合时形成共价键 |
| D | D与A、B、C均不同周期,其单质分子中只有一条共价键 |
| E | E在所处周期中电负性最大,且与D是同一主族元素 |
查看答案和解析>>
科目: 来源: 题型:
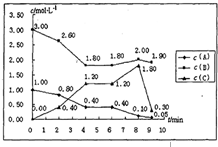 在一个容积固定为1L的密闭容器中,发生反应mA(g)+nB(g)═pC(g)△H=?.反应情况如下图所示:
在一个容积固定为1L的密闭容器中,发生反应mA(g)+nB(g)═pC(g)△H=?.反应情况如下图所示:| 10 |
| 9 |
| 10 |
| 9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com