
科目: 来源: 题型:
【题目】一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,2SO2(g)+O2(g)![]() 2SO3(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
2SO3(g),其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是

A.甲中反应的平衡常数小于乙B.该温度下,该反应的平衡常数K为400
C.SO2的平衡转化率:a1>a2=a3D.容器中S03的物质的量浓度:丙=丁<甲
查看答案和解析>>
科目: 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、Fe3+、SO![]() 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐![]()
![]()
![]()
![]()
![]() 滤液
滤液![]()
![]() 精盐
精盐
(1)判断BaCl2已过量的方法是__________________。
(2)第④步中,相关的化学方程式是______________________。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家预测,氨有望取代氢能,成为重要的新一代绿色能源。下列有关说法不正确的是
A.液氨作为清洁能源的反应原理是4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
B.液氨具有腐蚀性和毒性,在使用过程中要防止液氨泄漏
C.氨气比空气轻,标准状况下密度约为0.76 g·L-1
D.氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式正确的是
A.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH―=NH3↑+H2O
B.用惰性电极电解饱和氯化钠溶液:2Cl―+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
C.向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I―=2Fe2++I2
D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32―+6H++2MnO4―=5SO42―+2Mn2++3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1,E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略)请按要求填空:
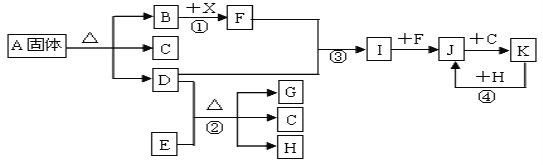
(1)A物质的化学式是 ;
(2)反应①中产生标准状况下1.12L气体F,则转移的电子数目是 ;
(3)反应③的化学方程式是 ;
(4)反应④的离子方程式是 ;
查看答案和解析>>
科目: 来源: 题型:
【题目】
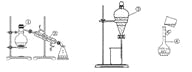
(1)写出下列仪器的名称:①_______________:②___________
(2)仪器①~④中,使用时必须检查是否漏水的有______(填序号)。
(3)若利用装置Ⅰ分离两种液态有机物乙二醇和丙三醇组成的混合物,还缺少的仪器有____,将仪器指补充完整后进行实验,②的进水口是_(填“f”或“g”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭气缸中,用一不漏气的滑动活塞隔开。常温时,左边充入1/4体积的N2,右边充入3/4体积的H2和O2的混合气。若右边气体点燃,反应后恢复到原温度,活塞停留在气缸正中,则原来混合气中H2和O2的体积比是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡;另一份加入含b mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁。则原混合溶液中钾离子的浓度为
A.![]() mol/L B.
mol/L B.![]() mol/L
mol/L
C.![]() mol/L D.
mol/L D.![]() mol/L
mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生欲配制6.0 mol/L的H2SO41 000 mL,实验室有三种不同浓度的硫酸:①480 mL 0.5 mol/L 的硫酸;②150 mL 25%的硫酸(ρ=1.18 g/mL);③足量的18 mol/L的硫酸。有三种规格的容量瓶:250 mL、500 mL、1 000 mL。老师要求把①②两种硫酸全部用完,不足的部分由③来补充。
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为__ ____mol/L(保留1位小数)。
(2)此实验所需的仪器为量筒、玻璃棒、胶头滴管、 、 。
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整。
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18 mol/L的浓硫酸_______mL,沿玻璃棒倒入上述混合液中。并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.________________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2 cm 处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀。
(4)如果省略操作D,对所配溶液浓度有何影响?_________(填“偏大”、“偏小”或“无影响”)。
(5)进行操作C前还需注意___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com