
科目: 来源: 题型:
【题目】化学反应中,有时“一种物质过量,另一种物质仍不能完全反应”。下列反应中不存在此类情况的是
A. 铁片与过量浓硝酸(常温) B. 铜粉与过量浓硝酸(常温)
C. 浓盐酸与过量MnO2(共热) D. 浓硫酸与过量铜片(共热)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同。回答下列问题:
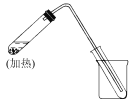
(1)左边大试管中要加入几片碎瓷片,其作用是_________________;
(2)该装置中使用的玻璃导管较长,其作用是__________________;
(3)烧杯中还要盛有的物质是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】
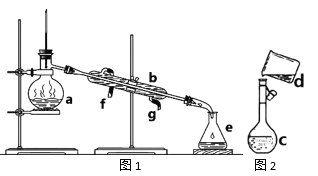
(1)写出下列仪器的名称:a:__________
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是_____________,将仪器补充完整后进行实验,冷凝水由___________(填f或g)口通入。
(3)现需配制0.lmol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是________________。除了图中给出的仪器和托盘天平外,为完成实验还需要的仪器有:_____________。
②根据计算得知,需称量NaOH的质量为_________g。
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)______ ______。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④下列操作使配制的NaOH溶液浓度偏低的有_________。
A.称量氢氧化钠时间过长 B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线 D.定容时俯视刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)甲醇(CH3OH)是一种重要的化工原料。已知
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H =-566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = + 44.00 kJ·mol-1
①试写出能表示CH3OH(1)燃烧热的热化学方程式: 。试利用热化学方程式计算,完全燃烧16g甲醇生成CO2和H2O(l)时,放出的热量为 kJ
②科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池。据此回答下列问题:氧气在 极反应;通入甲醇的电极反应式为_________________
(2)如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图像,回答问题:
①该反应的方程式为 。
②2min内,用B表示的反应速率为 。
③在其他条件下,测得A的反应速率为0.05mol/(L·s),此时的反应与800℃时相比, 。
A.比800℃时快 B.比800℃时慢
C.和800℃时速率一样 D.无法比较
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中,使2molN2和6molH2混合发生下列反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应)
2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是_______;N2和H2的转化率比是_________。
(2)升高平衡体系的温度(保持体积不变),混和气体的平均相对分子质量__________,密度___________。(填“变大”、“变小”或“不变” )
(3)当达到平衡时,将c(N2)、c(H2)、c(NH3)同时减小一倍,平衡将向__________移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将向_______________移动。
(5)若容器恒容,绝热、加热使容器内温度迅速升至原来的2倍,平衡将______________(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_____________(填“大于”“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用图Ⅰ所示的装置验证一些物质的性质。下列说法错误的是
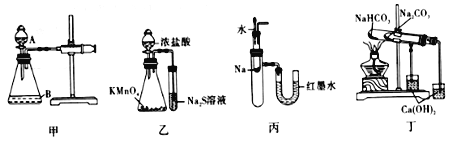
A.图甲中,为检查装置的气密性,可关闭分液漏斗A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否复原
B.图已中,可以比较KMnO4、Cl2和S氧化性的相对强弱
C.将胶头滴管中的水滴入到金属钠中,能看到U型管右侧红墨水上升
D.图丁中,可用装置验证NaHCO3和Na2CO3的热稳定性强弱
查看答案和解析>>
科目: 来源: 题型:
【题目】配制物质的量浓度为0.1 mol/L的Na2CO3溶液l00mL时,下列操作正确的是( )
A. 用托盘天平称取l.06g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 定容时,若仰视,则所配溶液的浓度将偏高
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上制取氯酸钾的主要步骤为:
I.将C12通入石灰浆,充分反应后过滤;
II.向滤液中加入稍过量的KCl固体,进行适当操作可析出KClO3固体。
请回答下列问题:
步骤I存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,总反应的化学方程式为6Ca(OH)2+ 6Cl2=Ca(ClO3)2+5CaCl2+ 6H2O 。
(1)①标出反应6Ca(OH)2+ 6Cl2=Ca(ClO3)2+5CaCl2+ 6H2O 中电子转移的方向和数目
② 滤液中Ca(ClO3)2与CaC12的物质的量之比n[Ca(ClO3)2]:n [CaCl2]___________l:5(填“>”、“<”或“=”),理由是___________ 。(请用有关反应和必要的文字进行说明)
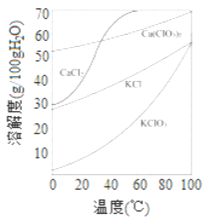
(2)上图是有关物质的溶解度曲线. 步骤II中,若溶液中KClO3的含量为100g·L-1,从该溶液中尽可能多地析出KClO3 固体的方法是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某双原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA,则:
(1)该气体的物质的量为__________;
(2)该气体在标准状况下的体积为__________;
(3)该气体在标准状况下的密度为________;
(4)该气体所含原子总数为__________;
(5)该气体的一个分子的质量为__________。
(6)标准状况下,112 mL某气体的质量为0.14 g,则其摩尔质量为________,相对分子质量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.64 g SO2含有氧原子数为2NA
B.物质的量浓度为0.5 mol·L-1的MgCl2溶液,含有Cl-数为1 NA
C.标准状况下,22.4 L H2O的分子数为1NA
D.常温常压下,14 g N2含有分子数为0.5 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com