
科目: 来源: 题型:
【题目】右图为部分元素在元素周期表中的相对位置。据此回答相关问题:

(1)其中非金属性最强的是 (填元素符号)。
(2)N、P两种元素的最高价氧化物对应的水化物的酸性:HNO3 H3PO4(填“>”、“=”或“<”)。
(3)O位于元素周期表中的第 族。
(4)S、Cl两种元素氢化物的稳定性:H2S HCl(填“>”、“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类:
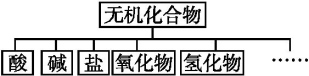
(1)上述所示物质分类方法的名称是 。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面。(各空填写一个化学式即可)
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O |
(3)写出⑦转化为⑤的化学方程式: 。
(4)写出①与③反应的离子方程式: 。
(5)写出②与⑤反应的离子方程式: 。
(6)书写下列反应的离子方程式
①Fe与CuSO4溶液反应:_________________________;
②CaCO3和稀盐酸溶液:__________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是对某水溶液进行离子检验的方法和结论,其中正确的是
A. 先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀。溶液中一定含有大量的SO42-
B. 加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定含有大量的CO32-
C. 加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体,该气体可以使湿润的红色石蕊试纸变蓝,则溶液中一定含有大量的NH4+
D. 先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】下列分子或离子在指定溶液中能大量共存的是( )
A.酸性溶液中:Cl-、SO![]() 、Fe3+、Mg2+
、Fe3+、Mg2+
B.使酚酞变红的溶液中:Na+、CO32-、Cl-、Al3+
C.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO![]()
D.1.0 mol·L-1的CuSO4溶液:H+、Ba2+、AlO2-、NH3·H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】已经部分被氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.92g,经如下处理:

下列说法不正确的是
①滤液A中的阳离子为Fe2+、Fe3+、H+
②V=224mL ③V=336mL
④样品中含氧元素的物质的量为0.03mol
⑤溶解样品的过程中消耗硫酸的总物质的量为0.04mol
A. ①③ B. ①③④ C. ②④⑤ D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A可以作水果的催熟剂,D是食醋的主要成分。相关的转化关系如下:
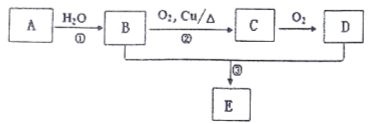
请回答下列问题:
(1)A的结构简式为 ,反应①的反应类型是 。
(2)C的名称是 。
(3)反应③的化学方程式为 ,该反应类型是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】用稀硝酸腐蚀废锌板后得到“烂版液”(含有微量的Cl-、Fe3+),某化学兴趣小组拟用该“烂版液”制取Zn(NO3)2·6H2O的过程如下:
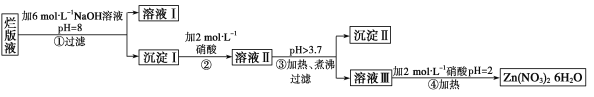
已知: Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)为检验“烂版液”中的Fe3+,下列试剂可选择的是 (填选项的代号)
A、NaOH溶液 B、KSCN溶液 C、K3[Fe(CN)6] 溶液 D、NaCl溶液
(2)若稀硝酸腐蚀锌板产生的气体为N2O,写出稀硝酸腐蚀锌板反应的主要化学方程式_________。
(3)在操作①中保持pH=8的目的是___________;操作④保持pH=2的目的是__________________;
(4)操作③中加热、煮沸的目的是___________________________;
(5)沉淀Ⅱ的主要成分是______________________。
(6)已知金属活泼性不同,其硝酸盐的分解产物也不同。
2KNO3=2KNO2+O2↑ 4Fe(NO3)2=2Fe2O3+8NO2↑+O2↑ 2Zn(NO3)2=2ZnO+4NO2↑+O2↑
某同学取KNO3、Zn(NO3)2、Fe(NO3)2混合粉末充分加热后,用排水法未收集到任何气体,则KNO3、 Zn(NO3)2、Fe(NO3)2的物质的量之比为 (填选项的代号)
A、2︰1︰3 B、1︰2︰2 C、1︰2︰3 D、3︰8︰5
查看答案和解析>>
科目: 来源: 题型:
【题目】某金属加工厂排放的污水中含有CuSO4、ZnSO4、FeSO4,某研究小组利用该污水回收工业重要原料硫酸锌和有关金属,其流程如右图所示:请回答下列问题:

(1)下列说法正确的是________。
A.该工艺流程中发生了3个置换反应
B.CuSO4与MgCl2可以发生复分解反应
C.步骤①②③④都包含化学变化
D.滤液A和滤液B含有相同的溶质
(2)写出步骤①发生反应的离子方程式:_______________、________________。
(3)步骤④中加入足量稀硫酸的目的是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】
A. 同一生物体不同组织细胞内化学元素种类和含量大体相同
B. C、H、O、N是组成生物体内酶所必需的元素
C. 蛋白质中的S元素存在于氨基酸的R基中
D. 占细胞的鲜重最多的元素是O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com