
科目: 来源: 题型:
【题目】完全沉淀等物质的量浓度的NaCl、MgCl2、A1C13溶液中的Cl-,消耗等物质的量浓度的AgNO3溶液的体积比为3: 2: 1,则上述溶液的体积比为
A.1: 1: 1 B.3: 2: 1 C.9: 3: 1 D.6: 3: 2
查看答案和解析>>
科目: 来源: 题型:
【题目】分子式为C3H7ClO,加入金属钠能产生气体,符合条件的同分异构体数目为(不考虑空间异构)( )
A. 5 种 B. 4 种
C. 3 种 D. 2 种
查看答案和解析>>
科目: 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法正确的是
A.1mol苯乙烯(![]() )中含有的C=C数为4NA
)中含有的C=C数为4NA
B.标准状况下,2.24L己烷含有的分子数为0.1NA
C.1mol甲基含10NA个电子
D.某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
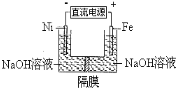
A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+
B.若隔膜为阴离子交换膜,则OH-自右向左移动
C.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,0.2 molL-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
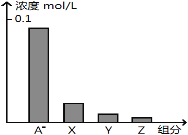
A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】由下列实验事实得出的结论正确的是( )
A. 由SiO2不能与水反应生成H2SiO3,可知SiO2不是H2SiO3的酸酐
B. 由SiO2+2C![]() Si+2CO↑,可知碳的非金属性大于硅
Si+2CO↑,可知碳的非金属性大于硅
C. CO2通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3
D. SiO2可与NaOH溶液反应,也可与氢氟酸反应,可知SiO2为两性氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热、充分反应后,过滤,弃掉滤渣,滤液中金属离子情况不可能是
A. 只含Cu2+、Fe3+、Zn2+ B. 只含Zn2+
C. 只含Zn2+、Fe2+ D. 只含Cu2+、Fe2+、Zn2+
查看答案和解析>>
科目: 来源: 题型:
【题目】锌焙砂是锌精矿经焙烧后所得的产物,主要含ZnO、ZnSO4,有少量FeO、CuO、NiO杂质,是炼锌最主要的原料。某科研小组设计了如下提取金属锌的实验流程:
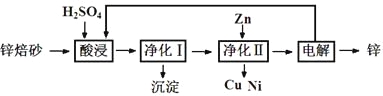
(1)酸浸时需要240 mL 4 mol·L-1稀H2SO4,用18.4 mol·L-1浓硫酸配制该稀H2SO4过程
中用到的玻璃仪器除烧杯、量筒、胶头滴管外,还要 、 ;酸浸得到的溶液中除Zn2+、Ni2+外,还含有的金属阳离子是 、 (填离子符号)。
(2)净化Ⅰ需要加入H2O2,加入H2O2时发生的离子反应方程式是 ;反应后控制溶液pH为4即沉淀完全,沉淀的主要成分是 。
(3)净化Ⅱ得到的Cu、Ni,需要进行洗涤操作,检验是否洗涤干净的方法是 ;本流程中可以循环利用的物质除锌外还有 、 。
(4)可用电解沉积硫酸锌溶液的方法制备锌,若在在阳极产生13.44L(标准状况下) 氧气,在阴极析出锌的质量为 。
(5)上述工艺中,如果不设计 “净化Ⅱ”,对提取金属锌造成的影响是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃A的相对分子质量为84.回答下列问题:
(1)烃A的分子式为 。
(2)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是 ;若总质量一定,充分燃烧消耗氧气的量不变的是 。
A.C7H8 B.C6H14 C.C7H14 D.C8H8
(3)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。
① A的结构简式为 名称为 。
② 链烃A与Br2的CCl4溶液反应生成B,写出由A生成B的化学方程式: 。
③ 与A互为同分异构体,且主链碳原子个数与A相同的链烃有 种(不包括A)
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com