
科目: 来源: 题型:
【题目】室温下,用0.1000mol/L盐酸滴定25mL0.1000mol/LNa2A溶液(已知H2A为二元弱酸),其滴定曲线如图所示,下列对滴定中所得溶液的相关离子浓度关系判断正确的是
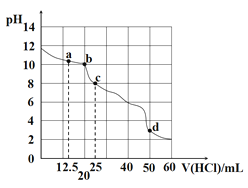
A.a点:c(A2-)=c(HA-)
B.b点:5c(Cl-)=4[c(A2-)+c(HA-)+c(H2A)]
C.c点:c(Na+)>c(HA-)>c(A2-)>c(H2A)
D.d点:c(H+)=c(HA-)+c(A2-)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示。

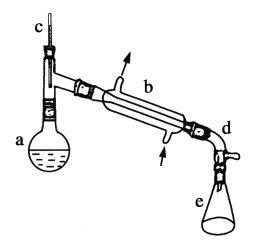
可能用到的相关数据如下:
相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是____________。
(2)加入碎瓷片的作用是______________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并________;在本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口放出”)。
(4)分离提纯过程中加入无水氯化钙的目的是______________。
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________(填正确答案标号)。
A.圆底烧瓶
B.温度计
C.吸滤瓶
D.球形冷凝管
E.接收器
(6)本实验所得到的环己烯产率是________(填正确答案标号)。
A.41% B.50%
C.61% D.70%
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机物性质和结构的叙述正确的是
A. 聚丙烯可使酸性高锰酸钾溶液褪色
B. 向溴乙烷中加入硝酸银溶液,生成淡黄色沉淀
C. CH4、CCl4、CF2Cl2均为正四面体结构的分子
D. 苯的邻二溴代物只有一种,说明苯分子中碳碳键的键长完全相同
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为Amol/L与Bmol/L,则A和B关系为( )
A.A>B B.A=10-4 B C.B=10-4 A D.A=B
查看答案和解析>>
科目: 来源: 题型:
【题目】为了验证SO2的性质,某同学利用输液管设计了如下微型实验:
回答下列问题:
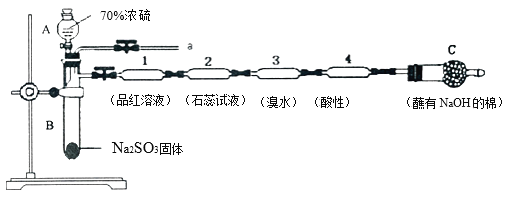
(1)仪器A的名称是__________。
(2)装置l中的现象是______;装置3中证明SO2具有______性。
(3)下列说法正确的是____________。
A.装置2中紫色石蕊试液变红的原因是SO2+H2O=H2SO3, H2SO3显酸性
B.实验结束后将输液管1加热溶液不变色
C.实验结束后,可由a导管向装置中加水,将气体赶出后再拆装置,防止残留的SO2有毒气体污染环境
D.在a导管处用向下排空气法收集SO2
(4)装置4中酸性高锰酸钾褪色,经测定反应后溶液中含有Mn2+和SO42—,请写出该反应的离子方程式__________。
(5)该学生还利用上图部分仪器组装成的装置(如图)证明S、C、Si非金属性强弱。可共选择的试剂有:硫酸、亚硫酸、硝酸、木炭、硅酸钠溶液。
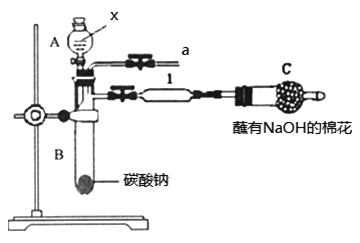
①装置A中试剂X是_______;装置1中反应的化学方程式是________。
②实验结论:因为酸性强弱是____>_____>_____(填化学式),故非金属性是S>C>Si。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com