
科目: 来源: 题型:
【题目】A、B、C、D是短周期元素组成的中学常见的四种物质,它们之间有下图所示的转化关系。已知:A是空气中的主要成分,B、C、D均为化合物,且C为红棕色气体。

请回答下列问题:
(1)写出B和C的化学式:B________,C________;
(2)写出A的电子式:____________;
(3)在D的稀溶液中滴入NaOH溶液,其反应的离子方程式是____________________;
(4)写出上图D→C的化学方程式:________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将4 mol A气体和2 mol B气体充入2 L的密闭容器中,一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g)。若经2 s后测得C的浓度为0.6 mol ·L-1,下列几种说法正确的是
2C(g)。若经2 s后测得C的浓度为0.6 mol ·L-1,下列几种说法正确的是
①用物质A表示的反应平均速率为0.3 mol ·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol ·L-1·s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol ·L-1
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能证明甲酸(HCOOH,一元酸)为弱酸的是( )
A.0.1mol/L甲酸的pH为2.3
B.将pH=2的甲酸稀释100倍后,溶液的pH小于4
C.温度升高,溶液的导电能力增强
D.等体积等浓度的甲酸和HCl与足量的锌反应,产生等量的氢气
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应A(g)+3B(s)![]() 2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A.v(A)=0.5 mol·L-1·min-1 B.v(B)=1.2 mol·L-1·s-1
C.v(D)=0.4 mol·L-1·min-1 D.v(C)=0.1 mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
【题目】糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是
A.植物油不能使溴的四氯化碳溶液褪色
B.葡萄糖能发生氧化反应和水解反应
C.麦芽糖水解的最终产物是葡萄糖
D.蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成的盐只有NaH2PO2一种。等浓度的次磷酸(H3PO2)溶液与盐酸,前者导电能力弱。下列说法错误的是( )
A.H3PO2中,P元素的化合价为+1价
B.H3PO2为一元弱酸,NaH2PO2溶液呈碱性。
C.次磷酸在水中的电离方程式为H3PO2+H2O![]() H2PO2—+ H3O+
H2PO2—+ H3O+
D.NaH2PO2属于酸式盐
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L 盐酸和20.00 mL 0.1000 mol/L 醋酸溶液,得到2条滴定曲线,如下图所示。若以HA表示酸,下列说法正确的是( )
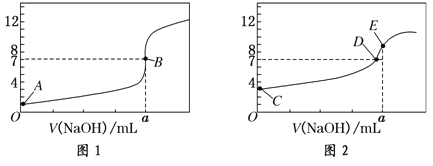
A.滴定盐酸的曲线是图2
B.达到B、D状态时,两溶液中离子浓度均为c(Na+) = c(A—)
C.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
D.当0 mL< V(NaOH) <20.00 mL时,对应混合溶液中各离子浓度由大到小的顺序均为 c(A—) >c(Na+)> c(H+) > c(OH—)
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)W原子的核外电子排布式为_________。
(2)均由X、Y、Z三种元素组成的三种常见物质A、B、C分别属于酸、碱、盐,其化学式依次为_________、__________、_________,推测盐中阴离子的空间构型为__________,其中心原子杂化方式为__________。
(3)Z、W两种元素电负性的大小关系为____;Y、Z两种元素第一电离能的大小关系为____。
(4)CO的结构可表示为C![]() O,元素Y的单质Y2的结构也可表示为Y
O,元素Y的单质Y2的结构也可表示为Y![]() Y。右表是两者的键能数据(单位:kJ·mol-1):
Y。右表是两者的键能数据(单位:kJ·mol-1):

①结合数据说明CO比Y2活泼的原因:_____。
②意大利罗马大学Fulvio Cacace等人获得了极具研究意义的Y4分子,其结构如图所示,请结合上表数据分析,下列说法中,正确的是_____。

A.Y4为一种新型化合物 B.Y4与Y2互为同素异形体
C.Y4的沸点比P4(白磷)高 D.1 mol Y4气体转变为Y2将放出954.6kJ热量
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列有关图象,说法正确的是( )
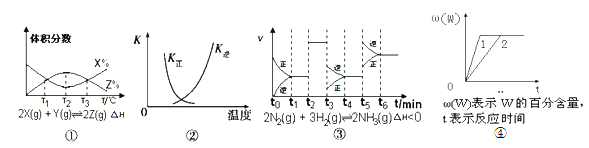
A. 由图①知,反应在T1、T3处达到平衡,且该反应的△H<0
B. 图②中曲线表示反应2SO2(g)+O2(g) ![]() 2SO3(g),ΔH<0的正、逆反应平衡常数K随温度的变化
2SO3(g),ΔH<0的正、逆反应平衡常数K随温度的变化
C. 由图③知,反应在t6时,NH3体积分数最大。
D. 其他条件不变时,图④中曲线表示不同压强对反应aX(g)+bY(s)![]() nW(g)的影响,且P1>P2,n=a+b。
nW(g)的影响,且P1>P2,n=a+b。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用中和滴定法测定某烧碱样品的纯度。先准确称量10.0g含有少量中性易溶杂质的样品,配成500mL待测溶液。用0.200mol/L的盐酸标准液滴定待测液,滴定时用酚酞做指示剂。试根据实验回答下列问题:
(1)下列有关滴定操作的顺序正确的是
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液
③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④ B.③⑤①②④ C.③⑤②①④ D.②①③⑤④
(2)用标准的盐酸滴定待测的NaOH溶液时,一手握酸式滴定管的活塞,一手摇动锥形瓶,眼睛注视_________,本实验滴定达到终点的标志是_________________________。
(3)根据下表数据,计算被测烧碱溶液的物质的量浓度是 ,烧碱样品的纯度是___________
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前刻度(mL) | 滴定后刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
第三次 | 10.00 | 0.20 | 24.20 |
(4)若该实验修改成“用待测碱液滴定盐酸标准液”,则下列操作会使烧碱样品纯度偏高的是
A.锥形瓶用蒸馏水洗净后,先用盐酸标准液润洗再装标准液。
B.碱式滴定管用蒸馏水洗净后未润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前仰视碱式滴定管读数,滴定后俯视滴定管读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com