
科目: 来源: 题型:
【题目】已知Ksp (CaC2O4)=4.010-9,若在c(Ca2+)=0.020mol·L-1的溶液生成CaC2O4沉淀,溶液中的c(C2O42-)最小应为( )
A. 4.010-9mol·L-1 B. 2.010-7mol·L-1 C. 2.010-9mol·L-1 D. 8.010-11mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求回答下列问题。
(1)用大理石和稀盐酸反应制CO2,产生CO2的体积与反应时间的关系如图所示,其中产生CO2速率最快的为____________段(选填“OE”、“EF”或“FG”),其主要原因为____________________,若要使该反应的反应速率加快,下列措施不可行的是______(选填序号);

①将大理石换用碳酸钙粉末 ②加入K2SO4溶液
③升高温度 ④加入NaCl固体
(2)请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,回答下列问题:
①该电池选择的电解质溶液为______(填化学式);
②负极材料为___________(填化学式),正极的电极反应式为______________;
③若导线上转移电子0.025mol,则生成银的质量为____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述不能体现相关主旨的是
A. “水域蓝天,拒绝污染”:严控PM 2.5排放,改善雾霾天气
B. “化学,引领科技进步”:研究合成光纤技术,让通讯更快捷
C. “节能减排,低碳经济”:综合利用煤和石油,发展绿色化学
D. “化学,让生活更美好”:积极开发风力发电,让能源更清洁
查看答案和解析>>
科目: 来源: 题型:
【题目】2015年12月12日,第21届联合国巴黎气候变化大会通过全球气候变化新协议.协议要求各国减少工业排放量的气体是( )
A.二氧化硫
B.氮的氧化物
C.二氧化碳
D.臭氧
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用电化学理论解释的是 ( )
A. 轮船水线以下的船壳上装一定数量的锌块
B. 铝片不用特殊方法保存
C. 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快
D. 镀锌的铁比镀锡的铁耐用
查看答案和解析>>
科目: 来源: 题型:
【题目】向2.0 L恒容密闭容器中充入1.0 mol PCl5,在温度为T℃时发生如下反应PCl5(g) ![]() PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
时间t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
回答下列问题:
(1)反应在前50 s的平均速率v(PCl5) = 。
(2)温度为T℃时,该反应的化学平衡常数= 。
(3)要提高上述反应的转化率,可采取的措施是 (任写一种)。
(4)在温度为T℃时,若起始时充入0.5 mol PCl5和a mol Cl2,平衡时PCl5的转化率仍为20%,则
a= 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(11分)某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。
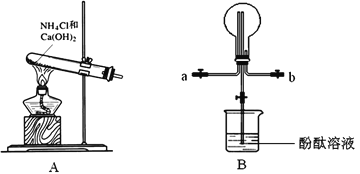
请回答:
(1)实验室制备氨气的化学方程式为 ;干燥氨气常用的干燥剂是 。
(2)收集氨气时,请你选择氨气的进气口 (填“a”或“b”),理由是 。
(3)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是 。
(4)为防止环境污染,以下装置(盛放的液体均为水)可用于吸收多余氨气的是 ( 填序号)。
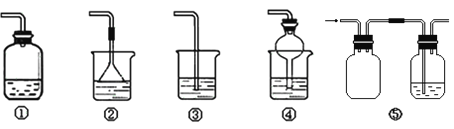
(5)氨气在催化剂并且加热时会被空气氧化,这是工业制硝酸的第一步反应,写出该反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com