
科目: 来源: 题型:
【题目】下列说法正确的是
A. 天然气和液化石油气的主要成分都是甲烷
B. 乙醇的沸点比丙烷高,是因为乙醇分子间存在氢键
C. 福尔马林有一定毒性,不能作消毒剂和防腐剂
D. 苯酚有毒,不慎沾到皮肤上,可以用氢氧化钠溶液处理
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 分子晶体中一定存在分子间作用力,不一定存在共价键
B. 分子中含两个氢原子的酸一定是二元酸
C. 含有共价键的晶体一定是分子晶体
D. 元素的非金属性越强,其单质的活泼性一定越强
查看答案和解析>>
科目: 来源: 题型:
【题目】氯仿(CHCl3 , 非电解质)在空气中能发生缓慢氧化,生成剧毒物质光气(COCl2 , 非电解质),化学方程式为2CHCl3+O2=2COCl2+2HCl.检验氯仿是否被氧化应选用的试剂是( )
A.水
B.NaOH溶液
C.酚酞溶液
D.硝酸酸化的硝酸银溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】I.请根据化学反应与热能的有关知识,填写下列空白:
(1)下列反应中,属于吸热反应的是_________(填数字序号)。
①煅烧石灰石制生石灰 ②燃烧木炭取暖 ③铝粉与氧化铁粉末在高温下反应
④酸碱中和反应 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)已知H2和O2反应放热,且断开1molH-H、1mo1O=O、1molO-H键需吸收的能量分别为Q1kJ、Q2kJ、Q3kJ,由此可以推知下列关系正确的是______(填字母编号)。
A. Q1+ Q2> Q3 B. 2Q1+ Q2<4 Q3 C. Q1+Q2>2Q3 D. 2Q1+Q2<2Q3
II.已知2mol氢气燃烧生成液态水时放出572KJ热量,反应的热化学方程式是2H2(g)+O2(g)=2H2O(l) △H=-572KJ·mol-1。
(3)该反应生成物的能量总和______(填“大于”“小于”或“等于”)反应物的能量总和。
(4)若2mol氢气完全燃烧生成水蒸气,则放出的热量_______(填“>”“<”或“=”)572KJ。
III.(5)已知16g固体硫完全燃烧时放出148.4KJ的热量,写出表示硫的燃烧热的热化学方程式:____________________________________。
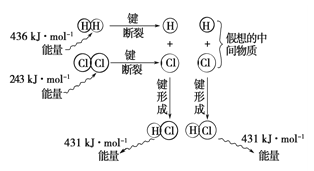
(6)观察下图,计算1molH2与1molCl2反应_______(“吸收”或“释放”)的能量为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,5种银盐的溶度积常数(Ksp)分别是:
AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
下列说法正确的是
A. 氯化银、溴化银和碘化银的溶解度依次增大
B. 将硫酸银溶解于水后,向其中加入少量硫化钠溶液,不能得到黑色沉淀
C. 在5mL1.8×10-5mol/L的NaCl溶液中,加入1滴(1mL约20滴)1.0×10-3 mol/L的AgNO3溶液,能观察到白色沉淀
D. 将浅黄色溴化银固体浸泡在饱和氯化钠溶液中,可以有少量白色固体生成窗体顶端
查看答案和解析>>
科目: 来源: 题型:
【题目】在澄清透明强酸性溶液中,能大量共存的离子组是( )
A.K+、Cu2+、OH﹣、SO42﹣
B.Fe3+、NH4﹣、NO3﹣、Cl﹣
C.K+、Na+、Cl﹣、CO32﹣
D.K+、Fe2﹣、MnO4﹣、SO42﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】I.电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
(1)请写出FeCl3溶液与铜反应的化学方程式:______________________________________。
检验反应后的溶液中存在Fe3+的试剂常用硫氰化钾溶液,写出反应的离子方程式:_____________________。
II.铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料.工业上提取氧化铝的工艺流程如下:

(2)沉淀A的成分是(填化学式)_________。
(3)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H++OH﹣=H2O还有:
_____________________________、________________________________;
(4)步骤③中通入过量CO2气体的离子方程式是______________________;
(5)准确称取8g铝土矿样品,加入一定量试剂a的溶液,使其中的Al2O3、Fe2O3恰好溶解;然后,向滤液中加入10mol·L-1的NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,则样品中Al2O3的百分含量为_________。

III.(6)某一反应体系有反应物和生成物共五种物质:O2 、H2CrO4 、Cr(OH)3 、H2O 、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
写出反应的化学方程式_____________________________________________,如反应转移了0.3mol电子,则产生的气体在标准状况下体积为_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。

(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为____________________极;
②电极b上发生的电极反应为____________________;
③列式计算电极b上生成的气体在标准状况下的体积:________________;
④电极c的质量变化是__________g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:甲溶液______________________________;乙溶液______________________________;丙溶液______________________________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么? ________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知质子数或中子数为奇数的原子核才有NMR现象,而质子数和中子数均为偶数的原子不产生核核磁共振,下列原子组一定能产生NMR现象的是( )
A. 18O、31P、119Sn B. 27Al、19F、12C
C. 6C、16S、9F D. 1H、13C、35Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com