
科目: 来源: 题型:
【题目】I .短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为![]() 。
。
W | X | Y |
Z |
请回答下列问题:
(1)Z元素在元素周期表中的位置是________________________________________。
(2)X、Y、Z三种元素的原子半径由大到小的顺序为_________________(元素符号表示)。
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为____________(用化学式表示)
(4)用电子式表示WY2的形成过程:__________________________________。
(5)写出W单质与浓硫酸反应的化学方程式:__________________________________。
Ⅱ.A、B、C三种物质存在如图转化关系。

(1)若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________。
(2)向B溶液中滴加铁氯化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组中两个化学反应,属于同一反应类型的一组是 ()
A.由苯制溴苯;由乙酸与乙醇制取乙酸乙酯
B.由乙烯制1,2-二溴乙烷;由乙烷制一氯乙烷
C.乙烯使溴水褪色;乙烯使酸性高锰酸钾溶液褪色
D.由溴乙烷制取乙烯;由苯制取环己烷
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行探究。
I.鉴别NaCl和NaNO2。
(1)用pH试纸分别测定0.1mol/L两种盐溶液的pH,测得NaNO2呈碱性。该溶液呈碱性的原因是_____________________________________(用离子方程式解释)。
(2)已知:Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10。分别向盛有5mL0.0001mol/L两种盐溶液的试管中逐滴滴加0.0001mol/L的硝酸银溶液,先生成沉淀的是装有____________溶液的试管。
(3)已知:2NaNO2+4HI==2NaI+I2+2NO↑+2H2O。根据这一反应,可以用试剂和生活中的常见物质鉴别亚硝酸钠和食盐,进行实验时,必须选用的物质有____________(填选项字母)
A.自来水 B.碘化钾溶液 C.淀粉 D.白糖 E.食醋 F.白酒
Ⅱ.NaNO2与酸反应。
已知:NO+NO2+2NaOH=2NaNO2+H2O。某同学据此认为NaNO2可与硫酸反应,且有NO和NO2生成,并欲用如图所示仪器 (夹持装置己省略)及药品,验证自己的假设。已知沸点:NO2为21℃,NO为-151℃。
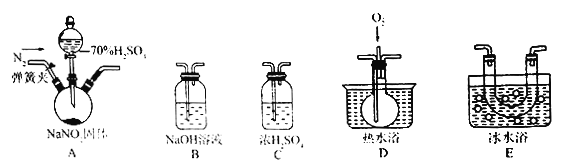
(1)按气流从左到右的方向,上述装置的连接顺序为A→___________→B。
(2)反应前,先打开弹簧夹,通入一段时间氮气,其目的是___________________________。
(3)关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生了红棕色气体。
①依据__________现象,可确认产物中有NO。
②裝置E的作用是______________________ 。
(4)如果没有装置C,对实验结论的影响是______________________________________。
(5)综合以上信息推断,NO2与NaOH溶液发生反应的化学方程式为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】强酸溶液A与强碱溶液B,在常温下其pH之和为15,当它们按一定体积比混合时,溶液的pH恰好为7,则A与B的体积比为
A. 1 : 1 B. 2 : 1 C. 1 : 10 D. 10 : 1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关有机化合物的说法正确的是
A. CH3CH==CHCH3分子中所有原子在一个平面上
B. ![]() 的同分异构体中,苯环上的一氯代物只有一种的结构有3种
的同分异构体中,苯环上的一氯代物只有一种的结构有3种
C. CH2=CHCH2OH能发生加成发应、取代反应、氧化反应等
D. 结构为…—CH==CH—CH==CH—CH==CH—CH==CH—…的高分子化合物,其单体是乙烯
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式碳酸铜可用于生产木材防腐剂等。工业上可用微蚀刻废液(含有一定量Cu2+、H+、SO42-、H2O2和微量Fe3+)制备高纯度碱式碳酸铜,其制备过程如下:
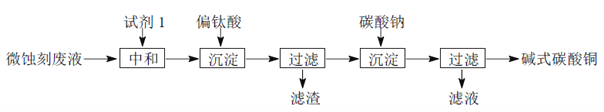
(1)试剂1最好选用________________。
a.Fe2O3 b.CaCO3 C.CuO
(2)加入Na2CO3沉淀前须除去Fe3+,否则Fe2(SO4)3会与Na2CO3反应,产生一种气体,同时生成NaFe3(OH)6(SO4)2沉淀,影响产品质量,写出该反应的化学方程式______________________。
(3)加入Na2CO3沉淀时,反应液pH对产品中SO42-的含量以及反应液中Cu2+沉淀效率的影响如下图所示,第二次沉淀时溶液pH最好控制在___________________________。

(4)所制得的碱式碳酸铜的组成可表示为:xCuCO3·yCu(OH)2·zH2O,要测定其组成,甲同学设计的实验方案中需要如下五个步骤:①称取12.0克的样品;②高温分解;③测出生成CO2的质量为2.2克;④测出生成水蒸气的质量为1.8克;⑤称量生成CuO的质量为8.0克。而乙同学认为除步骤②外,实验只需测定四个量中的部分数据即可,则合理的组合为______________(填序号,写一组即可)。根据你的选择,计算出碱式碳酸铜的组成,写出计算过程。____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】1 L某待测液中除含有0.2mol L的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl-、Br-、CO32-、HCO3-、SO32-、SO42- |
现进行如下实验操作(每次实验所加试剂均过量):

已知:无色气体D为单一气体。 请回答下列问题:
(1)气体B为_________(填化学式),白色沉淀E为________________(填化学式)。
(2)待测液中肯定存在的阴离子有______________________。
(3)写出生成白色沉淀B的离子方程式:_________________________________。
(4)判断原溶液中K+是否存在,若存在,其物质的量浓度的最小值为多少;若不存在,请说明理由:_________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组以粗镍(含少量Fe和Cr杂质)为原料制备Ni(NH3)6Cl2,并测定相关组分的含量。制备流程示意图如下:

已知:①部分离子生成氢氧化物沉淀的pH(开始沉淀的pH按离子浓度为0.1 molL-1计算)如下表所示:
离子 | Fe3+ | Cr3+ | Ni2+ |
开始沉淀的pH | 1.5 | 4.3 | 6.9 |
完全沉淀的pH | 2.8 | 5.6 | 8.9 |
②Ni(OH)2为绿色难溶物。Ni(NH3)6(NO3)2、Ni(NH3)6Cl2均为可溶于水的蓝紫色晶体,水溶液均显碱性。
请回答下列问题:
(1)实验需要配制250 mL 3.0 mol L-1的稀硝酸,需要的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管和_______________________。
(2)步骤(a)中Ni和浓硝酸反应的化学方程式为__________________________________。
(3)步骤(b)首先加入试剂X调节溶液的pH约为6,原因是_______________________________,过滤后再继续加入X调节pH以得到绿色沉淀。
(4)NH3含量的测定: [已知:Ni(NH3)6Cl2+6HC1==NiCl2+6NH4Cl]。
i.用电子天平称量m g产品于锥形瓶中,用25 mL水溶解后加入3.00mL 6 mol/L的盐酸,以甲基橙作指示剂,滴定至终点消耗0.5000 molL-1的NaOH标准溶液V1mL;
ii.空白试验:不加入样品重复实验i,消耗NaOH标准溶液V2mL。
①NH3的质量分数为______________(用含V1、V2、m的代数式表示)。
②在上述方案的基础上,下列措施能进—步提高测定准确度的有_______________(填选项字母)。
A.适当提高称量产品的质量 B.用H2SO4溶液替代盐酸
C.用酚酞替代甲基橙 D.进行平行实验
(5)为测定Cl-的含量,请补充完整下述实验方案。
称量m g产品于锥形瓶中,用25 mL水溶解,___________,滴入23滴K2CrO4溶液作指示剂,用已知浓度的AgNO3标准溶液滴定至终点,记录读数,重复操作23次。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定体积的容器中,加入1.5摩氙气和7.5摩氟气,于400℃和2633千帕压强下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5摩氟气.则所得无色晶体产物中,氙与氟的原子个数比是( )
A.1:2
B.1:3
C.1:4
D.1:6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com